按要求填空
(一)X、Y和Z均为短周期元素,原子序数依次增大,X的单质为密度最小的气体,Y的一种单质具有特殊臭味,Z与X原子最外层电子数相同。回答下列问题:
(1)由上述元素组成的化合物中,既含有极性共价键又含有离子键的化合物的电子式______ ;
(2)X和Y组成的化合物中,有一种既含有极性共价键又含有非极性共价键。此化合物可将碱性工业废水中的CNˉ氧化为碳酸盐和氨,相应的离子方程式为______ 。
(二)在一定条件下,RO 和Iˉ发生反应,离子方程式为:RO
和Iˉ发生反应,离子方程式为:RO +6Iˉ+6H+═Rˉ+3I2+3H2O
+6Iˉ+6H+═Rˉ+3I2+3H2O
RO 中R元素的化合价为
中R元素的化合价为______ ,R元素的原子最外层电子有______ 个。
(三)Na2Sx在碱性溶液中可被NaClO氧化为Na2SO4,而NaClO被还原为NaCl,若反应中Na2Sx与NaClO的物质的量之比为1:16,则x值是______ 。
(四)已知M2O 可与R2ˉ作用,R2ˉ被氧化为R的单质,M2O
可与R2ˉ作用,R2ˉ被氧化为R的单质,M2O 的还原产物中,M为+3价,又知c(M2O
的还原产物中,M为+3价,又知c(M2O )=0.3mol/L的溶液100mL可与c(R2ˉ)=0.6mol/L的溶液150mL恰好完全反应,则n值为
)=0.3mol/L的溶液100mL可与c(R2ˉ)=0.6mol/L的溶液150mL恰好完全反应,则n值为______ 。
(一)X、Y和Z均为短周期元素,原子序数依次增大,X的单质为密度最小的气体,Y的一种单质具有特殊臭味,Z与X原子最外层电子数相同。回答下列问题:
(1)由上述元素组成的化合物中,既含有极性共价键又含有离子键的化合物的电子式
(2)X和Y组成的化合物中,有一种既含有极性共价键又含有非极性共价键。此化合物可将碱性工业废水中的CNˉ氧化为碳酸盐和氨,相应的离子方程式为
(二)在一定条件下,RO
 和Iˉ发生反应,离子方程式为:RO
和Iˉ发生反应,离子方程式为:RO +6Iˉ+6H+═Rˉ+3I2+3H2O
+6Iˉ+6H+═Rˉ+3I2+3H2ORO
 中R元素的化合价为
中R元素的化合价为(三)Na2Sx在碱性溶液中可被NaClO氧化为Na2SO4,而NaClO被还原为NaCl,若反应中Na2Sx与NaClO的物质的量之比为1:16,则x值是
(四)已知M2O
 可与R2ˉ作用,R2ˉ被氧化为R的单质,M2O
可与R2ˉ作用,R2ˉ被氧化为R的单质,M2O 的还原产物中,M为+3价,又知c(M2O
的还原产物中,M为+3价,又知c(M2O )=0.3mol/L的溶液100mL可与c(R2ˉ)=0.6mol/L的溶液150mL恰好完全反应,则n值为
)=0.3mol/L的溶液100mL可与c(R2ˉ)=0.6mol/L的溶液150mL恰好完全反应,则n值为
更新时间:2016-12-08 20:58:27
|
相似题推荐
填空题
|
较难
(0.4)
【推荐1】某无色透明溶液中可能大量存在Ag+、Mg2+、Cu2+、Fe3+、Na+中的几种,请填写下列空白:
(1)不做任何实验就可以肯定原溶液中不存在的离子是______________ .
(2)取少量原溶液,加入过量稀盐酸,有白色沉淀生成;再加入过量的稀硝酸,沉淀不消失.说明原溶液中,肯定存在的离子是______________ ,有关的离子方程式为______________ .
(3)取(2)中的滤液,加入过量的NaOH溶液,出现白色沉淀,说明原溶液中肯定有__________ ,有关的离子方程式为__________ .
(1)不做任何实验就可以肯定原溶液中不存在的离子是
(2)取少量原溶液,加入过量稀盐酸,有白色沉淀生成;再加入过量的稀硝酸,沉淀不消失.说明原溶液中,肯定存在的离子是
(3)取(2)中的滤液,加入过量的NaOH溶液,出现白色沉淀,说明原溶液中肯定有
您最近半年使用:0次
填空题
|
较难
(0.4)
【推荐2】某待测液中可能含有大量Mg2+、Cu2+、Fe3+、K+、H+、NO3-、OH-离子中的一种或几种,现通过以下实验进行检验:
(1)取少量待测液,仔细观察,呈无色;
(2)向上述待测液中滴加NaOH溶液,先无明显现象,后有白色沉淀生成,
(3)向上述溶液中加入BaCl2溶液,无现象。
据此可以判断该待测液中一定大量存在的离子是___________ ,一定不能大量存在的离子是__________ ,不能确定是否存在的离子是___________ ,依次写出(2)中加入氢氧化钠后的离子反应:____________ ,___________ 。
(1)取少量待测液,仔细观察,呈无色;
(2)向上述待测液中滴加NaOH溶液,先无明显现象,后有白色沉淀生成,
(3)向上述溶液中加入BaCl2溶液,无现象。
据此可以判断该待测液中一定大量存在的离子是
您最近半年使用:0次
填空题
|
较难
(0.4)
名校
解题方法
【推荐3】 常用作陶瓷材料,可由锆英砂(主要成分为
常用作陶瓷材料,可由锆英砂(主要成分为 ,也可表示为
,也可表示为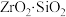 ,还含少量
,还含少量 等杂质)通过如图方法制取。
等杂质)通过如图方法制取。

已知:① 能与烧碱反应生成可溶于水的
能与烧碱反应生成可溶于水的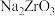 ,
,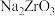 与酸反应生成
与酸反应生成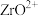 。
。
②部分金属离子在实验条件下开始沉淀和完全沉淀的 如表。
如表。
(1)熔融时 发生反应的化学方程式为
发生反应的化学方程式为_______ ,滤渣Ⅰ的化学式为_______ 。
(2)滤液Ⅰ中除 外还含金属的阳离子有
外还含金属的阳离子有_______ ,为使滤液Ⅰ的杂质离子沉淀完全,需用氨水调 ,则a的范围是
,则a的范围是_______ 。
(3)继续加氨水至 时,所发生反应的离子方程式为
时,所发生反应的离子方程式为_______ 。
(4)向过滤Ⅲ所得滤液中加入 粉末并加热,得到两种气体。该反应的离子方程式为
粉末并加热,得到两种气体。该反应的离子方程式为_______ 。
(5)为得到纯净的 ,
,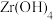 需要洗涤,检验
需要洗涤,检验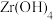 是否洗涤干净的方法是
是否洗涤干净的方法是_______ 。
 常用作陶瓷材料,可由锆英砂(主要成分为
常用作陶瓷材料,可由锆英砂(主要成分为 ,也可表示为
,也可表示为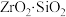 ,还含少量
,还含少量 等杂质)通过如图方法制取。
等杂质)通过如图方法制取。
已知:①
 能与烧碱反应生成可溶于水的
能与烧碱反应生成可溶于水的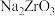 ,
,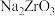 与酸反应生成
与酸反应生成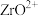 。
。②部分金属离子在实验条件下开始沉淀和完全沉淀的
 如表。
如表。| 金属离子 |  | 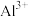 | 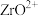 |
开始沉淀时 | 1.9 | 3.3 | 6.2 |
沉淀完全时 | 3.2 | 5.2 | 8.0 |
 发生反应的化学方程式为
发生反应的化学方程式为(2)滤液Ⅰ中除
 外还含金属的阳离子有
外还含金属的阳离子有 ,则a的范围是
,则a的范围是(3)继续加氨水至
 时,所发生反应的离子方程式为
时,所发生反应的离子方程式为(4)向过滤Ⅲ所得滤液中加入
 粉末并加热,得到两种气体。该反应的离子方程式为
粉末并加热,得到两种气体。该反应的离子方程式为(5)为得到纯净的
 ,
,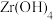 需要洗涤,检验
需要洗涤,检验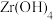 是否洗涤干净的方法是
是否洗涤干净的方法是
您最近半年使用:0次
填空题
|
较难
(0.4)
【推荐1】碘化亚铜(Cu2I2)是一种不溶于水也不溶于酸的白色固体,用途很广泛。
完成下列填空:
(1)碘化钾溶液中滴加适量硫酸铜溶液,就能得到碘化亚铜。请完成并配平上述反应:
____ KI+____ CuSO4→ ____ I2+____ Cu2I2↓+ ____________
该反应中氧化剂与还原剂的物质的量之比为___________ 。
(2)往上述反应后溶液中加入淀粉,溶液变蓝,再滴加亚硫酸溶液,蓝色又褪去。
写出KI、Cu2I2、H2SO3的还原性由强到弱的顺序是____________________ 。
(3)碘化亚铜能用于检测空气中的汞蒸气,其反应为:
2Cu2I2+Hg → Cu2HgI4(玫瑰红)+ 2Cu
产物Cu2HgI4中,Cu元素显____ 价。
当有1 molCu2I2参与反应时,转移电子____ mol。
(4)为除去稀盐酸中少量CuCl2杂质,可往溶液中加入过量的M试剂后进行过滤操作,再通入适量的Cl2后进行N操作。试剂M和操作N的组合正确的是_____ (选填编号)
完成下列填空:
(1)碘化钾溶液中滴加适量硫酸铜溶液,就能得到碘化亚铜。请完成并配平上述反应:
该反应中氧化剂与还原剂的物质的量之比为
(2)往上述反应后溶液中加入淀粉,溶液变蓝,再滴加亚硫酸溶液,蓝色又褪去。
写出KI、Cu2I2、H2SO3的还原性由强到弱的顺序是
(3)碘化亚铜能用于检测空气中的汞蒸气,其反应为:
2Cu2I2+Hg → Cu2HgI4(玫瑰红)+ 2Cu
产物Cu2HgI4中,Cu元素显
当有1 molCu2I2参与反应时,转移电子
(4)为除去稀盐酸中少量CuCl2杂质,可往溶液中加入过量的M试剂后进行过滤操作,再通入适量的Cl2后进行N操作。试剂M和操作N的组合正确的是
| 选项 | 试剂M | 操作N |
| a | 碘化钾溶液 | 升华 |
| b | 氢碘酸溶液 | 萃取分液 |
| c | 氢气 | 过滤 |
| d | 氢硫酸溶液 | 过滤 |
您最近半年使用:0次
填空题
|
较难
(0.4)
【推荐2】根据反应①~④四个反应,回答下列问题:
①H2S+I2=S+2HI
②2FeCl2+Cl2=2FeCl3
③Cu+2H2SO4(浓)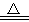 CuSO4+SO2↑+2H2O
CuSO4+SO2↑+2H2O
④Cl2+2KI=2KCl+I2
(1)反应①的反应类型为(填序号)_________ 。
(2)对于反应②,还原剂与氧化剂的物质的量之比为________ 。
(3)对于反应③,用双线桥法标明电子转移的方向和数目________________________ ,
(4)写出反应④的离子方程式_________________________ 。
①H2S+I2=S+2HI
②2FeCl2+Cl2=2FeCl3
③Cu+2H2SO4(浓)
 CuSO4+SO2↑+2H2O
CuSO4+SO2↑+2H2O④Cl2+2KI=2KCl+I2
(1)反应①的反应类型为(填序号)
| A.置换反应 | B.复分解反应 |
| C.化合反应 | D.氧化还原反应 |
(2)对于反应②,还原剂与氧化剂的物质的量之比为
(3)对于反应③,用双线桥法标明电子转移的方向和数目
(4)写出反应④的离子方程式
您最近半年使用:0次
填空题
|
较难
(0.4)
【推荐3】实验室可由软锰矿(主要成分为 MnO2)制备 KMnO4,方法如下:软锰矿与过量固体 KOH和 KClO3在高温下反应,生成锰酸钾(K2MnO4)和 KCl;用水溶解,滤去残渣,滤液酸化后,K2MnO4转变为MnO2和KMnO4;滤去MnO2沉淀,浓缩滤液,结晶得到深紫色的针状KMnO4请回答:
(1)软锰矿制备K2MnO4的化学方程式是_______ 。
(2)K2MnO4制备KMnO4的离子方程式是_______ 。
(3)配平氧化还原反应方程式:_ C2O +_MnO
+_MnO +_H+=_CO2+_Mn2++_H2O
+_H+=_CO2+_Mn2++_H2O
_______
(4)称取6.0 g含H2C2O4·2H2O、KHC2O4和K2SO4的试样,加水溶解,配成250mL溶液。量取两份此溶液各25.00 mL,分别置于两个锥形瓶中。
①第一份溶液中加入酚酞试液,滴加0.25 mol·L-1NaOH溶液至20.00 mL时,溶液由无色变为浅红色。该溶液被中和的H+的物质的量为___ mol。
②第二份溶液中滴加0.10 mol·L-1的酸性高锰酸钾溶液至16.00 mL时反应完全,此时溶液颜色由__ 变为__ 。该溶液中还原剂的物质的量为___ mol。
③原试样中H2C2O4·2H2O的质量分数为_____ 。
(1)软锰矿制备K2MnO4的化学方程式是
(2)K2MnO4制备KMnO4的离子方程式是
(3)配平氧化还原反应方程式:_ C2O
 +_MnO
+_MnO +_H+=_CO2+_Mn2++_H2O
+_H+=_CO2+_Mn2++_H2O(4)称取6.0 g含H2C2O4·2H2O、KHC2O4和K2SO4的试样,加水溶解,配成250mL溶液。量取两份此溶液各25.00 mL,分别置于两个锥形瓶中。
①第一份溶液中加入酚酞试液,滴加0.25 mol·L-1NaOH溶液至20.00 mL时,溶液由无色变为浅红色。该溶液被中和的H+的物质的量为
②第二份溶液中滴加0.10 mol·L-1的酸性高锰酸钾溶液至16.00 mL时反应完全,此时溶液颜色由
③原试样中H2C2O4·2H2O的质量分数为
您最近半年使用:0次
填空题
|
较难
(0.4)
【推荐1】化学用语是学习化学的基本工具,是高中化学的重要内容,请根据要求用合适的化学用语填空:
(1)从分子结构上来看,氮与碳有很多对应的物质(如CH4和NH3对应),请找出下列含碳化合物对应的含氮物质(填写化学式):H2CO3_____ ;C2H2_____ 。
(2)已知Fe元素在化合物里通常显+2或+3价,因此Fe3O4可写成氧化物形式FeO·Fe2O3,或盐的形式Fe(FeO2)2,它属于偏铁酸盐。Pb在化合物里显+2价或+4价,那么Pb3O4也可以写成_____ 或_____ 。(填写化学式)
(3)在法庭医学分析上常用马氏砷法来证明受害者是否为砒霜(As2O3)中毒。用锌和盐酸与试样混合在一起,若试样中有砒霜,就会发生反应生成砷化氢(AsH3)、锌盐溶液。写出该反应的化学方程式_____ 。
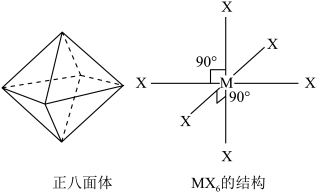
(4)某化合物MX6分子呈正八面体形式(如图所示)。由于六个X原子与M的连接完全对称,因此将任意一个X用Y原子替换均只能得到一种结构的MX5Y。按此思路,若将其中任意两个X原子用Y原子替换,请画出化学式为MX4Y2的各种结构_____ 。
(1)从分子结构上来看,氮与碳有很多对应的物质(如CH4和NH3对应),请找出下列含碳化合物对应的含氮物质(填写化学式):H2CO3
(2)已知Fe元素在化合物里通常显+2或+3价,因此Fe3O4可写成氧化物形式FeO·Fe2O3,或盐的形式Fe(FeO2)2,它属于偏铁酸盐。Pb在化合物里显+2价或+4价,那么Pb3O4也可以写成
(3)在法庭医学分析上常用马氏砷法来证明受害者是否为砒霜(As2O3)中毒。用锌和盐酸与试样混合在一起,若试样中有砒霜,就会发生反应生成砷化氢(AsH3)、锌盐溶液。写出该反应的化学方程式
(4)某化合物MX6分子呈正八面体形式(如图所示)。由于六个X原子与M的连接完全对称,因此将任意一个X用Y原子替换均只能得到一种结构的MX5Y。按此思路,若将其中任意两个X原子用Y原子替换,请画出化学式为MX4Y2的各种结构

您最近半年使用:0次
填空题
|
较难
(0.4)
【推荐2】A~I都是由短周期元素组成的常见物质,它们之间的转化关系如下图所示。已知:A为气体,其水溶液呈碱性;D、F均能与人体血液中的血红蛋白结合而使人中毒;E可作为半导体材料。

(1)化合物A的电子式为__________ 。
氧化物I中化学键类型:___________ 。
组成E单质的元素在元素周期表中的位置是________________ 。
图中物质所含元素原子的半径由大到小依次是(写元素符号)_____________ 。
(2)反应④的化学方程式为_________________________ 。
(3)将F与B按体积比2:1混合生成气体M,常温下测定M相对分子质量时,得到的实验值总是比理论值偏大,其原因是(用化学方程式表示)____________ 。
(4)某容积为V L的试管中充满F气体(标准状况下),若将该气体完全被水吸收,需通入B的物质的量为(写含V的表达式)_________ mol,此时所得溶液中再通入气体A,恰好完全反应后所得溶液中各离子浓度由大到小依次为:______________ 。

(1)化合物A的电子式为
氧化物I中化学键类型:
组成E单质的元素在元素周期表中的位置是
图中物质所含元素原子的半径由大到小依次是(写元素符号)
(2)反应④的化学方程式为
(3)将F与B按体积比2:1混合生成气体M,常温下测定M相对分子质量时,得到的实验值总是比理论值偏大,其原因是(用化学方程式表示)
(4)某容积为V L的试管中充满F气体(标准状况下),若将该气体完全被水吸收,需通入B的物质的量为(写含V的表达式)
您最近半年使用:0次
填空题
|
较难
(0.4)
【推荐3】铜、镓、硒、硅等元素的化合物是生产第三代太阳能电池的重要材料。请回答:
(1)基态铜原子的电子排布式为________________;已知高温下CuO→Cu2O+O2,从铜原子价层电子结构(3d和4s轨道上应填充的电子数)变化角度来看,能生成Cu2O的原因是____________________。
(2)硒、硅均能与氢元素形成气态氢化物,若“Si-H”中共用电子对偏向氢元素,氢气与硒反应时单质硒是氧化剂,则硒与硅的电负性相对大小为Se___________Si(填“>”、“<”)。与Si同周期部分元素的电离能如下图所示,其中a、b和c分别代表____________。

A.a为Il、b为I2、c为I3B.a为I2、b为I3、c为I1
C.a为I3、b为I2、c为I1D.a为Il、b为I3、c为I2
(3) SeO2常温下白色晶体,熔点为340~350℃,315℃时升华,则SeO2固体的晶体类型为____________;若SeO2类似于SO2是V型分子,则Se原子外层轨道的杂化类型为_____________。
(4)镓与某有机物形成的配合物过程如下图(左),在图上画出产物中的配位键。

(5)金刚砂(SiC)的硬度为9.5,其晶胞结构如上图(右)所示,则Si原子的配位数为___________,每个C原子周围最近的C原子数目为___________个;若晶胞的边长为a pm,则金刚砂的密度表达式为___________g/cm3。
(1)基态铜原子的电子排布式为________________;已知高温下CuO→Cu2O+O2,从铜原子价层电子结构(3d和4s轨道上应填充的电子数)变化角度来看,能生成Cu2O的原因是____________________。
(2)硒、硅均能与氢元素形成气态氢化物,若“Si-H”中共用电子对偏向氢元素,氢气与硒反应时单质硒是氧化剂,则硒与硅的电负性相对大小为Se___________Si(填“>”、“<”)。与Si同周期部分元素的电离能如下图所示,其中a、b和c分别代表____________。

A.a为Il、b为I2、c为I3B.a为I2、b为I3、c为I1
C.a为I3、b为I2、c为I1D.a为Il、b为I3、c为I2
(3) SeO2常温下白色晶体,熔点为340~350℃,315℃时升华,则SeO2固体的晶体类型为____________;若SeO2类似于SO2是V型分子,则Se原子外层轨道的杂化类型为_____________。
(4)镓与某有机物形成的配合物过程如下图(左),在图上画出产物中的配位键。

(5)金刚砂(SiC)的硬度为9.5,其晶胞结构如上图(右)所示,则Si原子的配位数为___________,每个C原子周围最近的C原子数目为___________个;若晶胞的边长为a pm,则金刚砂的密度表达式为___________g/cm3。
您最近半年使用:0次



