亚硫酰氯( )在医药、农药合成领域有广泛的应用。
)在医药、农药合成领域有广泛的应用。
(1) 含有S、O、Cl三种元素,其中位于元素周期表中第二周期的元素是
含有S、O、Cl三种元素,其中位于元素周期表中第二周期的元素是_______ 。
(2)Cl的非金属性强于S的非金属性。
①用原子结构解释:Cl和S位于元素周期表中同一周期,原子核外电子层数相同,核电荷数Cl大于S,原子半径_______ ,得电子能力Cl强于S。
②用实验事实验证:将 通入
通入 溶液中,生成淡黄色沉淀。淡黄色沉淀是
溶液中,生成淡黄色沉淀。淡黄色沉淀是_______ 。
(3)下列关于 的说法正确的是
的说法正确的是_______ (填字母)。
a.属于化合物 b.摩尔质量为119 g·mol
 )在医药、农药合成领域有广泛的应用。
)在医药、农药合成领域有广泛的应用。(1)
 含有S、O、Cl三种元素,其中位于元素周期表中第二周期的元素是
含有S、O、Cl三种元素,其中位于元素周期表中第二周期的元素是(2)Cl的非金属性强于S的非金属性。
①用原子结构解释:Cl和S位于元素周期表中同一周期,原子核外电子层数相同,核电荷数Cl大于S,原子半径
②用实验事实验证:将
 通入
通入 溶液中,生成淡黄色沉淀。淡黄色沉淀是
溶液中,生成淡黄色沉淀。淡黄色沉淀是(3)下列关于
 的说法正确的是
的说法正确的是a.属于化合物 b.摩尔质量为119 g·mol

更新时间:2023-04-12 09:35:58
|
相似题推荐
填空题
|
较易
(0.85)
名校
【推荐1】按要求回答下列问题
(1)金属钙在一定条件下可以与氢气化合生成CaH2(白色固体)。将该白色固体加入滴有酚酞的蒸馏水中,可以观察到有气泡生成,溶液变红。请根据以上事实书写CaH2与水反应的化学方程式,并用单线桥出电子转移方向和数目_______ 。
(2)设NA代表阿伏加德罗常数的数值,一个CO分子的质量可表示为_______ g。
(1)金属钙在一定条件下可以与氢气化合生成CaH2(白色固体)。将该白色固体加入滴有酚酞的蒸馏水中,可以观察到有气泡生成,溶液变红。请根据以上事实书写CaH2与水反应的化学方程式,并用单线桥出电子转移方向和数目
(2)设NA代表阿伏加德罗常数的数值,一个CO分子的质量可表示为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】回答下列问题:
(1)现有下列八种物质:①NaOH溶液②铁丝③液态HCl④熔融氯化钠⑤硫酸钠固体⑥CO2⑦酒精⑧生石灰。上述物质中,属于非电解质的是_____ (填序号,下同)。上述物质中,属于电解质但不导电的是_______
(2) 0.1mol的N2H4气体和0.2molNH3气体,它们在同温、同压下的体积比是______ 。所含的原子数比是________ 。
(3)12.4 克Na2R中含Na+0.4mol,则Na2R摩尔质量为_______ 。
(4)相同条件下,CO2和O2的混合气体相对于氢气的密度为20, 则CO2和O2的体积之比V(CO2):V(O2)=_____ 。
(1)现有下列八种物质:①NaOH溶液②铁丝③液态HCl④熔融氯化钠⑤硫酸钠固体⑥CO2⑦酒精⑧生石灰。上述物质中,属于非电解质的是
(2) 0.1mol的N2H4气体和0.2molNH3气体,它们在同温、同压下的体积比是
(3)12.4 克Na2R中含Na+0.4mol,则Na2R摩尔质量为
(4)相同条件下,CO2和O2的混合气体相对于氢气的密度为20, 则CO2和O2的体积之比V(CO2):V(O2)=
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】元素在周期表中的位置,反映了元素的原子结构和元素的性质,右图是元素周期表的一部分。
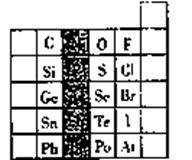
(1)阴影部分元素在元素周期表中的位置为第_________ 族。根据元素周期律、预测;酸性强弱H3AsO4______ H3PO4(用“>”或“<”表示)
(2)元素S的最高正价和最低负价的代数和为________ ,在一定条件下,S与H2反应有一定限度(可理解为反应进行的程度)。请判断:在相同条件下Se与H2反应的限度比S与H2反应限度____________ 。(选填“更大”、“更小”或“相同”)
(3)Br2具有较强的氧化性,SO2具有较强的还原性,将SO2气体通入溴水后,溶液中存在的主要离子是__________
(4)下列说法正确的是__________
A.C、N、O、F的原子半径随着原子数的增大而减小
B.Si、P、S、Cl元素的非金属性随着核电荷数的增加而增强
C.干冰升华、液态水转变为气态都要克服分子内的共价键
D.HF、HCl、HBr、HI的热稳定性依次减弱

(1)阴影部分元素在元素周期表中的位置为第
(2)元素S的最高正价和最低负价的代数和为
(3)Br2具有较强的氧化性,SO2具有较强的还原性,将SO2气体通入溴水后,溶液中存在的主要离子是
(4)下列说法正确的是
A.C、N、O、F的原子半径随着原子数的增大而减小
B.Si、P、S、Cl元素的非金属性随着核电荷数的增加而增强
C.干冰升华、液态水转变为气态都要克服分子内的共价键
D.HF、HCl、HBr、HI的热稳定性依次减弱
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】(1) 指出下列元素在周期表中的位置:硅在第_____ 周期第______ 族;氟在第_____ 周期第______ 族。
(2)写出下列物质的电子式:
氮气________ ;氯化镁_________ ;二氧化碳_______ ;氟化氢______
(2)写出下列物质的电子式:
氮气
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】下表是元素周期律的一部分用元素符号或化学式、化学用语填空。
(1)在写出元素⑦的气态氢化物的电子式___ ;元素⑨的核外电子排布式为___ ;
(2)元素③的原子核外有___ 种能量不同的电子,有___ 种运动状态电子。
(3)元素⑧与⑥形成的晶体是___ 晶体:元素⑤和⑩形成的分子属于___ 分子(极性、非极性):
(4)写出元素②与④的最高价氧化物对应水化物之间反应的方程式___ ;
(5)元素⑨和⑩的非金属性比较更强___ (元素符号),用一个方程式说明这一结论___ 。
(6)关于氟、钠、镁、氯四种元素的性质递变规律,描述正确的是___ (写编号)。
a.原子半径:Na<Cl b.离子半径:F-<Mg2+
c.热稳定性:HF>HCl d.碱性:NaOH>Mg(OH)2
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ⑤ | ⑦ | ⑧ | ||||
| 3 | ② | ③ | ④ | ⑥ | ⑨ | ⑩ |
(1)在写出元素⑦的气态氢化物的电子式
(2)元素③的原子核外有
(3)元素⑧与⑥形成的晶体是
(4)写出元素②与④的最高价氧化物对应水化物之间反应的方程式
(5)元素⑨和⑩的非金属性比较更强
(6)关于氟、钠、镁、氯四种元素的性质递变规律,描述正确的是
a.原子半径:Na<Cl b.离子半径:F-<Mg2+
c.热稳定性:HF>HCl d.碱性:NaOH>Mg(OH)2
您最近一年使用:0次
【推荐1】五种元素的原子电子层结构如下:A.1s22s1;B.1s22s22p4;C.1s22s22p6;D.1s22s22p63s23p2;E.[Ar]3d104s1.(用元素符号作答)
(1)元素的性质最稳定的是_____ 。
(2)属于过渡元素的是_____ 。
(3)元素的非金属性最大的是_____ 。
(4)上述元素之间能形成X2Y型化合物的化学式是_____ 。
(1)元素的性质最稳定的是
(2)属于过渡元素的是
(3)元素的非金属性最大的是
(4)上述元素之间能形成X2Y型化合物的化学式是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】下表是元素周期表的一部分,请参照元素①~⑩在表中的位置,回答下列问题。
(1)②的原子结构示意图是_______ 。
(2)化学性质最不活泼的元素是_______ (填元素符号)。
(3)在③、④、⑤、⑥这些元素形成的最简单离子中,离子半径由大到小的顺序是_______ (填离子符号)。
(4)表中④⑧⑨元素的氢化物的稳定性最强的为_______ (填化学式)。
(5)表中元素⑤与元素⑥金属性更强的是_______ (填化学式),这两种元素的最高价氧化物对应的水化物之间反应的离子方程式为_______ ;
(6)元素③、⑤能形成两种化合物,其中较稳定的化合物的电子式为_______
(7)在这些元素的最高价氧化物对应的水化物中,酸性最强的物质的化学式为_______ ,碱性最强的物质的化学式为_______ 。
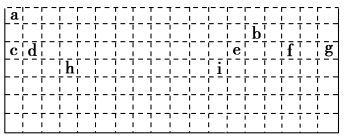
(8)下图是不完整的元素周期表,补全元素周期表的轮廓____________ 。
| 族周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 2 | ① | ② | ③ | ④ | ||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
(2)化学性质最不活泼的元素是
(3)在③、④、⑤、⑥这些元素形成的最简单离子中,离子半径由大到小的顺序是
(4)表中④⑧⑨元素的氢化物的稳定性最强的为
(5)表中元素⑤与元素⑥金属性更强的是
(6)元素③、⑤能形成两种化合物,其中较稳定的化合物的电子式为
(7)在这些元素的最高价氧化物对应的水化物中,酸性最强的物质的化学式为
(8)下图是不完整的元素周期表,补全元素周期表的轮廓

您最近一年使用:0次




