Ⅰ.为探究原电池和电解池的工作原理,某研究性小组分别用如图所示装置进行实验。
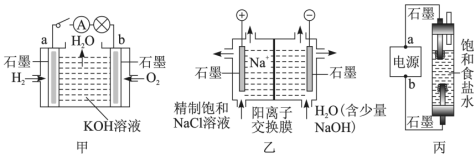
(1)甲装置中,a电极的反应式为___________ 。
(2)乙装置中,阴极区产物为___________ 。
(3)丙装置是一种家用环保型消毒液发生器。外接电源a为___________ (填“正”或“负”)极,该装置内发生反应的化学方程式为___________ 。
(4)若甲装置作为乙装置的电源,一段时间后,甲中消耗气体与乙中产生气体的物质的量之比为___________ (不考虑气体的溶解)。
Ⅱ.利用如图装置,可以模拟铁的电化学防护。
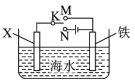
(5)若X为碳棒,为减缓铁的腐蚀,开关K应置于___________ 处。
(6)若X为锌,开关K置于M处,该电化学防护法称为___________ 。

(1)甲装置中,a电极的反应式为
(2)乙装置中,阴极区产物为
(3)丙装置是一种家用环保型消毒液发生器。外接电源a为
(4)若甲装置作为乙装置的电源,一段时间后,甲中消耗气体与乙中产生气体的物质的量之比为
Ⅱ.利用如图装置,可以模拟铁的电化学防护。

(5)若X为碳棒,为减缓铁的腐蚀,开关K应置于
(6)若X为锌,开关K置于M处,该电化学防护法称为
更新时间:2023-03-16 10:57:55
|
相似题推荐
【推荐1】某研究小组对铁钉生锈进行研究
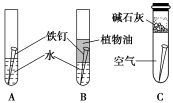
(1)经过较长时间后,甲同学观察到的现象是:上述图中的铁钉最容易生锈的是____ (填序号)。
(2)在铁钉的锈蚀过程中,Fe发生了____ (填“氧化”或“还原”反应)。
(3)铁生锈的外部条件是____ 。
(4)若为了防止铁钉生锈,该同学想在铁钉表面镀上一层金属,该金属最好是____ 。
A.锡 B.铜 C.锌
(5)水是一种宝贵的自然资源。下列做法会造成水污染的是_____ (填序号)。
①生活污水任意排放②海上油轮原油泄漏③水力发电④农药化肥不合理施用
向含Hg2+的废水中加入Na2S以除去Hg2+,该反应的离子方程式为_____ 。

(1)经过较长时间后,甲同学观察到的现象是:上述图中的铁钉最容易生锈的是
(2)在铁钉的锈蚀过程中,Fe发生了
(3)铁生锈的外部条件是
(4)若为了防止铁钉生锈,该同学想在铁钉表面镀上一层金属,该金属最好是
A.锡 B.铜 C.锌
(5)水是一种宝贵的自然资源。下列做法会造成水污染的是
①生活污水任意排放②海上油轮原油泄漏③水力发电④农药化肥不合理施用
向含Hg2+的废水中加入Na2S以除去Hg2+,该反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.64)
【推荐2】钢铁容易生锈的主要原因是因为钢铁在炼制过程中混有少量的碳杂质,在潮湿的空气中容易形成原电池,发生电化学腐蚀.金属发生电化学腐蚀时,可分为析氢腐蚀和吸氧腐蚀.两者的本质相同,该腐蚀过程中负极电极反应式为_____ ,但正极反应不同,析氢腐蚀的正极反应为_____ ,钢铁腐蚀主要是吸氧腐蚀,吸氧腐蚀的正极反应为_____ .
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】研究NOx、CO等大气污染气体的处理,对保护环境有重要的意义。回答下列问题:
(1)NOx与CO反应生成无污染气体的相关热化学方程式如下:①NO2(g)+CO(g) CO2(g)+NO(g) ΔH1=−234.0 kJ·mol−1,②N2(g) +O2(g)
CO2(g)+NO(g) ΔH1=−234.0 kJ·mol−1,②N2(g) +O2(g) 2NO(g)ΔH2=+179.5 kJ·mol−1,③2NO(g)+O2(g)
2NO(g)ΔH2=+179.5 kJ·mol−1,③2NO(g)+O2(g) 2NO2(g) ΔH3=−112.3 kJ·mol−1,反应2NO2(g) +4CO(g)
2NO2(g) ΔH3=−112.3 kJ·mol−1,反应2NO2(g) +4CO(g) N2(g)+4CO2(g)的ΔH=
N2(g)+4CO2(g)的ΔH=__________ kJ·mol−1。
(2)在一定温度下,向2 L的恒容密闭容器中充入4.0 mol NO2和4.0 mol CO,在催化剂作用下发生反应:2NO2(g)+4CO(g) N2(g) +4CO2(g),测得相关数据如下:
N2(g) +4CO2(g),测得相关数据如下:
①在0~10 min,用CO2的浓度变化表示的反应速率为______________ 。
②为使该反应的反应速率增大,下列措施中可采用的是________ (填字母代号)。
a.减小压强 b.适当升高温度 c.增大CO的浓度 d.选择高效催化剂
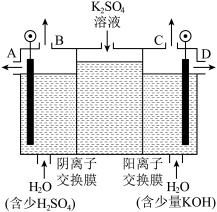
(3)如果模拟工业上离子交换膜法制烧碱的方法,那么可以设想用如图装置电解硫酸钾溶液来制取氢气、氧气、硫酸和氢氧化钾。
①该电解槽的阳极反应式为_______ 。此时通过阴离子交换膜的离子数____ (填“大于”“小于”或“等于”)通过阳离子交换膜的离子数。
②制得的氢氧化钾溶液从出口____ (填“A”“B”“C”或“D”)导出。
③若将制得的氢气、氧气和氢氧化钾溶液组合为氢氧燃料电池,则电池负极的电极反应式为_____ 。
(1)NOx与CO反应生成无污染气体的相关热化学方程式如下:①NO2(g)+CO(g)
 CO2(g)+NO(g) ΔH1=−234.0 kJ·mol−1,②N2(g) +O2(g)
CO2(g)+NO(g) ΔH1=−234.0 kJ·mol−1,②N2(g) +O2(g) 2NO(g)ΔH2=+179.5 kJ·mol−1,③2NO(g)+O2(g)
2NO(g)ΔH2=+179.5 kJ·mol−1,③2NO(g)+O2(g) 2NO2(g) ΔH3=−112.3 kJ·mol−1,反应2NO2(g) +4CO(g)
2NO2(g) ΔH3=−112.3 kJ·mol−1,反应2NO2(g) +4CO(g) N2(g)+4CO2(g)的ΔH=
N2(g)+4CO2(g)的ΔH=(2)在一定温度下,向2 L的恒容密闭容器中充入4.0 mol NO2和4.0 mol CO,在催化剂作用下发生反应:2NO2(g)+4CO(g)
 N2(g) +4CO2(g),测得相关数据如下:
N2(g) +4CO2(g),测得相关数据如下:| 0 min | 5 min | 10 min | 15 min | 20 min | |
| c(NO2)/mol·L−1 | 2.0 | 1.7 | 1.56 | 1.5 | 1.5 |
| c(N2)/mol·L−1 | 0 | 0.15 | 0.22 | 0.25 | 0.25 |
②为使该反应的反应速率增大,下列措施中可采用的是
a.减小压强 b.适当升高温度 c.增大CO的浓度 d.选择高效催化剂
(3)如果模拟工业上离子交换膜法制烧碱的方法,那么可以设想用如图装置电解硫酸钾溶液来制取氢气、氧气、硫酸和氢氧化钾。
①该电解槽的阳极反应式为
②制得的氢氧化钾溶液从出口
③若将制得的氢气、氧气和氢氧化钾溶液组合为氢氧燃料电池,则电池负极的电极反应式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】O3可由臭氧发生器(原理如图所示)电解稀硫酸制得。
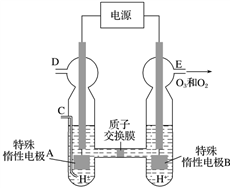
(1)图中阴极为________ (填“A”或“B”)。
(2)若C处不通入O 2 ,D、E处分别收集到11.2 L和 4.48 L 气体(标准状况下), 则E处收集的气体中O3所占的体积分数为
,D、E处分别收集到11.2 L和 4.48 L 气体(标准状况下), 则E处收集的气体中O3所占的体积分数为__________ (忽略O 3 的分解)。
(3)若C处通入O 2,则A极的电极反应式为________________________________________ 。

(1)图中阴极为
(2)若C处不通入O 2
 ,D、E处分别收集到11.2 L和 4.48 L 气体(标准状况下), 则E处收集的气体中O3所占的体积分数为
,D、E处分别收集到11.2 L和 4.48 L 气体(标准状况下), 则E处收集的气体中O3所占的体积分数为(3)若C处通入O 2,则A极的电极反应式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】如图所示,某同学设计一个甲醚燃料电池并探究氯碱工业原理和粗铜的精炼原理,其中乙装置中X为阳离子交换膜。

根据要求回答相关问题:
(1)写出负极的电极反应式_____________________________ 。
(2)铁电极为________ (填“阳极”或“阴极”),石墨电极(C)的电极反应式为________________ 。
(3)如果粗铜中含有锌、银等杂质,丙装置中反应一段时间,硫酸铜溶液浓度将____ (填“增大”、“ 减小”或“不变”)。
(4)若在标准状况下,有2.24L氧气参加反应,则丙装置中阴极析出铜的质量为______ 。假设乙装置中氯化钠溶液足够多,若在标准状况下,有224mL氧气参加反应,则乙装置中阳离子交换膜左侧溶液质量将____________ (填“增大”、“减小”或“不变”),且变化了_______ 克。
(5)若将乙装置中铁电极与石墨电极位置互换,其他装置不变,此时乙装置中发生的总反应式为_________________________________ 。

根据要求回答相关问题:
(1)写出负极的电极反应式
(2)铁电极为
(3)如果粗铜中含有锌、银等杂质,丙装置中反应一段时间,硫酸铜溶液浓度将
(4)若在标准状况下,有2.24L氧气参加反应,则丙装置中阴极析出铜的质量为
(5)若将乙装置中铁电极与石墨电极位置互换,其他装置不变,此时乙装置中发生的总反应式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】某同学用下图装置电解硫酸钾溶液来获得氧气、氢气、硫酸和氢氧化钾。
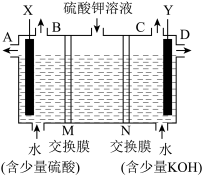
(1)X极与电源的________ (填“正”或“负”)极相连,氢气从________ (填“A”“B”“C”或“D”)口导出。
(2)离子交换膜只允许一类离子通过,则M为________ (填“阴离子”或“阳离子”,下同)交换膜,N为________ 交换膜,图中少量硫酸和少量氢氧化钾的作用是________________________________________ 。
(3)若将制得的氢气、氧气和氢氧化钾溶液组合为氢氧燃料电池(石墨为电极),则电池负极的电极反应式为______________________________________________ 。
(4)若使用铅蓄电池作电源完成上述电解,当制得11.2 L标准状况下的氢气时,理论上铅蓄电池消耗硫酸________ mol,正极板质量增加______ g,负极板质量增加________ g。

(1)X极与电源的
(2)离子交换膜只允许一类离子通过,则M为
(3)若将制得的氢气、氧气和氢氧化钾溶液组合为氢氧燃料电池(石墨为电极),则电池负极的电极反应式为
(4)若使用铅蓄电池作电源完成上述电解,当制得11.2 L标准状况下的氢气时,理论上铅蓄电池消耗硫酸
您最近一年使用:0次
填空题
|
适中
(0.65)
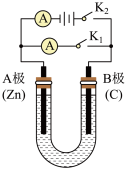
【推荐2】如图所示,U形管内盛有150mL的溶液,按要求回答下列问题:
(1)打开K2,闭合K1,若所盛溶液为稀硫酸,则B极为___________ 极(填电极名称),该装置的能量转化形式为:__________ ,B极的电极反应式为:______________________ 。
(2)打开K1,闭合K2,若所盛溶液为NaCl溶液,一段时间后U形管内溶液的pH___________ (填“变大”、“不变”或“变小”),总反应的化学方程式是:______________________ 。若要使U形管内溶液恢复到起始状态,应向U形管内的溶液加入(或通入)___________ 。
(3)如果要在铁块上镀上铜,打开K1,闭合K2,电解液选用CuSO4溶液,则A电极的材料应换成是___ (填“铁块”或“纯铜”),反应一段时间后电解质溶液中Cu2+的浓度将会_____ (填“增大”、“减小”或“不变”)。
(1)打开K2,闭合K1,若所盛溶液为稀硫酸,则B极为
(2)打开K1,闭合K2,若所盛溶液为NaCl溶液,一段时间后U形管内溶液的pH
(3)如果要在铁块上镀上铜,打开K1,闭合K2,电解液选用CuSO4溶液,则A电极的材料应换成是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】如图所示,某同学设计一个燃料电池并探究氯碱工业原理和电解 溶液,根据要求回答相关问题:
溶液,根据要求回答相关问题:
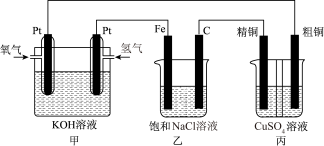
(1)通入氧气的电极为_______ (填“正极”或“负极”),铁电极为_______ (填“阳极”或“阴极”)
(2)正极的电极反应式为_______ 。
(3)乙装置中电解的总反应的离子方程式为_______ 。
(4)乙中装有2L饱和氯化钠溶液,若在标准状况下,有1.12L氧气参加反应,乙中溶液的pH=_______ ,丙装置中阴极增重的质量为_______ g。
(5)若将该燃料电池的燃料改为甲烷,则该极的电极反应式为_______ 。
 溶液,根据要求回答相关问题:
溶液,根据要求回答相关问题:
(1)通入氧气的电极为
(2)正极的电极反应式为
(3)乙装置中电解的总反应的离子方程式为
(4)乙中装有2L饱和氯化钠溶液,若在标准状况下,有1.12L氧气参加反应,乙中溶液的pH=
(5)若将该燃料电池的燃料改为甲烷,则该极的电极反应式为
您最近一年使用:0次



