以熔融盐( 、
、 )为电解液,以石墨为阳极,电解
)为电解液,以石墨为阳极,电解 和
和 获取电池材料
获取电池材料 ,下列说法正确的是
,下列说法正确的是
 、
、 )为电解液,以石墨为阳极,电解
)为电解液,以石墨为阳极,电解 和
和 获取电池材料
获取电池材料 ,下列说法正确的是
,下列说法正确的是A.阳极上 被还原 被还原 | B.阴极发生的反应为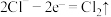 |
| C.电解时,阳离子向阳极移动 | D.理论上每生成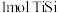 电路中转移 电路中转移 电子 电子 |
更新时间:2023/03/16 15:17:51
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】对氨基苯甲酸(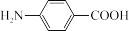 )是一种用途广泛的化工产品和医药中间体,以对硝基苯甲酸(
)是一种用途广泛的化工产品和医药中间体,以对硝基苯甲酸( )为原料,采用电解法合成对氨基苯甲酸的装置如图。
)为原料,采用电解法合成对氨基苯甲酸的装置如图。
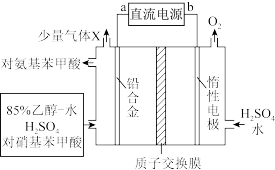
下列说法错误的是
 )是一种用途广泛的化工产品和医药中间体,以对硝基苯甲酸(
)是一种用途广泛的化工产品和医药中间体,以对硝基苯甲酸( )为原料,采用电解法合成对氨基苯甲酸的装置如图。
)为原料,采用电解法合成对氨基苯甲酸的装置如图。
下列说法错误的是
| A.b为直流电源正极 |
| B.少量气体X为H2 |
| C.质子交换膜中H+由左向右迁移 |
D.阴极的主要电极反应式为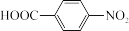 +6e-+6H+= +6e-+6H+=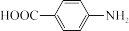 +2H2O +2H2O |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】化学反应原理在生产生活中有重要应用,下列说法不正确 的是
A.锅炉水垢中的 可先用 可先用 溶液处理后,再用酸去除 溶液处理后,再用酸去除 |
| B.在潮湿空气中,表面破损的镀锡铁皮比镀锌铁皮的腐蚀速率要快得多 |
| C.电解精炼铜时,若阳极质量减少64g,则转移到阴极的电子数为2mol |
D.铜片上镀银时,将铜片接在电源的负极上,用 溶液做电解质 溶液做电解质 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
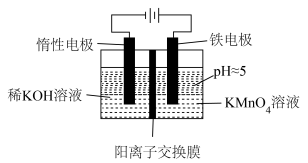
【推荐1】用如图装置处理含 的废液,使Mn元素转化为
的废液,使Mn元素转化为 沉淀,从而消除重金属污染,下列说法错误的是
沉淀,从而消除重金属污染,下列说法错误的是
 的废液,使Mn元素转化为
的废液,使Mn元素转化为 沉淀,从而消除重金属污染,下列说法错误的是
沉淀,从而消除重金属污染,下列说法错误的是 
| A.为了增大右侧溶液的导电性可以加稀硫酸造成强酸性环境 |
B.右侧产生的 沉淀 沉淀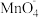 的离子方程式为: 的离子方程式为: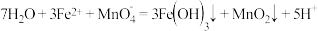 |
C.当电路中转移6mol 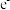 时,可以产生 时,可以产生 沉淀 沉淀 |
D.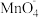 处理完全后,实验结束时左侧可能会生成沉淀 处理完全后,实验结束时左侧可能会生成沉淀 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】在直流电场作用下,双极膜可将水解离,在膜两侧分别得到 和
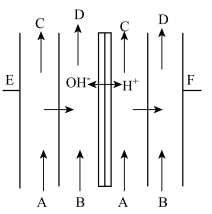
和 。利用这一特点,将双极膜与其他阴、阳离子交换膜组合成的双极膜电渗析系统,能够在不引入新组分的情况下将水溶液中的盐转化为对应的酸和碱,可用于将抗坏血酸的钠盐(NaVc)高效清洁地转化成抗坏血酸(Vc),同时获得NaOH溶液,其工作原理如图,下列有关说法正确的是
。利用这一特点,将双极膜与其他阴、阳离子交换膜组合成的双极膜电渗析系统,能够在不引入新组分的情况下将水溶液中的盐转化为对应的酸和碱,可用于将抗坏血酸的钠盐(NaVc)高效清洁地转化成抗坏血酸(Vc),同时获得NaOH溶液,其工作原理如图,下列有关说法正确的是
 和
和 。利用这一特点,将双极膜与其他阴、阳离子交换膜组合成的双极膜电渗析系统,能够在不引入新组分的情况下将水溶液中的盐转化为对应的酸和碱,可用于将抗坏血酸的钠盐(NaVc)高效清洁地转化成抗坏血酸(Vc),同时获得NaOH溶液,其工作原理如图,下列有关说法正确的是
。利用这一特点,将双极膜与其他阴、阳离子交换膜组合成的双极膜电渗析系统,能够在不引入新组分的情况下将水溶液中的盐转化为对应的酸和碱,可用于将抗坏血酸的钠盐(NaVc)高效清洁地转化成抗坏血酸(Vc),同时获得NaOH溶液,其工作原理如图,下列有关说法正确的是
| A.E接电源负极 |
| B.图中的电解装置是由双极膜与阴离子交换膜组合而成 |
| C.A为NaVc,B为NaOH稀溶液,C为Vc,D为NaOH浓溶液 |
D.F电极上发生的反应为 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
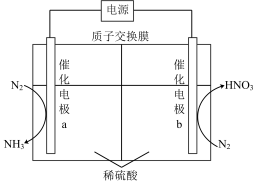
【推荐1】我国科研人员发明膜电极电解器电解脱硫废水制备硫酸铵技术,下图为制备装置示意图。下列说法正确的是
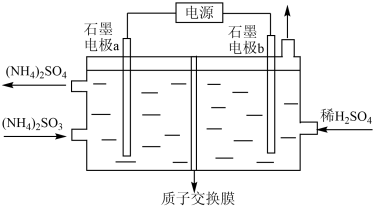

| A.电极a为阴极 |
| B.b极有NH3生成 |
| C.b极附近酸性增强 |
D.SO 在a极放电的电极反应式是:SO 在a极放电的电极反应式是:SO + H2O −2e- =SO + H2O −2e- =SO + 2H+ + 2H+ |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】用石墨电极电解CuCl2溶液(装置右图所示),下列相关分析正确的是


| A.a端是直流电源的正极 |
| B.阴极上发生的反应:Cu2++2e-=Cu |
| C.通电使CuCl2发生电离 |
| D.通电一段时间后,在阴极附近观察到黄绿色气体 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】传统的氯碱工业具有能耗高的缺点,科学家正在开发一种叫“氧阴极技术”的新工艺,新工艺与传统工艺相比在于阴极结构,通过向阴极区供应纯氧从而避免 直接得电子生成
直接得电子生成 ,这样可以降低电压,从而减少能耗。下图是采用“氧阴极技术”的氯碱工业的装置图:
,这样可以降低电压,从而减少能耗。下图是采用“氧阴极技术”的氯碱工业的装置图:
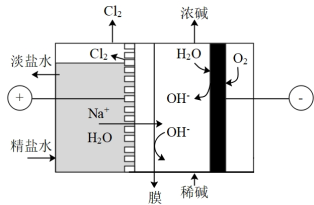
下列说法中不正确 的是
 直接得电子生成
直接得电子生成 ,这样可以降低电压,从而减少能耗。下图是采用“氧阴极技术”的氯碱工业的装置图:
,这样可以降低电压,从而减少能耗。下图是采用“氧阴极技术”的氯碱工业的装置图:
下列说法中
| A.电解池中采用阳离子交换膜,可以提高NaOH的产量和纯度 |
B.电解时阴极电极反应式为: |
C.电解的总反应离子方程式为: |
| D.电解过程中转移4 mol电子,理论上可获得4 mol NaOH |
您最近一年使用:0次
单选题-单题
|
适中
(0.65)
【推荐2】小组同学模拟工业上常采用电解法处理含铬(Ⅵ)盐废水。不同反应条件时,对Cr2O 处理的结果如表1所示(Cr2O
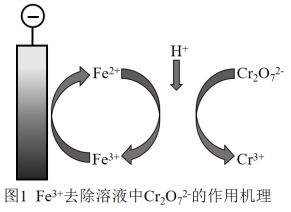
处理的结果如表1所示(Cr2O 的起始浓度、体积、电压、电解时间均相同);其中,实验③中Fe3+在去除Cr2O
的起始浓度、体积、电压、电解时间均相同);其中,实验③中Fe3+在去除Cr2O 过程中的作用机理如图1所示。
过程中的作用机理如图1所示。
表1不同条件下电解法处理Cr2O 的结果
的结果
 (橙)+ H2O
(橙)+ H2O 2 CrO
2 CrO (黄) + 2 H+
(黄) + 2 H+
下列对实验过程的分析中,不正确 的是
 处理的结果如表1所示(Cr2O
处理的结果如表1所示(Cr2O 的起始浓度、体积、电压、电解时间均相同);其中,实验③中Fe3+在去除Cr2O
的起始浓度、体积、电压、电解时间均相同);其中,实验③中Fe3+在去除Cr2O 过程中的作用机理如图1所示。
过程中的作用机理如图1所示。表1不同条件下电解法处理Cr2O
 的结果
的结果| 实验 | ④ | ② | ③ | ④ | |
| 是否加入Fe2(SO4)3 | 否 | 否 | 加入5g | 否 | |
| 是否加入H2SO4 | 否 | 加入1mL | 加入1mL | 加入1mL | |
| 电极材料 | 阴极 | 石墨 | 石墨 | 石墨 | 石墨 |
| 阳极 | 石墨 | 石墨 | 石墨 | 铁 | |
Cr2O 的去除率/% 的去除率/% | 0.922 | 12.7 | 20.8 | 57.3 | |
 (橙)+ H2O
(橙)+ H2O 2 CrO
2 CrO (黄) + 2 H+
(黄) + 2 H+下列对实验过程的分析中,
A.实验①~④中,实验④的Cr2O 去除效果最好 去除效果最好 |
B.实验②~④中,加入H2SO4可以提高溶液中Cr2O 的浓度和氧化性 的浓度和氧化性 |
C.分析图1, Cr2O 参与的反应为:6 Fe2++ 14 H+ + Cr2O 参与的反应为:6 Fe2++ 14 H+ + Cr2O = 6 Fe3+ + 2Cr3++ 7H2O = 6 Fe3+ + 2Cr3++ 7H2O |
| D.实验④中,阳极上Fe发生的反应为:Fe – 3e-=Fe3+ |
您最近一年使用:0次

 溶液的
溶液的 燃料电池中,负极反应式:
燃料电池中,负极反应式:
 的密封管放入热水中,气体红棕色变深:
的密封管放入热水中,气体红棕色变深:



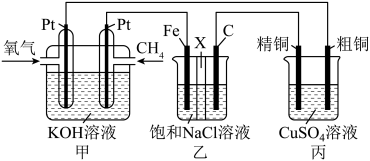
 电极上可能有副产物 O2生成
电极上可能有副产物 O2生成


