氮化铝(AlN)广泛应用于电子陶瓷等工业领域。在一定条件下,AlN可通过反应:Al2O3+N2+3C 2AlN+3CO合成。下列叙述正确的是
2AlN+3CO合成。下列叙述正确的是
 2AlN+3CO合成。下列叙述正确的是
2AlN+3CO合成。下列叙述正确的是A.上述反应中,N2是还原剂,Al2O3是氧化剂 | B.上述反应中,每生成1molAlN需转移3mol电子 |
| C.AlN中氮的化合价为+3 | D.AlN的摩尔质量为41g |
22-23高一下·福建莆田·阶段练习 查看更多[3]
福建省仙游县枫亭中学2022-2023学年高一下学期第一次月考化学试题(已下线)【2023】【高一下】【其他】【余高1】【高中化学】【刘尼尼收集】(已下线)第03讲 氧化还原反应的基本概念-【暑假自学课】2023年新高一化学暑假精品课(人教版2019必修第一册)
更新时间:2023-03-29 18:51:48
|
相似题推荐
【推荐1】可用还原法将硝酸厂烟气中的大量氮氧化物转化为无毒的物质。常温下,将NO和H2的混合气体通过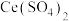 与Ce2(SO4)3的混合溶液中,其转化过程如图所示,下列说法错误的是
与Ce2(SO4)3的混合溶液中,其转化过程如图所示,下列说法错误的是

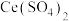 与Ce2(SO4)3的混合溶液中,其转化过程如图所示,下列说法错误的是
与Ce2(SO4)3的混合溶液中,其转化过程如图所示,下列说法错误的是
A.反应Ⅰ的离子方程式为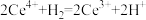 |
| B.反应Ⅱ中作氧化剂的是NO,在反应中被还原 |
| C.理论上,每消耗2.24 L氢气,转移的电子的物质的量为0.2 mol |
| D.反应混合液中,Ce4+和Ce3+的总数目保持不变 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】二氧化氯具有杀菌消毒作用,是一种广谱型消毒剂。工业上常用Cl2氧化NaClO2制得,方程式为:Cl2+2NaClO2=2ClO2+2NaCl,下列相关说法不正确的是
| A.反应中只有Cl元素的化合价发生变化 |
| B.还原剂与氧化剂的物质的量之比为1:2 |
| C.ClO2是氧化产物 |
| D.消耗0.1molNaClO2时,转移0.1mol电子 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】工业上由黄铜矿(主要成分CuFeS2)冶炼铜的主要流程如图所示:下列说法不正确的是
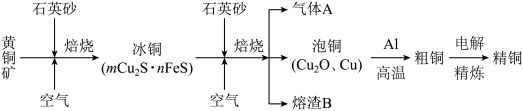

| A.气体A中含有大气污染物SO2 |
| B.由黄铜矿冶炼冰铜的过程中发生了氧化还原反应 |
| C.过量稀硫酸可全部溶解熔渣B |
| D.电解精炼铜时粗铜应接在电源的正极 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】硫化氢的转化是资源利用和环境保护的重要研究课题。将H2S和空气的混合气体通入FeCl2、CuCl2的混合溶液中反应回收S,其物质转化如图所示。下列说法错误的是
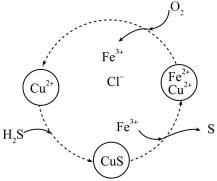

| A.在图示的转化中,CuS是中间产物 |
| B.在图示的转化中,化合价不变的元素只有铜 |
C.图示转化的总反应是2H2S+O2 2S+2H2O 2S+2H2O |
| D.当有1molH2S转化为硫单质时,需要消耗O2的物质的量为0.5mol |
您最近一年使用:0次


 与
与 可以发生化合反应
可以发生化合反应 与
与 为酸性氧化物
为酸性氧化物 也为酸性氧化物
也为酸性氧化物 是正盐
是正盐 是一元酸
是一元酸 4NaCl+Ti可以制取金属钛。下列说法不正确的是
4NaCl+Ti可以制取金属钛。下列说法不正确的是

