现有下列十种物质:①HCl ②NaCl ③纯碱 ④CO2 ⑤CH3COOH ⑥KOH ⑦氢氧化铁胶体 ⑧NH3 ⑨空气 ⑩Fe2(SO4)3
(1)上述十种物质中,属于电解质的有___________ ,属于非电解质的有___________ 。
(2)有两种物质在水溶液中可发生反应,离子方程式为H++OH-=H2O,该反应的化学方程式为___________ ;
(3)标准状况下,___________ L ④分子中含有0.2mol氧原子;
(4)现有100mL⑩溶液中含有Fe2(SO4)3 40.0g,则溶液中Fe2(SO4)3的物质的量浓度是___________ 。
(1)上述十种物质中,属于电解质的有
(2)有两种物质在水溶液中可发生反应,离子方程式为H++OH-=H2O,该反应的化学方程式为
(3)标准状况下,
(4)现有100mL⑩溶液中含有Fe2(SO4)3 40.0g,则溶液中Fe2(SO4)3的物质的量浓度是
更新时间:2023-04-04 13:27:35
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】在标准状况下,有2 g H2,求:
(1)该气体的物质的量为_______ ;
(2)该气体所含分子数为_______ ;
(3)该气体所含原子总数为_______ ;
(4)该气体在标准状况下的体积为_______ ;
(5)该气体在标准状况下的密度为_______ 。
(1)该气体的物质的量为
(2)该气体所含分子数为
(3)该气体所含原子总数为
(4)该气体在标准状况下的体积为
(5)该气体在标准状况下的密度为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】现有以下物质:①NaCl固体;②液态CO2;③液态氯化氢;④汞;⑤固体BaSO4;⑥蔗糖;⑦酒精;⑧熔融的Na2CO3,请回答下列问题:
(1)以上物质中能导电的是________ ;
(2)以上物质属于电解质的是________ ;
(3)以上物质属于非电解质的是_______ ;
(4)以上物质溶于水后形成的溶液能导电的是______ ;
(5)属于盐的有________ ;
(6)写出⑧溶于水中的电离方程式_____ ;
(7)分离胶体和溶液常用的方法叫__________ ;
(8)等质量的O2和O3所含原子个数比为______ ;
(9)设NA为阿伏加 德罗常数的数值,若ag某气体中含有的分子数为b,则c g该气体在标准状况下的体积是___________ 。(用含有NA的式子表示)
(1)以上物质中能导电的是
(2)以上物质属于电解质的是
(3)以上物质属于非电解质的是
(4)以上物质溶于水后形成的溶液能导电的是
(5)属于盐的有
(6)写出⑧溶于水中的电离方程式
(7)分离胶体和溶液常用的方法叫
(8)等质量的O2和O3所含原子个数比为
(9)设NA为阿伏加 德罗常数的数值,若ag某气体中含有的分子数为b,则c g该气体在标准状况下的体积是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】有以下物质:①氯气、②碳酸钙、③纯醋酸、④二氧化碳、⑤氯化铁固体、⑥碳酸氢钠固体、⑦氢氧化钡溶液、⑧氨气。
(1)以上物质属于强电解质的是___________ 。
(2)写出②和③反应的离子方程式:___________ 。
(3)写出①和水反应的离子方程式:___________ 。
(4)写出用⑤的饱和溶液制备 胶体的离子方程式:
胶体的离子方程式:___________ 。
(5)将物质⑥配制成溶液逐滴加入到⑦溶液中,直至沉淀量最大,停止滴加,写出离子方程式:___________ 。
(6)标准状况下,若④和⑧混合气体相对于氢气的密度为14.5,则④和⑧物质的量之比为___________ 。标准状况下, 溶入
溶入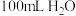 中,溶液密度为
中,溶液密度为 ,则氨水物质的量浓度表达式为
,则氨水物质的量浓度表达式为___________  。
。
(1)以上物质属于强电解质的是
(2)写出②和③反应的离子方程式:
(3)写出①和水反应的离子方程式:
(4)写出用⑤的饱和溶液制备
 胶体的离子方程式:
胶体的离子方程式:(5)将物质⑥配制成溶液逐滴加入到⑦溶液中,直至沉淀量最大,停止滴加,写出离子方程式:
(6)标准状况下,若④和⑧混合气体相对于氢气的密度为14.5,则④和⑧物质的量之比为
 溶入
溶入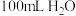 中,溶液密度为
中,溶液密度为 ,则氨水物质的量浓度表达式为
,则氨水物质的量浓度表达式为 。
。
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】2 mol NH3质量为_______ g,在标准状况下体积为_______ 升,溶于水配成500mL溶液,物质的量浓度为_______ mol/L,将此溶液加水稀释到1000mL,稀释后溶液的物质的量浓度为_______ 。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】(1)把标准状况下VL气体(摩尔质量为Mg·mol-1)溶于1L水中(不考虑反应),所得溶液密度为ρg/cm3,则此溶液的物质的量浓度为_________________ mol/L;
(2)把100mL0.3mol/LNa2SO4溶液和400mL0.2mol/LNaCl溶液混合后,溶液中Na+的物质的量浓度为_____________________
(3)一定质量的Al与足量盐酸反应,当转移了2 mol电子时,参与反应的铝的质量是________ g。
(4)下列物质:①Fe ②NaCl ③Na2O ④CO ⑤CO2 ⑥蔗糖 ⑦NH3 ⑧NaCl溶液 ⑨盐酸 ⑩ H2SO4 ⑪Ba(OH)2
属于电解质的是_______ , 属于非电解质的是 ________ ,能导电的是_____________ 。
(2)把100mL0.3mol/LNa2SO4溶液和400mL0.2mol/LNaCl溶液混合后,溶液中Na+的物质的量浓度为
(3)一定质量的Al与足量盐酸反应,当转移了2 mol电子时,参与反应的铝的质量是
(4)下列物质:①Fe ②NaCl ③Na2O ④CO ⑤CO2 ⑥蔗糖 ⑦NH3 ⑧NaCl溶液 ⑨盐酸 ⑩ H2SO4 ⑪Ba(OH)2
属于电解质的是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】回答下列问题:
(1)下列物质能导电且属于电解质的是_______(填字母)。
(2)一种中子数为9的氧原子的质量数为_______ 。
(3)臭氧和氧气互为_______ (填“同位素”或“同素异形体”),它们在一定条件下可以相互转化,该变化过程属于_______ (填“物理变化”或“化学变化”)。
(4)FeCl2、FeCl3和Na2FeO4(高铁酸钾)都是铁的重要化合物。那么Na2FeO4所含铁元素的化合价是_______ 。
(5)在100 mL 0.2 mol·L-1 Na2SO4溶液中加入蒸馏水稀释至200mL,那么稀释后的溶液中Na+的物质的量浓度为_______ 。
(6)向含n mol FeBr2溶液中通入n mol的Cl2,充分反应的离子方程式为_______ 。
(1)下列物质能导电且属于电解质的是_______(填字母)。
| A.氯化钠固体 | B.熔融的氯化钠 | C.氯化钠溶液 | D.钠 |
(3)臭氧和氧气互为
(4)FeCl2、FeCl3和Na2FeO4(高铁酸钾)都是铁的重要化合物。那么Na2FeO4所含铁元素的化合价是
(5)在100 mL 0.2 mol·L-1 Na2SO4溶液中加入蒸馏水稀释至200mL,那么稀释后的溶液中Na+的物质的量浓度为
(6)向含n mol FeBr2溶液中通入n mol的Cl2,充分反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】有以下物质:①NaHSO4溶液 ②小苏打③氨水④铜⑤FeCl3固体⑥稀NaOH溶液⑦Al(OH)3⑧二氧化碳
(1)上述物质中能导电的物质有(填序号,下同)________ 属于电解质的是 _________ ,属于非电解质的_____________
(2)写出NaHSO4在水中的电离方程式:__________
(3)写出小苏打与胃酸(主要成分为稀盐酸)作用的离子方程式:_____________
(4)实验室用⑤制备胶体的化学方程式为_______ 如果将1molFeCl3全部变成胶体,胶粒数目_____ NA(选填“大于”“等于”“小于”)
(1)上述物质中能导电的物质有(填序号,下同)
(2)写出NaHSO4在水中的电离方程式:
(3)写出小苏打与胃酸(主要成分为稀盐酸)作用的离子方程式:
(4)实验室用⑤制备胶体的化学方程式为
您最近一年使用:0次
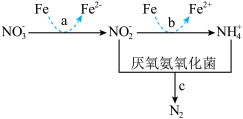
【推荐1】短程硝化-厌氧氨氧化工艺的目的是将氨氮( )废水中的氮元素转变为
)废水中的氮元素转变为 脱除,其机理如下:
脱除,其机理如下:

资料:氧气浓度过高时, 会被氧化成
会被氧化成 。
。
(1)参与I中反应的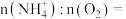
_____ 。
(2)Ⅱ中生成 的离子方程式为
的离子方程式为_____ 。
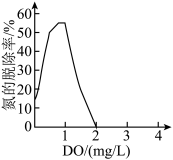
(3)废水溶解氧浓度(DO)对氮的脱除率的影响如图所示。当DO>2mg/L时,氮的脱除率为0,其原因可能是厌氧氨氧化菌被㧕制,Ⅱ中反应无法发生;还有可能是_____ 。
(4)经上述工艺处理后,排出的水中含有一定量的 ,加入铁粉能有效除去
,加入铁粉能有效除去 。该过程涉及的三个反应(a、b和c)如图:在整个反应过程中几乎监测不到
。该过程涉及的三个反应(a、b和c)如图:在整个反应过程中几乎监测不到 浓度的增加。请从化学反应速率的角度解释其原因:
浓度的增加。请从化学反应速率的角度解释其原因:_____ 。
 )废水中的氮元素转变为
)废水中的氮元素转变为 脱除,其机理如下:
脱除,其机理如下:
资料:氧气浓度过高时,
 会被氧化成
会被氧化成 。
。(1)参与I中反应的
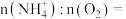
(2)Ⅱ中生成
 的离子方程式为
的离子方程式为(3)废水溶解氧浓度(DO)对氮的脱除率的影响如图所示。当DO>2mg/L时,氮的脱除率为0,其原因可能是厌氧氨氧化菌被㧕制,Ⅱ中反应无法发生;还有可能是

(4)经上述工艺处理后,排出的水中含有一定量的
 ,加入铁粉能有效除去
,加入铁粉能有效除去 。该过程涉及的三个反应(a、b和c)如图:在整个反应过程中几乎监测不到
。该过程涉及的三个反应(a、b和c)如图:在整个反应过程中几乎监测不到 浓度的增加。请从化学反应速率的角度解释其原因:
浓度的增加。请从化学反应速率的角度解释其原因:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】铜是生命必需的元素,也是人类最早使用的金属之一,铜的生产和使用对国计民生各个方面产生了深远的影响,请回答下列问题:
(1)西汉古籍中曾有记载:曾青(硫酸铜)得铁则化为铜。
该反应的化学方程式是____________________ ;
该反应的离子方程式是______________________ 。
(2)铜器表面有时会生成铜绿,其化学式为Cu2(OH)2CO3。
请写出生成铜绿的化学方程式:______________ ;铜绿可用化学方法除去,请写出除去铜绿而不损伤器物的化学方程式:_________ 。铜制品的保护方法是___________ 。
(3)铜钱在历史上曾经是一种广泛流通的货币。试从物理性质和化学性质的角度分析铜常用于制造货币的原因(已知铜的熔点是1183.4 ,铁的熔点是1534.8 ):_________________ 。
(1)西汉古籍中曾有记载:曾青(硫酸铜)得铁则化为铜。
该反应的化学方程式是
该反应的离子方程式是
(2)铜器表面有时会生成铜绿,其化学式为Cu2(OH)2CO3。
请写出生成铜绿的化学方程式:
(3)铜钱在历史上曾经是一种广泛流通的货币。试从物理性质和化学性质的角度分析铜常用于制造货币的原因(已知铜的熔点是1183.4 ,铁的熔点是1534.8 ):
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】Ⅰ.现有下列物质:①Fe(OH)3胶体 ②铜丝 ③氯化氢气体 ④稀硫酸 ⑤二氧化碳气体 ⑥石墨 ⑦碳酸钠溶液 ⑧乙醇 ⑨熔融氯化钠。请用序号填空:
(1)属于电解质的是_______ 。
(2)属于非电解质的是_______ 。
Ⅱ.书写离子反应方程式:
(3)金属钠与水反应的离子反应方程式_______ 。
(4) 溶于稀盐酸的离子反应方程式
溶于稀盐酸的离子反应方程式_______ 。
(5)澄清石灰水中滴入足量的Na2CO3溶液的离子反应方程式_______ 。
(6) 溶液与
溶液与 溶液反应的离子反应方程式
溶液反应的离子反应方程式_______ 。
(1)属于电解质的是
(2)属于非电解质的是
Ⅱ.书写离子反应方程式:
(3)金属钠与水反应的离子反应方程式
(4)
 溶于稀盐酸的离子反应方程式
溶于稀盐酸的离子反应方程式(5)澄清石灰水中滴入足量的Na2CO3溶液的离子反应方程式
(6)
 溶液与
溶液与 溶液反应的离子反应方程式
溶液反应的离子反应方程式
您最近一年使用:0次

 某双原子气体中含有的原子数为b,则
某双原子气体中含有的原子数为b,则 该气体在标准状况下的体积是(式中
该气体在标准状况下的体积是(式中 为阿伏加德罗常数的值)
为阿伏加德罗常数的值)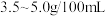 (总酸含量即
(总酸含量即 食醋中含醋酸的质量)。某兴趣小组为测定一市售食醋的总酸含量,进行了实验。实验后,得知
食醋中含醋酸的质量)。某兴趣小组为测定一市售食醋的总酸含量,进行了实验。实验后,得知 该食醋样品与
该食醋样品与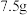 溶质的质量分数为
溶质的质量分数为 的氢氧化钠溶液恰好完全反应。计算该市售食醋样品中的总酸含量,并说明是否符合国家标准
的氢氧化钠溶液恰好完全反应。计算该市售食醋样品中的总酸含量,并说明是否符合国家标准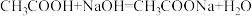 假设该市售食醋样品中其它物质不与氢氧化钠发生反应)
假设该市售食醋样品中其它物质不与氢氧化钠发生反应)


