题型:解答题-结构与性质
难度:0.4
引用次数:380
题号:18784481
离子液体是指室温或接近室温时呈液态,而本身由阴、阳离子构成的化合物。GaCl3和氯化- 1-乙基- 3-甲基咪唑( ,简称EMIC)混合形成的离子液体被认为是21世纪理想的绿色溶剂。请回答下列问题:
,简称EMIC)混合形成的离子液体被认为是21世纪理想的绿色溶剂。请回答下列问题:
(1)请写出基态Ga原子的核外电子排布式___________ , 同周期主族元素中基态原子未成对电子数与Ga相同的___________ ( 填元素符号)。
(2)EMIC阳离子中的几种元素电负性由大到小顺序为___________ 。
(3)EMIC中碳原子的杂化类型为___________ 。
(4)已知分子中的大 键可用符号
键可用符号 表示,其中m代表参与形成大
表示,其中m代表参与形成大 键的原子数,n代表大II键中的电子数,则EMIC中大
键的原子数,n代表大II键中的电子数,则EMIC中大 键可表示为
键可表示为___________ 。
(5)GaCl3熔点为77.8°C, GaF3熔点高于1000°C,其原因是___________ 。
(6)某种Ga的氧化物晶胞结构如图所示。O2-以六方密堆积形成晶胞, Ga3+位于由A、B、C、D四个O2-围成的四边形的中心,但晶胞中只,有 的四边形中心位置占据了Ga3+,另外
的四边形中心位置占据了Ga3+,另外 的位置空置。
的位置空置。
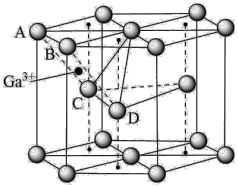
①Ga3+位于O2-围成的___________ 面体空隙中。
②若该晶胞的体积为Vcm3,用NA表示阿伏加德罗常数的值,该氧化物晶体密度为___________ g·cm-3。
 ,简称EMIC)混合形成的离子液体被认为是21世纪理想的绿色溶剂。请回答下列问题:
,简称EMIC)混合形成的离子液体被认为是21世纪理想的绿色溶剂。请回答下列问题:(1)请写出基态Ga原子的核外电子排布式
(2)EMIC阳离子中的几种元素电负性由大到小顺序为
(3)EMIC中碳原子的杂化类型为
(4)已知分子中的大
 键可用符号
键可用符号 表示,其中m代表参与形成大
表示,其中m代表参与形成大 键的原子数,n代表大II键中的电子数,则EMIC中大
键的原子数,n代表大II键中的电子数,则EMIC中大 键可表示为
键可表示为(5)GaCl3熔点为77.8°C, GaF3熔点高于1000°C,其原因是
(6)某种Ga的氧化物晶胞结构如图所示。O2-以六方密堆积形成晶胞, Ga3+位于由A、B、C、D四个O2-围成的四边形的中心,但晶胞中只,有
 的四边形中心位置占据了Ga3+,另外
的四边形中心位置占据了Ga3+,另外 的位置空置。
的位置空置。
①Ga3+位于O2-围成的
②若该晶胞的体积为Vcm3,用NA表示阿伏加德罗常数的值,该氧化物晶体密度为
更新时间:2023-04-25 11:22:25
|
【知识点】 物质结构与性质综合考查解读
相似题推荐
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐1】新型储氢材料是开发利用氢能的重要研究方向。
(1)Ti(BH4)3是一种储氢材料,可由TiCl4和LiBH4反应制得。
①基态Cl原子中,电子占据的最高电子层符号为__ ,该电子层具有的原子轨道数为__ 。
②LiBH4由Li+和BH4-构成,BH4-的立体构型是__ ,B原子的杂化轨道类型是___ 。
③Li、B元素的电负性由小到大的顺序为___ 。
(2)金属氢化物是具有良好发展前景的储氢材料。
①LiH中,离子半径:Li+__ H-(填“>”“=”或“<”)。
②某储氢材料是短周期金属元素M的氢化物。M的部分电离能如下表所示:
M是__ 族元素。
(3)图2是立方氮化硼晶胞沿z轴的投影图,请在图中圆球上涂“●”和涂“ ”分别标明B与N的相对位置
”分别标明B与N的相对位置___ 。

(4)NaH具有NaCl型晶体结构,已知NaH晶体的晶胞参数a=488pm,Na+半径为102pm,H-的半径为__ ,NaH的理论密度是__ g·cm-3(保留3个有效数字)。
(1)Ti(BH4)3是一种储氢材料,可由TiCl4和LiBH4反应制得。
①基态Cl原子中,电子占据的最高电子层符号为
②LiBH4由Li+和BH4-构成,BH4-的立体构型是
③Li、B元素的电负性由小到大的顺序为
(2)金属氢化物是具有良好发展前景的储氢材料。
①LiH中,离子半径:Li+
②某储氢材料是短周期金属元素M的氢化物。M的部分电离能如下表所示:
| I1/kJ·mol-1 | I2/kJ·mol-1 | I3/kJ·mol-1 | I4/kJ·mol-1 | I5/kJ·mol-1 |
| 738 | 1451 | 7733 | 10540 | 13630 |
(3)图2是立方氮化硼晶胞沿z轴的投影图,请在图中圆球上涂“●”和涂“
 ”分别标明B与N的相对位置
”分别标明B与N的相对位置
(4)NaH具有NaCl型晶体结构,已知NaH晶体的晶胞参数a=488pm,Na+半径为102pm,H-的半径为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐2】硼及其化合物应用广泛。回答下列问题:
(1)基态B原子的价电子轨道表达式为________ ,其第一电离能比Be ________ (填“大”或“小”)。
(2)氨硼烷(NH3BH3)被认为是最具潜力的新型储氢材料之一,分子中存在配位键,提供孤电子对的成键原子是________ ,写出一种与氨硼烷互为等电子体的分子________ (填化学式)。
(3)常温常压下硼酸(H3BO3)晶体结构为层状,其二维平面结构如图a。
① B原子的杂化方式为________ 。从氢键的角度解释硼酸在冷水中的溶解度小而加热时溶解度增大:________ 。
② 路易斯酸碱理论认为,任何可接受电子对的分子或离子叫路易斯酸,任何可给出电子对的分子或离子叫路易斯碱。从结构角度分析硼酸是路易斯酸:________ 。
(4)立方氮化硼(BN)是特殊的耐磨和切削材料,其晶胞结构与金刚石相似,如图b所示。
① 与氮原子直接连接的硼原子构成的几何形状为________ 。硼原子和氮原子所连接的最小环为________ 元环。
② 晶胞有两个基本要素:
原子坐标参数,表示晶胞内部各原子的相对位置。如图b所示,其中原子坐标参数X为(0,0,0),Y原子的坐标参数为(1/2,0,1/2),则Z原子的坐标参数为________ 。
晶胞参数,描述晶胞的大小和形状。已知立方氮化硼的密度为d g∙cm-3,阿伏伽德罗常数值为NA,则晶胞参数a=________ nm。(列出计算式即可)
(1)基态B原子的价电子轨道表达式为
(2)氨硼烷(NH3BH3)被认为是最具潜力的新型储氢材料之一,分子中存在配位键,提供孤电子对的成键原子是

(3)常温常压下硼酸(H3BO3)晶体结构为层状,其二维平面结构如图a。
① B原子的杂化方式为
② 路易斯酸碱理论认为,任何可接受电子对的分子或离子叫路易斯酸,任何可给出电子对的分子或离子叫路易斯碱。从结构角度分析硼酸是路易斯酸:
(4)立方氮化硼(BN)是特殊的耐磨和切削材料,其晶胞结构与金刚石相似,如图b所示。
① 与氮原子直接连接的硼原子构成的几何形状为
② 晶胞有两个基本要素:
原子坐标参数,表示晶胞内部各原子的相对位置。如图b所示,其中原子坐标参数X为(0,0,0),Y原子的坐标参数为(1/2,0,1/2),则Z原子的坐标参数为
晶胞参数,描述晶胞的大小和形状。已知立方氮化硼的密度为d g∙cm-3,阿伏伽德罗常数值为NA,则晶胞参数a=
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐3】周期表前四周期的元素a、b、c、d、e,原子序数依次增大,b2a4常做火箭推进剂的燃料,c是地壳中含量最多的元素,d2+离子3d轨道中有6个电子,e单质不溶于稀硫酸,常用作电缆材料。回答下列问题:
(1)区别晶体和非晶体最科学的方法是_______ 。
(2)a2c的VSEPR模型为_______ ,d3+比d2+稳定的原因是_______ 。
(3)向e2+硫酸盐的水溶液中加入过量的氨水,可得到深蓝色透明溶液,加入乙醇可析出深蓝色晶体。该深蓝色晶体是_______ (化学式),写出上述过程中发生反应的离子方程式__________________________________ , _____________________________________ 。
(4)已知某化合物是由b和d两种元素组成的晶体,其晶胞结构如图所示,则该晶体的化学式为_______ 。若该晶体的密度是ρ g/cm3,则晶胞中两个最近的 d的核间距为__________________ cm(用含ρ的代数式表示)

(1)区别晶体和非晶体最科学的方法是
(2)a2c的VSEPR模型为
(3)向e2+硫酸盐的水溶液中加入过量的氨水,可得到深蓝色透明溶液,加入乙醇可析出深蓝色晶体。该深蓝色晶体是
(4)已知某化合物是由b和d两种元素组成的晶体,其晶胞结构如图所示,则该晶体的化学式为

您最近一年使用:0次



