按照要求回答下列问题:
(1)通过电解废旧锂电池中的LiMn2O4可获得难溶性的Li2CO3和MnO2,电解示意图如图(其中滤布的作用是阻挡固体颗粒,但离子可自由通过,电解过程中溶液的体积变化忽略不计)。
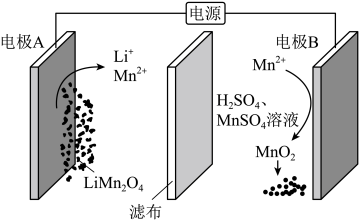
①电极B发生的电极反应式为______ 。
②电解一段时间后溶液中Mn2+浓度______ (填“增大”“减小”或“不变”)。
(2)用NaOH溶液吸收烟气中的SO2,将所得的Na2SO3溶液进行电解,可循环再生NaOH,同时得到H2SO4,其原理如图所示(电极材料均为石墨)。

①图中A口产生的气体为______ ,B口流出的物质是______ 。
②b电极表面发生的电极反应式为______ 。
(3)Co是磁性合金的重要材料,也是维生素的重要组成元素。工业上可用如图装置制取单质Co并获得副产品盐酸(A、B均为离子交换膜)。

①A为______ (填“阳”或“阴”)离子交换膜。
②该电解池的总反应离子方程式为______ 。
③若产品室中阴极质量增加11.8g,则产品室增加的HCl的物质的量为______ 。
(1)通过电解废旧锂电池中的LiMn2O4可获得难溶性的Li2CO3和MnO2,电解示意图如图(其中滤布的作用是阻挡固体颗粒,但离子可自由通过,电解过程中溶液的体积变化忽略不计)。

①电极B发生的电极反应式为
②电解一段时间后溶液中Mn2+浓度
(2)用NaOH溶液吸收烟气中的SO2,将所得的Na2SO3溶液进行电解,可循环再生NaOH,同时得到H2SO4,其原理如图所示(电极材料均为石墨)。

①图中A口产生的气体为
②b电极表面发生的电极反应式为
(3)Co是磁性合金的重要材料,也是维生素的重要组成元素。工业上可用如图装置制取单质Co并获得副产品盐酸(A、B均为离子交换膜)。

①A为
②该电解池的总反应离子方程式为
③若产品室中阴极质量增加11.8g,则产品室增加的HCl的物质的量为
更新时间:2023-04-27 08:30:42
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】依据甲、乙、丙三个图回答下列问题:
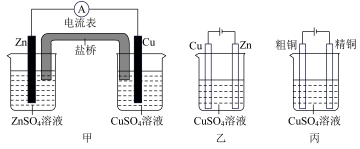
(1)①甲装置中,锌为_____ 极,锌电极上电极反应式为________________
②乙装置中,锌为_____ 极,锌电极上电极反应式为________________
(2)丙装置中,Cu2+浓度________ (填“增大”“减小”或“不变”),原因是_______________________________________________________________________
(3)在25 ℃时,用石墨电极电解2.0 L 0.5 mol·L-1CuSO4溶液。5 min后,在一个石墨电极上有6.4 g Cu生成。试回答下列问题:
若电解后溶液的体积不变,则电解后溶液的[H+]为___________ 。
若将溶液恢复到与电解前一样,则需加入_____ mol的______ 。

(1)①甲装置中,锌为
②乙装置中,锌为
(2)丙装置中,Cu2+浓度
(3)在25 ℃时,用石墨电极电解2.0 L 0.5 mol·L-1CuSO4溶液。5 min后,在一个石墨电极上有6.4 g Cu生成。试回答下列问题:
若电解后溶液的体积不变,则电解后溶液的[H+]为
若将溶液恢复到与电解前一样,则需加入
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】(1)CH3COOH是最常见的有机弱酸。
①CH3COOH的电离方程式为_____________ 。
②CH3COONa溶液呈碱性,原因是__________ (填“CH3COO-”或“Na+”)水解引起的。
③在CH3COONa溶液中,c(Na+)_______ c(CH3COO-)(填“>”“=”或“<”)。
(2)已知:反应C(s)+H2O(g) CO(g)+H2(g)的△H=131.3kJ/mol。
CO(g)+H2(g)的△H=131.3kJ/mol。
①该反应是反应__________ (填“吸热”或“放热”)。
②若反应消耗24g C(s),则反应的热效应为__________ 。
(3)在一定温度下,将CO(g)和H2O(g)各0.16mol通入容积为2.0L的恒容密闭容器中,发生以下反应:CO(g)+H2O(g) CO2(g)+H2(g),得到如下数据:
CO2(g)+H2(g),得到如下数据:
① 2min内,v(CO)=__________ 。
②该温度下,此反应的平衡常数表达式K=_________ 。
③其他条件不变,再充入0.1mol CO和0.1mol H2O(g),达到平衡时CO的体积分数_____ (填“增大”、“减小”或“不变”)。
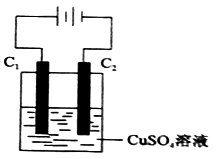
(4)下图为直流电源电解CuSO4溶液的装置,C1和C2都为石墨电极,请回答下列问题:
① C1作_________ (填“阳极”或”阴极”)。
② C2极电极反应式为____________ 。
①CH3COOH的电离方程式为
②CH3COONa溶液呈碱性,原因是
③在CH3COONa溶液中,c(Na+)
(2)已知:反应C(s)+H2O(g)
 CO(g)+H2(g)的△H=131.3kJ/mol。
CO(g)+H2(g)的△H=131.3kJ/mol。①该反应是反应
②若反应消耗24g C(s),则反应的热效应为
(3)在一定温度下,将CO(g)和H2O(g)各0.16mol通入容积为2.0L的恒容密闭容器中,发生以下反应:CO(g)+H2O(g)
 CO2(g)+H2(g),得到如下数据:
CO2(g)+H2(g),得到如下数据:t/min | 2 | 4 | 7 | 9 |
n(H2O)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
① 2min内,v(CO)=
②该温度下,此反应的平衡常数表达式K=
③其他条件不变,再充入0.1mol CO和0.1mol H2O(g),达到平衡时CO的体积分数
(4)下图为直流电源电解CuSO4溶液的装置,C1和C2都为石墨电极,请回答下列问题:
① C1作
② C2极电极反应式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】I. 作为化石燃料燃烧产生的废气,是主要的温室气体之一,使用电化学方法能够对
作为化石燃料燃烧产生的废气,是主要的温室气体之一,使用电化学方法能够对 进行吸收。利用活泼金属与二氧化碳的反应,能够构建金属-
进行吸收。利用活泼金属与二氧化碳的反应,能够构建金属- 电池,其中一种
电池,其中一种 电池的模型如下图所示:(图中
电池的模型如下图所示:(图中 是固体)
是固体)
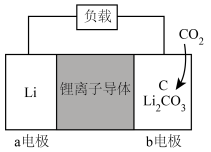
(1)下列有关该原电池的说法中,正确的是___________。
(2)写出该原电池的正极反应以及总反应,正极:___________ ;总反应:___________ 。
(3)原电池中每转移 电子,能够吸收
电子,能够吸收___________ 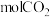 。
。
II.利用电解池,通过电化学还原, 能够被还原为低价碳化合物。一种电化学还原二氧化碳的装置能够将二氧化碳还原为甲酸
能够被还原为低价碳化合物。一种电化学还原二氧化碳的装置能够将二氧化碳还原为甲酸 ,该装置中,石墨作为阳极,单质银作为阴极,电解质溶液是硫酸溶液。
,该装置中,石墨作为阳极,单质银作为阴极,电解质溶液是硫酸溶液。
(4)在该装置中,应该向___________ 极(填“阴”或“阳”)附近通入 气体。
气体。
(5)写出 在该电极上反应的电极反应式:
在该电极上反应的电极反应式:___________ 。
(6)当电极上生成5.6L(标准状况)的氧气时,生成甲酸的质量为___________ g。
 作为化石燃料燃烧产生的废气,是主要的温室气体之一,使用电化学方法能够对
作为化石燃料燃烧产生的废气,是主要的温室气体之一,使用电化学方法能够对 进行吸收。利用活泼金属与二氧化碳的反应,能够构建金属-
进行吸收。利用活泼金属与二氧化碳的反应,能够构建金属- 电池,其中一种
电池,其中一种 电池的模型如下图所示:(图中
电池的模型如下图所示:(图中 是固体)
是固体)
(1)下列有关该原电池的说法中,正确的是___________。
| A.该原电池工作时,电子由正极向负极移动 |
| B.在该原电池中,石墨作为负极 |
| C.原电池工作时,阳离子一定向正极方向移动 |
| D.原电池工作时,b电极发生氧化反应 |
(2)写出该原电池的正极反应以及总反应,正极:
(3)原电池中每转移
 电子,能够吸收
电子,能够吸收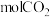 。
。II.利用电解池,通过电化学还原,
 能够被还原为低价碳化合物。一种电化学还原二氧化碳的装置能够将二氧化碳还原为甲酸
能够被还原为低价碳化合物。一种电化学还原二氧化碳的装置能够将二氧化碳还原为甲酸 ,该装置中,石墨作为阳极,单质银作为阴极,电解质溶液是硫酸溶液。
,该装置中,石墨作为阳极,单质银作为阴极,电解质溶液是硫酸溶液。(4)在该装置中,应该向
 气体。
气体。(5)写出
 在该电极上反应的电极反应式:
在该电极上反应的电极反应式:(6)当电极上生成5.6L(标准状况)的氧气时,生成甲酸的质量为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】实验过程中为什么要不断搅拌正极________ ?
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】日常生活、科学研究、工业生产中有许多问题与原电池或电解池的工作原理有关,回答下列问题:

(1)写出三个装置中铁电极的电极反应式:①________ ,②________ ,③________ 。
(2)为了比较Fe、Co、Cu三种金属的活动性,某实验小组设计如下实验装置。

丙装置中充入滴有酚酞的氯化钠溶液,X、Y均为石墨电极。反应一段时间后,可观察到甲装置中Co电极附近产生气泡,丙装置中X极附近溶液变红。
①丙装置中Y极为_______ 极(填“正”、“负”、“阴”或“阳”)。
②写出甲装置中Co电极的电极反应式:___________ 。
③三种金属的活动性由强到弱的顺序是__________ (填元素符号)。
(3)中国科学院应用化学研究所在甲醚(CH3OCH3)燃料电池技术方面获得新突破。甲醚燃料电池的工作原理如下图所示:

①甲醚由________ (填a或b)通入
②该电池负极的电极反应式__________ 。
③工作一段时间后,当9.2g的甲醚完全反应时,有______ mol电子转移。

(1)写出三个装置中铁电极的电极反应式:①
(2)为了比较Fe、Co、Cu三种金属的活动性,某实验小组设计如下实验装置。

丙装置中充入滴有酚酞的氯化钠溶液,X、Y均为石墨电极。反应一段时间后,可观察到甲装置中Co电极附近产生气泡,丙装置中X极附近溶液变红。
①丙装置中Y极为
②写出甲装置中Co电极的电极反应式:
③三种金属的活动性由强到弱的顺序是
(3)中国科学院应用化学研究所在甲醚(CH3OCH3)燃料电池技术方面获得新突破。甲醚燃料电池的工作原理如下图所示:

①甲醚由
②该电池负极的电极反应式
③工作一段时间后,当9.2g的甲醚完全反应时,有
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】如图装置所示,C、D、E、F、X、Y都是惰性电极,甲、乙中溶液的体积和浓度都相同(假设通电前后溶液体积不变),A、B为外接直流电源的两极。将直流电源接通后,F极附近呈红色。
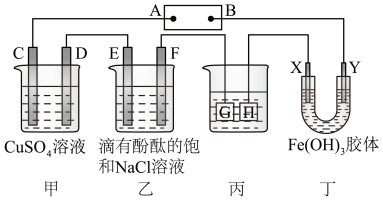
(1)B极是电源的____ (填“正极”或“负极”),一段时间后,丁中X极附近的颜色逐渐____ (填“变深”或“变浅”)。
(2)若甲、乙装置中的C、D、E、F电极均只有一种单质生成时,对应单质的物质的量之比为___ 。
(3)现用丙装置给铜件镀银,则H应是___ 。若乙溶液体积为500mL,当乙中溶液的pH=13时,丙中镀件上析出银的质量为___ ,甲中溶液的pH____ (填“变大”“变小”或“不变”)。
(4)若将C电极换为铁,其他装置都不变,则甲中发生的总反应的离子方程式为____ 。

(1)B极是电源的
(2)若甲、乙装置中的C、D、E、F电极均只有一种单质生成时,对应单质的物质的量之比为
(3)现用丙装置给铜件镀银,则H应是
(4)若将C电极换为铁,其他装置都不变,则甲中发生的总反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】电解原理在化学工业中有广泛应用。下图表示一个电解池,其中a为电解质溶液, X、Y是两块电极板,通过导线与直流电源相连。请回答以下问题:

(1)X的电极名称是____________ (填写“阳极”或“阴极”)。
(2)若X、Y都是惰性电极,a是饱和食盐水,实验开始时,同时在两边各滴入几滴酚酞试液,一段时间后,在X极附近观察到的现象是_____________________________ ,Y极上的电极反应式为____________ 。
(3)若X、Y都是惰性电极,a是CuSO4溶液,电解一段时间后,阳极上产生气体的体积为0.224L(标准状况下),则阴极上析出金属的质量为_________ g。
(4)若要用该装置电解精炼粗铜,电解液a选用CuSO4溶液,则X电极的材料是__________ ,Y电极的材料是____________ 。
(5)若要用电镀方法在铁表面镀一层金属银,应该选择的方案是___________ 。

(1)X的电极名称是
(2)若X、Y都是惰性电极,a是饱和食盐水,实验开始时,同时在两边各滴入几滴酚酞试液,一段时间后,在X极附近观察到的现象是
(3)若X、Y都是惰性电极,a是CuSO4溶液,电解一段时间后,阳极上产生气体的体积为0.224L(标准状况下),则阴极上析出金属的质量为
(4)若要用该装置电解精炼粗铜,电解液a选用CuSO4溶液,则X电极的材料是
(5)若要用电镀方法在铁表面镀一层金属银,应该选择的方案是
| 方案 | X | Y | a溶液 |
| A | 银 | 石墨 | AgNO3 |
| B | 银 | 铁 | AgNO3 |
| C | 铁 | 银 | Fe(NO3)3 |
| D | 铁 | 银 | AgNO3 |
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】第三代混合动力车,可以用电动机、内燃机或二者结合推动车辆。汽车上坡或加速时,电动机提供推动力,降低汽油的消耗;在刹车或下坡时,电池处于充电状态。
(1)混合动力车的内燃机以汽油为燃料,汽油(以辛烷C8H18液体计)和氧气充分反应,生成1 mol水蒸气放热 569.1kJ。则该反应的热化学方程式为_______ 。
(2)混合动力车目前一般使用镍氢电池,该电池中镍的化合物为正极,储氢金属(以M表示)为负极,碱液(主要为KOH溶液)为电解质溶液。镍氢电池充放电原理示意如图1,其总反应式为H2+2NiO(OH) 2Ni(OH)2。根据所给信息判断,混合动力车上坡或加速时,乙电极周围溶液的pH
2Ni(OH)2。根据所给信息判断,混合动力车上坡或加速时,乙电极周围溶液的pH_______ (填“增大”“减小”或“不变”),该电极的电极反应式为_______ 。

(3)Cu2O是一种半导体材料,可通过如图2所示的电解装置制取,电解总反应式为2Cu+H2O Cu2O+H2↑,阴极的电极反应式是
Cu2O+H2↑,阴极的电极反应式是_______ 。用镍氢电池作为电源进行电解,当电池中有2 mol H2被消耗时,Cu2O的理论产量为_______ mol。

(1)混合动力车的内燃机以汽油为燃料,汽油(以辛烷C8H18液体计)和氧气充分反应,生成1 mol水蒸气放热 569.1kJ。则该反应的热化学方程式为
(2)混合动力车目前一般使用镍氢电池,该电池中镍的化合物为正极,储氢金属(以M表示)为负极,碱液(主要为KOH溶液)为电解质溶液。镍氢电池充放电原理示意如图1,其总反应式为H2+2NiO(OH)
 2Ni(OH)2。根据所给信息判断,混合动力车上坡或加速时,乙电极周围溶液的pH
2Ni(OH)2。根据所给信息判断,混合动力车上坡或加速时,乙电极周围溶液的pH
(3)Cu2O是一种半导体材料,可通过如图2所示的电解装置制取,电解总反应式为2Cu+H2O
 Cu2O+H2↑,阴极的电极反应式是
Cu2O+H2↑,阴极的电极反应式是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】某小组同学设想利用燃料电池和电解池组合,设计一种制备硫酸和氨的装置,相关的物质及工作原理示意图如图。a、b、c、d均为惰性电极,电解池中d上有可催化N2放电的纳米颗粒,固体氧化物电解质只允许O2-在其中迁移。
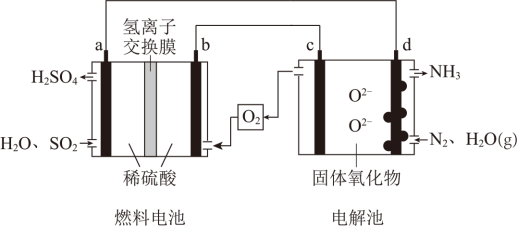
(1)燃料电池制备硫酸。
①a为_____ (填“正极”或“负极”),电极反应式为_____ 。
②H+的迁移方向为______ (填“a→b”或“b→a”)。
③电池总反应的化学方程式为______ 。
(2)电解池制备氨。下列关于电解过程的说法正确的是_____ 。
A.d上,N2被还原
B.c的电极反应:2O2--4e-=O2↑
C.固体氧化物中O2-的迁移方向为d→c
(3)燃料电池中每消耗48gSO2,在电解池中,理论上产生的NH3在标准状况下的体积为_____ L。

(1)燃料电池制备硫酸。
①a为
②H+的迁移方向为
③电池总反应的化学方程式为
(2)电解池制备氨。下列关于电解过程的说法正确的是
A.d上,N2被还原
B.c的电极反应:2O2--4e-=O2↑
C.固体氧化物中O2-的迁移方向为d→c
(3)燃料电池中每消耗48gSO2,在电解池中,理论上产生的NH3在标准状况下的体积为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】下图是一个化学过程的示意图。
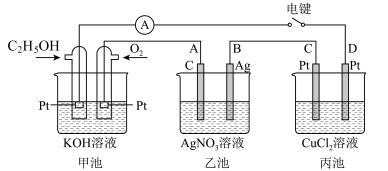
请回答下列问题:
(1)甲池中OH-移向________ 极(填“C2H5OH”或“O2”),通入C2H5OH电极的电极反应式为___________ 。
(2)乙池中A(石墨)电极的名称为________ (填“正极”“负极”“阴极”或“阳极”),并写出此电极的反应式: ________ ,
(3) 若丙中电极不变,将其溶液换成NaCl溶液,电键闭合一段时间后,甲中溶液的pH将_____ (填“增大”“减小”或“不变”);丙中溶液的pH将________ (填“增大”“减小”或“不变”)。
(4) 当乙池中B(Ag)极质量增加3.24g时,甲池中理论上消耗O2的体积为______ mL(标准状况下),乙池的pH是______ (若此时乙池中溶液的体积为500mL);

请回答下列问题:
(1)甲池中OH-移向
(2)乙池中A(石墨)电极的名称为
(3) 若丙中电极不变,将其溶液换成NaCl溶液,电键闭合一段时间后,甲中溶液的pH将
(4) 当乙池中B(Ag)极质量增加3.24g时,甲池中理论上消耗O2的体积为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】某兴趣小组利用如图装置进行一系列探究学习,请依据探究情况回答有关问题:
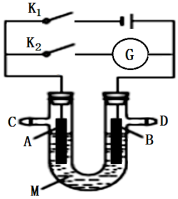
(1)若打开K1,闭合K2
①A为Zn、B为Cu、M为稀H2SO4,则A为_______ 极,溶液中H+离子向_______ 极迁移(填“A”或“B”)。
②A为Fe、B为石墨、M为NaCl饱和溶液,则B为_______ 极,发生的电极反应式为_______ ,铁将主要发生_______ 腐蚀(填“化学”“吸氧”或“析氢”)。
(2)打开K2,闭合K1
①要实现在铁表面上镀银,则A为_______ ,B为_______ , M为_______ 。
②若A、B均为石墨,M为CuSO4溶液,电解一段时间后电极A增重了0.64g,则理论上D处可收集到_______ L气体(标准状况)。

(1)若打开K1,闭合K2
①A为Zn、B为Cu、M为稀H2SO4,则A为
②A为Fe、B为石墨、M为NaCl饱和溶液,则B为
(2)打开K2,闭合K1
①要实现在铁表面上镀银,则A为
②若A、B均为石墨,M为CuSO4溶液,电解一段时间后电极A增重了0.64g,则理论上D处可收集到
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】由甲醇 、氧气和
、氧气和 溶液构成的新型手机电池,可使手机连续使用一个月才充一次电。
溶液构成的新型手机电池,可使手机连续使用一个月才充一次电。
(1)写出该电池负极电极反应式______
(2)若以该电池为电源,用石墨作电极电解含有如下离子的溶液。
电解一段时间后,当两极收集到相同体积(相同条件)的气体时(忽略溶液体积的变化及电极产物可能存在的溶解现象),阳极上发生的电极反应为______ ;阴极收集到的气体体积为(标准状况)______ 。
(3)若用该电池做电源,用石墨做电极电解硫酸铜溶液,当电路中转移 时,实际上消耗的甲醇的质量比理论上大,可能原因是
时,实际上消耗的甲醇的质量比理论上大,可能原因是______ 。
 、氧气和
、氧气和 溶液构成的新型手机电池,可使手机连续使用一个月才充一次电。
溶液构成的新型手机电池,可使手机连续使用一个月才充一次电。(1)写出该电池负极电极反应式
(2)若以该电池为电源,用石墨作电极电解含有如下离子的溶液。
| 离子 |  |  |  |  |
 |  |  |  |  |
电解一段时间后,当两极收集到相同体积(相同条件)的气体时(忽略溶液体积的变化及电极产物可能存在的溶解现象),阳极上发生的电极反应为
(3)若用该电池做电源,用石墨做电极电解硫酸铜溶液,当电路中转移
 时,实际上消耗的甲醇的质量比理论上大,可能原因是
时,实际上消耗的甲醇的质量比理论上大,可能原因是
您最近一年使用:0次



