回答下列问题:
(1)正常雨水的pH值为________
(2)常在医疗上用作消化系统X射线检查的内服药剂“钡餐”的化学式为________
(3)在粗盐的提纯实验中,欲除去其中的杂质Mg2+,应加入的试剂为________ (填化学式)。
(4)任写出一个“氮的固定”的相关方程式________
(5)新型碳化硅(SiC)陶瓷可用作耐高温结构材料和半导体材料,其中的碳原子和硅原子通过________ 键连接的 。(填“离子”或“共价”)
(6)根据元素周期律的知识,请写出新型陶瓷氮化硅的化学式________
(1)正常雨水的pH值为
(2)常在医疗上用作消化系统X射线检查的内服药剂“钡餐”的化学式为
(3)在粗盐的提纯实验中,欲除去其中的杂质Mg2+,应加入的试剂为
(4)任写出一个“氮的固定”的相关方程式
(5)新型碳化硅(SiC)陶瓷可用作耐高温结构材料和半导体材料,其中的碳原子和硅原子通过
(6)根据元素周期律的知识,请写出新型陶瓷氮化硅的化学式
更新时间:2023-04-19 08:24:27
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】氯元素是生产生活中常见的非金属元素。
(1)生物质混煤燃烧是当今能源燃烧利用的最佳方式之一,但生物质中氯含量较多,燃烧过程中会形成金属氯化物(如NaCl)和Cl2等物质,对金属炉壁造成腐蚀。
①NaCl和Cl2中化学键的类型分别是________ 和________ 。
②燃煤过程中生成的SO2会与NaCl等物质发生反应,生成硫酸盐和Cl2。若生成Cl2 22.4 L(标况)时转移电子数为4×6.02×1023,该反应的化学方程式是__________________
(2)已知:2H2O2(l)===2H2O(l)+O2(g) ΔH1=-196.46 kJ·mol-1
H2(g)+1/2O2(g)===H2O(l) ΔH2=-285.84 kJ·mol-1
Cl2(g)+H2(g)===2HCl(g) ΔH3=-184.60 kJ·mol-1
在催化剂作用下,用H2O2(l)可除去上述燃烧过程中产生的Cl2。依据上述已知反应,写出该反应的热化学方程式:________________________________ 。
(3)使用“催化转化器”可以减少尾气中的CO和NOx,转化过程中发生反应的化学方程式为CO+NOx→N2+CO2(未配平),若x=1.5,则化学方程式中CO2和N2的化学计量数之比为___ 。
(1)生物质混煤燃烧是当今能源燃烧利用的最佳方式之一,但生物质中氯含量较多,燃烧过程中会形成金属氯化物(如NaCl)和Cl2等物质,对金属炉壁造成腐蚀。
①NaCl和Cl2中化学键的类型分别是
②燃煤过程中生成的SO2会与NaCl等物质发生反应,生成硫酸盐和Cl2。若生成Cl2 22.4 L(标况)时转移电子数为4×6.02×1023,该反应的化学方程式是
(2)已知:2H2O2(l)===2H2O(l)+O2(g) ΔH1=-196.46 kJ·mol-1
H2(g)+1/2O2(g)===H2O(l) ΔH2=-285.84 kJ·mol-1
Cl2(g)+H2(g)===2HCl(g) ΔH3=-184.60 kJ·mol-1
在催化剂作用下,用H2O2(l)可除去上述燃烧过程中产生的Cl2。依据上述已知反应,写出该反应的热化学方程式:
(3)使用“催化转化器”可以减少尾气中的CO和NOx,转化过程中发生反应的化学方程式为CO+NOx→N2+CO2(未配平),若x=1.5,则化学方程式中CO2和N2的化学计量数之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】填空。
(1)有下列物质:He、N2、CaO、H2SO4、Na2S、KOH、NaHCO3。
①其中只含共价键的是___________ ;
②只含离子键的是___________ ;
③既含有共价键又含有离子键的是___________ ;
④属于共价化合物的是___________ ;
⑤属于离子化合物的是___________ 。
(2)下列变化中,不需要破坏化学键的是___________(填字母)。
(1)有下列物质:He、N2、CaO、H2SO4、Na2S、KOH、NaHCO3。
①其中只含共价键的是
②只含离子键的是
③既含有共价键又含有离子键的是
④属于共价化合物的是
⑤属于离子化合物的是
(2)下列变化中,不需要破坏化学键的是___________(填字母)。
| A.硫酸与氢氧化钠反应 | B.加热氯酸钾使其分解 |
| C.冰融化 | D.氯化钠溶于水 |
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】氢氟酸可用于半导体工业,也常用来蚀刻玻璃,其刻蚀反应原理如下:6HF + Na2SiO3 =2NaF + SiF4↑+ 3H2O完成下列填空:
(1)根据HF的________ (选填编号)大于H2O,可推断氟元素的非金属性强于氧元素。
A.酸性 B.熔沸点 C.稳定性 D.键的极性
(2)SiF4与甲烷结构相似,SiF4是含___ 键的_____ 分子(均选填“极性”或“非极性”)。刻蚀反应中的三种元素可组成同时含离子键和共价键的化合物,该化合物的电子式为__________ 。
(3)Si原子核外电子有_____ 种不同能量的电子,其中最高能量的电子处于______ 轨道。
(4)在相同条件下,Na2SiO3、CaSiO3分别与等浓度等体积的氢氟酸反应,两个反应原理相似,但前者的反应速率明显大于后者。原因是__________________________ 。
(5)同浓度的H2SO3和HF两溶液的pH为:H2SO3_____ HF(选填“>”或“<”)。浓度均为0.01 mol/L 的H2SO3和HF的1L混合溶液中,通入0.02 mol NH3充分反应后,SO32-、HSO3-、F-、NH4+浓度从大到小的顺序为:____________________ 。
已知:H2SO3 Ki1=1.54×10-2 Ki2=1.02×10-7 HF Ki=6.8×10-4 NH3·H2O Ki=1.8×10-5
(1)根据HF的
A.酸性 B.熔沸点 C.稳定性 D.键的极性
(2)SiF4与甲烷结构相似,SiF4是含
(3)Si原子核外电子有
(4)在相同条件下,Na2SiO3、CaSiO3分别与等浓度等体积的氢氟酸反应,两个反应原理相似,但前者的反应速率明显大于后者。原因是
(5)同浓度的H2SO3和HF两溶液的pH为:H2SO3
已知:H2SO3 Ki1=1.54×10-2 Ki2=1.02×10-7 HF Ki=6.8×10-4 NH3·H2O Ki=1.8×10-5
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】现有混有少量SO2杂质的CO2气体,请选用适当的实验装置,收集纯净干燥的CO2气体。

(1)要达到实验目的,按气流从左到右,各接口连接顺序正确的是_______ (填序号,下同)。
A.dcabh B.efabg C.feabg
(2)本实验除去SO2的原理是利用SO2的_______。
(3)SO2与酸性高锰酸钾溶液反应的离子方程式是_______ 。

(1)要达到实验目的,按气流从左到右,各接口连接顺序正确的是
A.dcabh B.efabg C.feabg
(2)本实验除去SO2的原理是利用SO2的_______。
| A.氧化性 | B.漂白性 | C.还原性 | D.酸性 |
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】用于分离或提纯物质的已学方法有:
A.萃取 B.分液 C.过滤 D.加热分解 E.蒸发 F. 蒸馏
下列各组混合物的分离或提纯应选上述哪种方法最合适?(把选用方法的标号填入括号内)
(1)除去Ca(OH)2溶液中悬浮的Ca(OH)2颗粒_____
(2)把饱和食盐水中的食盐提取出来_____
(3)把溴水中的溴提取出来_____
(4)除去氧化钙中的碳酸钙_____
(5)分离柴油和水的混合物_____
(6)用自来水制备医用蒸馏水_____
A.萃取 B.分液 C.过滤 D.加热分解 E.蒸发 F. 蒸馏
下列各组混合物的分离或提纯应选上述哪种方法最合适?(把选用方法的标号填入括号内)
(1)除去Ca(OH)2溶液中悬浮的Ca(OH)2颗粒
(2)把饱和食盐水中的食盐提取出来
(3)把溴水中的溴提取出来
(4)除去氧化钙中的碳酸钙
(5)分离柴油和水的混合物
(6)用自来水制备医用蒸馏水
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】(1)“电解”所用食盐水由粗盐水精制而成,精制时,为除去Mg2+和Ca2+,要加入的试剂分别为________ 、________ 。
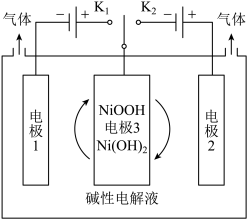
(2)氢能源是最具应用前景的能源之一,高纯氢制备是目前的研究热点。可利用太阳能光伏电池电解水制高纯氢,工作示意图如下。通过控制开关连接K1或K2,可交替得到H2和O2。
①制H2时,连接_______________ (填K1或者K2)。产生H2的电极反应式是_____________ 。
②改变开关连接方式,可得O2,写出制备氧气时电极3对应的电极反应式是_______________ 。

(2)氢能源是最具应用前景的能源之一,高纯氢制备是目前的研究热点。可利用太阳能光伏电池电解水制高纯氢,工作示意图如下。通过控制开关连接K1或K2,可交替得到H2和O2。
①制H2时,连接
②改变开关连接方式,可得O2,写出制备氧气时电极3对应的电极反应式是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】(1)现有下列几种物质:
A.青霉素 B.葡萄糖 C.苯甲酸钠 D.柠檬黄
请你根据题意,选择恰当的选项用字母代号填空:
①常用作食品着色剂的是__________ ;
②可用作食品防腐剂的是__________ ;
③有阻止多种细菌生长的功能的抗生素类药物是_________ ;
④可直接进入人体血液补充能量的是________ 。
(2)防止环境污染和改善生态环境已成为全球共识。
①下列物质不会污染室内空气的是______ (填字母代号,下同)。
A.氮气(N2) B. 一氧化碳(CO) C.甲醛( HCHO)
②工业废水需处理达标后才能排放。下列废水处理的方法不合理的是______ 。
A.要除去钢铁厂、电镀厂产生的酸性废水,可使用熟石灰[ Ca(OH)2 ]
B.要除去废水中含有的Hg2+,可使用硫化钠(Na2S)
C.要除去废水中的悬浮物,可使用氯气
③下列有关环境污染防治的叙述中,不正确的是______ 。
A.推广使用无铅汽油可减少铅污染
B.室外焚烧塑料垃圾可减少大气污染
C.淘汰含磷洗衣粉可降低水体富营养化程度
(3)材料与社会生活密不可分。
①在下列材料中,属于无机非金属材料的是______ (填字丹代号)。
A.硬币 B.聚氯乙烯塑料 C.氮化硅陶瓷
②为防止轮船的船体在海水中被腐蚀,一般在船身连接_____ (填“ 锌块”或“铜块” )。
③炒过菜的铁锅未及时洗净易被腐蚀出现红褐色锈斑,这是铁锅在潮湿的空气中发生电化学腐蚀造成的,铁锅锈蚀的正极反应方程式为______________ 。
A.青霉素 B.葡萄糖 C.苯甲酸钠 D.柠檬黄
请你根据题意,选择恰当的选项用字母代号填空:
①常用作食品着色剂的是
②可用作食品防腐剂的是
③有阻止多种细菌生长的功能的抗生素类药物是
④可直接进入人体血液补充能量的是
(2)防止环境污染和改善生态环境已成为全球共识。
①下列物质不会污染室内空气的是
A.氮气(N2) B. 一氧化碳(CO) C.甲醛( HCHO)
②工业废水需处理达标后才能排放。下列废水处理的方法不合理的是
A.要除去钢铁厂、电镀厂产生的酸性废水,可使用熟石灰[ Ca(OH)2 ]
B.要除去废水中含有的Hg2+,可使用硫化钠(Na2S)
C.要除去废水中的悬浮物,可使用氯气
③下列有关环境污染防治的叙述中,不正确的是
A.推广使用无铅汽油可减少铅污染
B.室外焚烧塑料垃圾可减少大气污染
C.淘汰含磷洗衣粉可降低水体富营养化程度
(3)材料与社会生活密不可分。
①在下列材料中,属于无机非金属材料的是
A.硬币 B.聚氯乙烯塑料 C.氮化硅陶瓷
②为防止轮船的船体在海水中被腐蚀,一般在船身连接
③炒过菜的铁锅未及时洗净易被腐蚀出现红褐色锈斑,这是铁锅在潮湿的空气中发生电化学腐蚀造成的,铁锅锈蚀的正极反应方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】硅酸盐具有特殊的性质与应用,回答下列问题:
(1)硅酸盐材料是传统无机非金属材料,下列产品不属于硅酸盐的是___________ (填序号)。
①玻璃 ②石英玻璃 ③陶瓷 ④硅芯片 ⑤砖瓦 ⑥水泥 ⑦光导纤维
(2)制备陶瓷和水泥时用到的相同原料是___________ 。
(3)磷酸钙陶瓷是一种新型无机非金属材料,可用于制造人造骨骼,这是利用了这类材料的___________(填字母)。
(4)0.1mol  与0.05mol
与0.05mol  在高温下充分反应,可生成标准状况下气体
在高温下充分反应,可生成标准状况下气体___________ L。
(5)我国成功地发射了嫦娥一号探测卫星,对月球土壤中14种元素的分布及含量进行探测。月球上的主要矿物有辉石[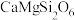 ]和橄榄石[
]和橄榄石[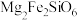 ])等,则辉石[
])等,则辉石[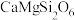 ]的氧化物形式可表示为
]的氧化物形式可表示为___________ ,斜长石[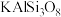 ]
]___________ (填“难”或“易”)溶于水,1mol 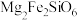 完全溶解于盐酸中消耗溶质HCl
完全溶解于盐酸中消耗溶质HCl___________ mol。
(1)硅酸盐材料是传统无机非金属材料,下列产品不属于硅酸盐的是
①玻璃 ②石英玻璃 ③陶瓷 ④硅芯片 ⑤砖瓦 ⑥水泥 ⑦光导纤维
(2)制备陶瓷和水泥时用到的相同原料是
(3)磷酸钙陶瓷是一种新型无机非金属材料,可用于制造人造骨骼,这是利用了这类材料的___________(填字母)。
| A.生物功能 | B.电学特性 | C.光学特性 | D.耐高温的特性 |
 与0.05mol
与0.05mol  在高温下充分反应,可生成标准状况下气体
在高温下充分反应,可生成标准状况下气体(5)我国成功地发射了嫦娥一号探测卫星,对月球土壤中14种元素的分布及含量进行探测。月球上的主要矿物有辉石[
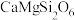 ]和橄榄石[
]和橄榄石[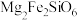 ])等,则辉石[
])等,则辉石[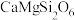 ]的氧化物形式可表示为
]的氧化物形式可表示为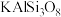 ]
]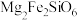 完全溶解于盐酸中消耗溶质HCl
完全溶解于盐酸中消耗溶质HCl
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】材料是现代社会发展的重要支柱。材料分为金属材料、无机非金属材料、有机高分子材料和复合材料。
(1)金属材料包括纯金属和它们的合金,常见的一些合金的硬度比其成分金属的___________ (填“大”或“小”)。钢是用途最广的合金,在钢铁厂的生产中,炽热的铁水或钢水注入模具之前,模具不得留有水,这是因为高温下,铁与水蒸气发生化学反应。其化学方程式为___________ 。
(2)传统的无机非金属多为硅酸盐材料,如制作餐具的___________ ,窗户上的玻璃、建筑用的水泥等。无机非金属材料突破了传统的硅酸盐体系,如用于制作计算机芯片的半导体材料___________ (填化学式);再如用于生产光导纤维的___________ (填化学式)。
(3)人们很早使用的棉花、羊毛、蚕丝等属于___________ 材料。小青同学想鉴别某衣物的材质为蚕丝还是纯棉的简便方法是___________ 。
(4)___________ (填物质名称)的产量可以用来衡量一个国家石油化学工业的发展水平。其聚合物可制成薄膜,用于食品、药物的包装材料。
(1)金属材料包括纯金属和它们的合金,常见的一些合金的硬度比其成分金属的
(2)传统的无机非金属多为硅酸盐材料,如制作餐具的
(3)人们很早使用的棉花、羊毛、蚕丝等属于
(4)
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】按照要求回答问题。
(1)硅是无机非金属材料的主角,Si在元素周期表中的位置___________ ,氮化硅是一种性能优异的无机非金属材料,化学式为___________ ,氮原子和硅原子通过___________ (填“离子键”或“共价键”)连接。建筑粘合剂和防火剂硅酸钠,可用 溶解在
溶解在 溶液中制备,反应的离子方程式为
溶液中制备,反应的离子方程式为___________ 。
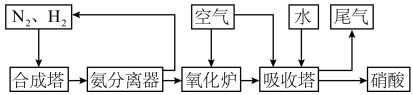
(2)氨和硝酸是重要的化工产品,工业合成氨及制备硝酸的部分流程图如下___________ 。
②氧化炉中,标准状况下
 转化为
转化为 时转移的电子数目为
时转移的电子数目为___________ 。
③吸收塔中出来的尾气 和
和 ,通过调节其体积比,可用
,通过调节其体积比,可用 溶液完全吸收,生成硫酸盐或亚硝酸盐。
溶液完全吸收,生成硫酸盐或亚硝酸盐。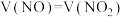 时,发生反应的化学方程式为
时,发生反应的化学方程式为___________ 。标准状况下22.4L仅含 和
和 的混合气被完全吸收,若
的混合气被完全吸收,若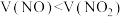 ,消耗
,消耗 的物质的是为
的物质的是为___________  。
。
(1)硅是无机非金属材料的主角,Si在元素周期表中的位置
 溶解在
溶解在 溶液中制备,反应的离子方程式为
溶液中制备,反应的离子方程式为(2)氨和硝酸是重要的化工产品,工业合成氨及制备硝酸的部分流程图如下
②氧化炉中,标准状况下

 转化为
转化为 时转移的电子数目为
时转移的电子数目为③吸收塔中出来的尾气
 和
和 ,通过调节其体积比,可用
,通过调节其体积比,可用 溶液完全吸收,生成硫酸盐或亚硝酸盐。
溶液完全吸收,生成硫酸盐或亚硝酸盐。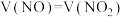 时,发生反应的化学方程式为
时,发生反应的化学方程式为 和
和 的混合气被完全吸收,若
的混合气被完全吸收,若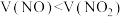 ,消耗
,消耗 的物质的是为
的物质的是为 。
。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】细菌可以促使铁、氮两种元素进行氧化还原反应,并耦合两种元素的循环。耦合循环中的部分转化如下图所示。___________ (填字母序号)。
a.N2转化为氨态氮 b.硝化过程 c.反硝化过程
(2)氨气是生产氮肥的主要原料,工业合成氨的化学方程式为___________ 。
(3)硝化过程中,含氮物质发生___________ (填“氧化”或“还原”)反应。
(4)氨态氮与亚硝态氮可以在氨氧化细菌的作用下转化为氮气。该反应中,当产生0.02 mol氮气时,转移的电子的物质的量为___________ mol。
(5)土壤中的铁循环可用于水体脱氮(脱氮是指将氮元素从水体中除去),用离子方程式说明利用土壤中的铁循环脱除水体中氨态氮的原理:___________ 。

a.N2转化为氨态氮 b.硝化过程 c.反硝化过程
(2)氨气是生产氮肥的主要原料,工业合成氨的化学方程式为
(3)硝化过程中,含氮物质发生
(4)氨态氮与亚硝态氮可以在氨氧化细菌的作用下转化为氮气。该反应中,当产生0.02 mol氮气时,转移的电子的物质的量为
(5)土壤中的铁循环可用于水体脱氮(脱氮是指将氮元素从水体中除去),用离子方程式说明利用土壤中的铁循环脱除水体中氨态氮的原理:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】I.某地出现硫酸型酸雨,现采集了一份雨水样品,其pH随时间变化如下:
(1)用化学方程式表示雨水样品pH变化的原因_______ 。
(2)如将刚采集到的雨水样品与自来水混合(自来水含氯气), pH将_______ (选填“变大”、 “变小”、 “不变”。反应的方程式为_______ 。
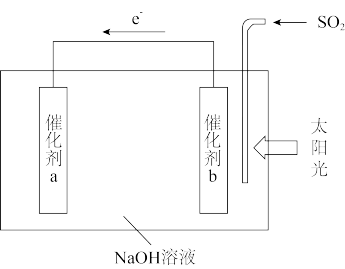
(3)我国科研人员借助太阳能,将光解水制H2与脱硫结合起来,既能大幅度提高光解水制H2的效率,又能脱除SO2,工作原理如图所示。产生标况下2.24LH2时,脱除SO2_______ g。
II.如图是土壤中发生的氮循环示意图,回答下列问题:
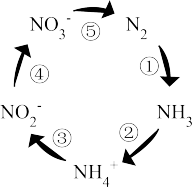
(4)固氮过程的序 号是_______ 。人工固氮的反应方程式为_______ 。
(5)为了消除NOx对大气的污染,工业上通常利用NH3还原的方法实现无害化处理,现有 NO2和NO的混合气体3L,可用相同状况下3.5L的NH3恰好使其完全转化为N2,则混合气体中NO2和NO体积之比为_______ 。
| 测试时间/h | 0 | 2 | 4 | 6 |
| pH | 4.73 | 4.55 | 4.42 | 4.41 |
(2)如将刚采集到的雨水样品与自来水混合(自来水含氯气), pH将
(3)我国科研人员借助太阳能,将光解水制H2与脱硫结合起来,既能大幅度提高光解水制H2的效率,又能脱除SO2,工作原理如图所示。产生标况下2.24LH2时,脱除SO2

II.如图是土壤中发生的氮循环示意图,回答下列问题:

(4)固氮过程的序 号是
(5)为了消除NOx对大气的污染,工业上通常利用NH3还原的方法实现无害化处理,现有 NO2和NO的混合气体3L,可用相同状况下3.5L的NH3恰好使其完全转化为N2,则混合气体中NO2和NO体积之比为
您最近一年使用:0次



