原电池是直接把化学能转化为电能的装置。
(1)如图所示:
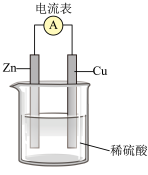
①在Cu-Zn原电池中,Zn片上发生___________ 反应(填“氧化”或“还原”)。 Cu片上发生的电极反应式为___________ 。
②外电路中电子流向___________ 极(填 “正”或“负”,下同); 内电路溶液中SO 移向
移向___________ 极。
(2)某原电池的总反应为Zn + Cu2+ = Cu + Zn2+,该原电池组成正确的是___________。
(3)某锂-空气电池的总反应为4Li + O2 + 2H2O = 4LiOH,其工作原理如图所示:
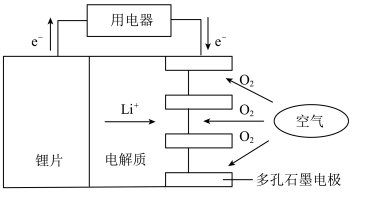
下列说法正确的是___________ 。
a.锂片作负极
b.O2发生氧化反应
c.正极的反应式为 O2 + 4e-+ 2H2O = 4OH-
(1)如图所示:

①在Cu-Zn原电池中,Zn片上发生
②外电路中电子流向
 移向
移向(2)某原电池的总反应为Zn + Cu2+ = Cu + Zn2+,该原电池组成正确的是___________。
A.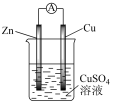 | B.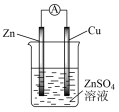 |
C. | D.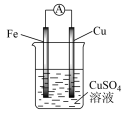 |

下列说法正确的是
a.锂片作负极
b.O2发生氧化反应
c.正极的反应式为 O2 + 4e-+ 2H2O = 4OH-
更新时间:2023-04-28 21:55:01
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】某课外活动小组用如图装置进行实验,试回答下列问题。

(1)若开始时开关K与a连接,则B极的电极反应式为______ 。
(2)若开始时开关K与b连接,则总反应的离子方程式为______ ;关于此实验的说法正确的是______ (填序号)。
A.溶液中 向A极移动
向A极移动
B.从B极处逸出的气体能使湿润的KI淀粉试纸变蓝
C.反应一段时间后通入适量 气体可恢复到电解前电解质的浓度
气体可恢复到电解前电解质的浓度
D.若标准状况下B极产生2.24L气体,则有0.2mol电子发生转移
(3)该小组同学认为,如果模拟工业上离子交换膜法制烧碱的方法,那么可以设想用如图装置电解硫酸钾溶液来制取氢气、氧气、硫酸和氢氧化钾。
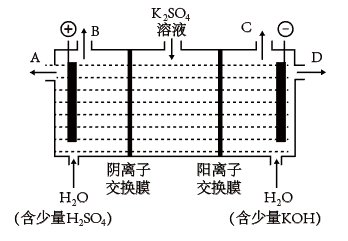
①B出口生成的气体是______ 。
②通电开始后,阴极附近溶液pH会增大,请简述原因______ ;通过阴离子交换膜的离子数______ (填“>”、“<”或“=”)通过阳离子交换膜的离子数。
③若将制得的氢气、氧气和氢氧化钾溶液组合为氢氧燃料电池,则电池正极的电极反应式为______ 。

(1)若开始时开关K与a连接,则B极的电极反应式为
(2)若开始时开关K与b连接,则总反应的离子方程式为
A.溶液中
 向A极移动
向A极移动B.从B极处逸出的气体能使湿润的KI淀粉试纸变蓝
C.反应一段时间后通入适量
 气体可恢复到电解前电解质的浓度
气体可恢复到电解前电解质的浓度D.若标准状况下B极产生2.24L气体,则有0.2mol电子发生转移
(3)该小组同学认为,如果模拟工业上离子交换膜法制烧碱的方法,那么可以设想用如图装置电解硫酸钾溶液来制取氢气、氧气、硫酸和氢氧化钾。

①B出口生成的气体是
②通电开始后,阴极附近溶液pH会增大,请简述原因
③若将制得的氢气、氧气和氢氧化钾溶液组合为氢氧燃料电池,则电池正极的电极反应式为
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
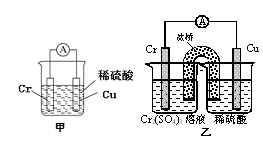
【推荐2】原电池是将化学能转化为电能的装置。分析甲、乙两原电池装置,回答下列问题:
(1)甲、乙两装置中铜电极都产生大量的无色气泡,则Cr电极是______ 极,Cu电极表面发生反应的电极反应式为_______ ;与甲装置相比,乙装置的优点是________________ ,原因是_________ 。
(2)如果将甲装置中的稀硫酸改为浓硝酸,则铜电极上无气体产生,而铬电极上产生大量的有色气体。由(1)、(2)两个实验推测金属Cr具有的两点化学性质______________________________ 。
(1)甲、乙两装置中铜电极都产生大量的无色气泡,则Cr电极是
(2)如果将甲装置中的稀硫酸改为浓硝酸,则铜电极上无气体产生,而铬电极上产生大量的有色气体。由(1)、(2)两个实验推测金属Cr具有的两点化学性质
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】(1)CO还原脱硝技术可有效降低烟气中的NOx的排放量。回答下列问题:
CO还原NO的脱硝反应:2CO(g)+2NO(g)⇌2CO2(g)+N2(g) △H
已知:CO(g)+NO2(g)⇌CO2(g)+NO(g) △H1=—226kJ•mol—1
N2(g)+2O2(g)⇌2NO2(g) △H2=+68kJ•mol—1
N2(g)+O2(g)⇌2NO(g) △H3=+183kJ•mol—1
脱硝反应△H=______ ,该反应向正反应方向自发进行的倾向很大,其原因是_______ ,有利于提高NO平衡转化率的条件是(写出两条)________ 、___________ 。
(2)直接供氨式燃料电池是以NaOH溶液为电解质的.电池反应为:4NH3+3O2=2N2+6H2O,则负极电极反应式为_________ 。
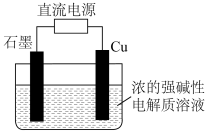
(3)用甲醇燃料电池作为直流电源,设计如图装置制取Cu2O,电解总反应为:2Cu+H2O=Cu2O+H2↑。写出阳极的电极反应式_______ 。
CO还原NO的脱硝反应:2CO(g)+2NO(g)⇌2CO2(g)+N2(g) △H
已知:CO(g)+NO2(g)⇌CO2(g)+NO(g) △H1=—226kJ•mol—1
N2(g)+2O2(g)⇌2NO2(g) △H2=+68kJ•mol—1
N2(g)+O2(g)⇌2NO(g) △H3=+183kJ•mol—1
脱硝反应△H=
(2)直接供氨式燃料电池是以NaOH溶液为电解质的.电池反应为:4NH3+3O2=2N2+6H2O,则负极电极反应式为
(3)用甲醇燃料电池作为直流电源,设计如图装置制取Cu2O,电解总反应为:2Cu+H2O=Cu2O+H2↑。写出阳极的电极反应式

您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】为验证不同化合价铁的氧化还原能力,利用下列电池装置进行实验。
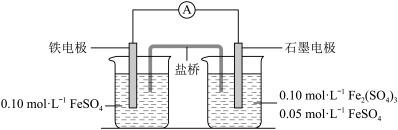
回答下列问题:
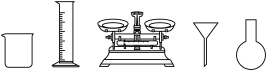
(1)由FeSO4·7H2O固体配制0.10 mol·L-1FeSO4溶液,需要的仪器有药匙、玻璃棒、________ (从下列图中选择,写出名称)。
(2)电池装置中,盐桥连接两电极电解质溶液。盐桥中阴、阳离子不与溶液中的物质发生化学反应,并且电迁移率(u∞)应尽可能地相近。根据下表数据,盐桥中应选择________ 作为电解质。
(3)电流表显示电子由铁电极流向石墨电极。可知,盐桥中的阳离子进入________ 电极溶液中。
(4)电池反应一段时间后,测得铁电极溶液中c(Fe2+)增加了0.02 mol·L-1。石墨电极上未见Fe析出。可知,石墨电极溶液中c(Fe2+)=________ 。
(5)根据(3)、(4)实验结果,可知石墨电极的电极反应式为________ ,铁电极的电极反应式为______________ 。因此,验证了Fe2+氧化性小于Fe3+还原性小于Fe。

回答下列问题:
(1)由FeSO4·7H2O固体配制0.10 mol·L-1FeSO4溶液,需要的仪器有药匙、玻璃棒、

(2)电池装置中,盐桥连接两电极电解质溶液。盐桥中阴、阳离子不与溶液中的物质发生化学反应,并且电迁移率(u∞)应尽可能地相近。根据下表数据,盐桥中应选择
| 阳离子 | u∞×108/(m2·s-1·V-1) | 阴离子 | u∞×108/(m2·s-1·V-1) |
| Li+ | 4.07 |  | 4.61 |
| Na+ | 5.19 |  | 7.40 |
| Ca2+ | 6.59 | Cl- | 7.91 |
| K+ | 7.62 |  | 8.27 |
(3)电流表显示电子由铁电极流向石墨电极。可知,盐桥中的阳离子进入
(4)电池反应一段时间后,测得铁电极溶液中c(Fe2+)增加了0.02 mol·L-1。石墨电极上未见Fe析出。可知,石墨电极溶液中c(Fe2+)=
(5)根据(3)、(4)实验结果,可知石墨电极的电极反应式为
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐2】反应Fe+H2SO4=FeSO4+H2↑的能量变化趋势如下图所示:
(1)该反应为________ 反应(填“吸热”或“放热”)。

(2)若要使该反应的反应速率加快,下列措施可行的是_______ (填字母)。
A.改铁片为铁粉 B.改稀硫酸为98%的浓硫酸 C.升高温度
(3)若将上述反应设计成原电池,画出原电池的装置图,并在图上标出正负极材料、电解质溶液名称_______ ,写出正负极电极反应式:正极__________ ,负极_______ 。
(4)氢氧燃料电池汽车作为上海世博园中的交通工具之一,以稀硫酸为介质的这种电池的正极电极反应式为_________________________ 。
(1)该反应为

(2)若要使该反应的反应速率加快,下列措施可行的是
A.改铁片为铁粉 B.改稀硫酸为98%的浓硫酸 C.升高温度
(3)若将上述反应设计成原电池,画出原电池的装置图,并在图上标出正负极材料、电解质溶液名称
(4)氢氧燃料电池汽车作为上海世博园中的交通工具之一,以稀硫酸为介质的这种电池的正极电极反应式为
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】图甲、乙所示装置进行实验,图中两个烧杯里的溶液为同浓度的稀硫酸,乙中 G 为电流计。请回答下列问题

(1)以下叙述中,正确的是_____ 。
A.甲中锌片是负极,乙中铜片是正极
B.两烧杯中铜片表面均有气泡产生
C.两烧杯中溶液的 pH 均增大
D.乙中电子从铜片经导线流向锌片
E.乙溶液中SO42-向锌片方向移动
(2)变化过程中能量转化的形式主要是:甲为_____ ;乙为____________ 。
(3)若反应过程中有 2mol 电子发生转移,则生成的氢气在标况下的体积为______ ;
(4)原电池在工作时,下列反应可以作为原电池工作时发生的反应的是:_____
A. Cu2AgNO3Cu(NO3 )22Ag
B.H2SO4+ Na2SO3==Na2SO4+ SO2+H2O
C.NaOHHClNaClH2O
D.2H2O22H2O

(1)以下叙述中,正确的是
A.甲中锌片是负极,乙中铜片是正极
B.两烧杯中铜片表面均有气泡产生
C.两烧杯中溶液的 pH 均增大
D.乙中电子从铜片经导线流向锌片
E.乙溶液中SO42-向锌片方向移动
(2)变化过程中能量转化的形式主要是:甲为
(3)若反应过程中有 2mol 电子发生转移,则生成的氢气在标况下的体积为
(4)原电池在工作时,下列反应可以作为原电池工作时发生的反应的是:
A. Cu2AgNO3Cu(NO3 )22Ag
B.H2SO4+ Na2SO3==Na2SO4+ SO2+H2O
C.NaOHHClNaClH2O
D.2H2O22H2O
您最近半年使用:0次



