结合图中信息,下列结论或推测不正确 的是
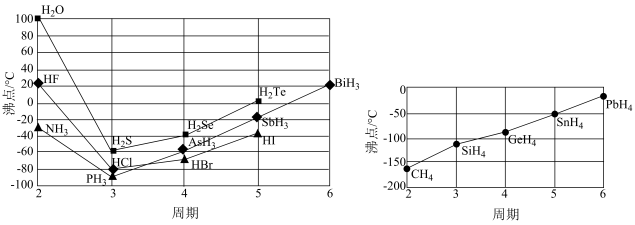

| A.第二周期元素氢化物随着相对分子质量的增加,沸点逐渐升高 |
| B.随着同主族元素氢化物的相对分子质量的增加,范德华力增大 |
| C.随原子序数的递增,第IVA族元素的氢化物的沸点逐渐升高 |
D.随原子序数的递增,除 外,第VIIA族元素氢化物的沸点逐渐增大 外,第VIIA族元素氢化物的沸点逐渐增大 |
更新时间:2023-05-02 11:48:15
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】X、Y、Z、M、W为五种短周期元素,X、Y、Z是原子序数依次递增的同周期元素,最外层电子数之和为15,X与Z可形成XZ2分子;Y与M形成的气态化合物在标准状态下的密度为0.76g/L;W的质子数是X、Y、Z、M四种元素质子数之和的一半。下列说法正确的是
| A.原子半径W>Z>Y>X>M |
| B.将XZ2通入W单质与水反应后的溶液中,生成的盐一定只有一种 |
| C.由X、Y、Z、M四种元素共同形成的化合物中一定有共价键可能有离子键 |
| D.CaX2、CaM2、CaZ2等3种化合物中,阳离子与阴离子个数比均为1:2 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】已知X、Y、Z为三种原子序数相连的元素,最高价氧化物对应水化物的酸性相对强弱是:HXO4>H2YO4>H3ZO4。则下列说法正确的是( )
| A.气态氢化物的酸性:HX>H2Y>ZH3 |
| B.非金属活泼性:Y<X<Z |
| C.原子半径:X>Y>Z |
| D.与H2化合的剧烈程度:X>Y>Z |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】原子序数逐渐增大的短周期主族元素W、X、Y、Z,元素X的氢化物水溶液可用于雕刻玻璃,元素Y的简单离子半径是同周期中最小的,W、X、Y的原子序数满足 ,元素X与Z位于同主族。下列说法正确的是
,元素X与Z位于同主族。下列说法正确的是
 ,元素X与Z位于同主族。下列说法正确的是
,元素X与Z位于同主族。下列说法正确的是A.原子半径: | B.不能电解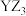 制取Y单质 制取Y单质 |
C.X、Z的简单氢化物的沸点: | D. 中各原子均满足8电子稳定结构 中各原子均满足8电子稳定结构 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】短周期元素W、X、Y、Z的原子序数依次增加。W、X、Y简单离子的电子层结构相同,X元素在短周期主族元素中原子半径最大;W的简单氢化物常温下呈液态,Y的氧化物和氯化物熔融时都能导电,X、Y和Z原子的最外层电子数之和为10。下列说法正确的是
| A.原子半径: W<Y<Z |
| B.工业上采用电解Y 的氧化物冶炼单质Y |
| C.单质沸点: W<X |
| D.W、X、Z三种元素组成的化合物水溶液一定显碱性 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列对一些事实的理论解释正确的是
| 选项 | 事实 | 理论解释 |
| A | 硫酸铵晶体中存在氢键 |  中的H与 中的H与 中的O之间的作用力大小在范德华力和共价键之间 中的O之间的作用力大小在范德华力和共价键之间 |
| B | 熔融NaCl可以导电 | 熔融态NaCl中有自由移动的电子 |
| C | 金刚石的熔点低于石墨 | 金刚石是分子晶体,石墨是共价晶体 |
| D | HF的沸点高于HCl | F的电负性大于Cl |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】丙酮、2-丙醇都是有机溶剂,它们的沸点分别为56.5℃、82.5℃。2-丙醇催化氧化制备丙酮时会有部分2-丙醇残余,利用如图装置提纯丙酮。下列叙述正确的是
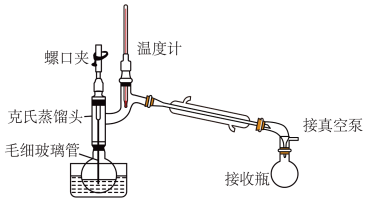

| A.2-丙醇分子内存在氢键导致沸点高于丙酮 |
| B.克氏蒸馏头的优点是避免烧瓶中液体进入接收瓶 |
| C.毛细玻璃管的作用是引入空气氧化2-丙醇 |
| D.实验中,必须控制水浴温度高于82.5℃ |
您最近一年使用:0次

 +SOCl2
+SOCl2
 ↑+HCl↑,下列说法正确的是
↑+HCl↑,下列说法正确的是 的空间结构为平面三角形
的空间结构为平面三角形

