回答下列问题
(1)①写出重晶石的化学式___________ ;
②乙烯的结构简式___________ 。
(2)工业上制取粗硅的化学方程式___________ 。
(3)稀硫酸除去多余氨气的离子方程式:___________
(1)①写出重晶石的化学式
②乙烯的结构简式
(2)工业上制取粗硅的化学方程式
(3)稀硫酸除去多余氨气的离子方程式:
更新时间:2023/05/31 22:20:58
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】氮的常见化合物在工、农业生产中用途广泛。NH3、NH3•H2O、NH4Cl、HNO3是最常见的含氮化合物。回答下列问题:
(1)工业上采用液化法从合成氨的混合气体中分离出氨,这利用了氨_________ 的性质。
(2)实验室制取氨气的化学方程式为___________ 。
(3)NH3在空气中与HCl相遇产生白烟,这里“白烟”是_______ ,打开盛浓硝酸的试剂瓶塞,瓶口有白雾出现,这里“白雾”是 _________ 。
(4)NH3和SiH4两种氢化物中,________ 更稳定。NH3是工业上制硝酸、铵盐的原料,写出NH3催化氧化的化学方程式:____________ 。
(1)工业上采用液化法从合成氨的混合气体中分离出氨,这利用了氨
(2)实验室制取氨气的化学方程式为
(3)NH3在空气中与HCl相遇产生白烟,这里“白烟”是
(4)NH3和SiH4两种氢化物中,
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】下图是氮及其化合物的“类别-价态二维图”。
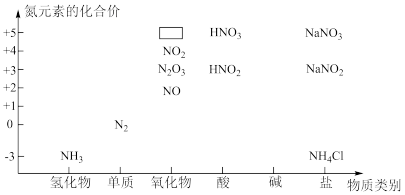
(1)写出实验室制取氨气的化学方程式:_______ 。
(2)图中方框中的化学式为_______ ,氨水电离可使溶液显碱性,写出氨水的电离方程式:_______ 。
(3)请写出氨气和氧气在催化剂和加热条件下生成NO的化学方程式:_______ 。
(4)氮氧化合物是常见的空气污染物,工业上可用氢氧化钠溶液来吸收一氧化氮和二氧化氮的混合气体,生成图中+3价的一种盐,请写出该反应的化学方程式:_______ ;每生成4mol该+3价的盐,转移_______ mol电子。

(1)写出实验室制取氨气的化学方程式:
(2)图中方框中的化学式为
(3)请写出氨气和氧气在催化剂和加热条件下生成NO的化学方程式:
(4)氮氧化合物是常见的空气污染物,工业上可用氢氧化钠溶液来吸收一氧化氮和二氧化氮的混合气体,生成图中+3价的一种盐,请写出该反应的化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】碳元素是日常生活中接触非常多的一种元素,回答下列问题。
(1)用化学方程式表示溶洞生成的反应原理:______________________ 。
(2)可用稀盐酸来鉴别Na2CO3和NaHCO3溶液,现将稀盐酸慢慢滴入碳酸钠溶液中,请写出开始阶段发生反应的离子方程式_____________________ 。
(3)写出用小苏打来治疗胃酸过多时发生反应的离子方程式:_____________ 。
氮元素在生命活动中扮演着重要的角色,回答下列与氮及其化合物有关的问题:
(4)德国化学家哈伯、波施等科学家成功地开发了将氮气转化为氨气的生产工艺。请用化学方程式表示工业合成氨的反应原理:_____________________ ,写出在氨气的出气口处,检验有氨气生成的操作:__________________________ 。
(5)将氨气通入酚酞溶液中,酚酞溶液变成红色,请用方程式解释原因:________ 。
印刷电路板是由塑料和铜箔复合而成,刻制印刷电路时要用FeCl3溶液作为“腐蚀液”溶解铜。
(6)写出该反应的离子方程式:_____________________ 。
(7)从使用过的腐蚀液中可以回收金属铜,下列试剂能实现的是__________(填序号)。
(8)向使用过的腐蚀液中通入Cl2,可使Fe2+转化为Fe3+,写出反应的离子方程式_________________ 。
(1)用化学方程式表示溶洞生成的反应原理:
(2)可用稀盐酸来鉴别Na2CO3和NaHCO3溶液,现将稀盐酸慢慢滴入碳酸钠溶液中,请写出开始阶段发生反应的离子方程式
(3)写出用小苏打来治疗胃酸过多时发生反应的离子方程式:
氮元素在生命活动中扮演着重要的角色,回答下列与氮及其化合物有关的问题:
(4)德国化学家哈伯、波施等科学家成功地开发了将氮气转化为氨气的生产工艺。请用化学方程式表示工业合成氨的反应原理:
(5)将氨气通入酚酞溶液中,酚酞溶液变成红色,请用方程式解释原因:
印刷电路板是由塑料和铜箔复合而成,刻制印刷电路时要用FeCl3溶液作为“腐蚀液”溶解铜。
(6)写出该反应的离子方程式:
(7)从使用过的腐蚀液中可以回收金属铜,下列试剂能实现的是__________(填序号)。
| A.氯气 | B.铁 | C.硝酸 | D.稀硫酸 |
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】(1)钡餐的化学式_______ 。
(2)Na2O2的电子式_______ 。
(3)用电子式表示MgCl2的形成过程_______ 。
(4)写出铜与稀硝酸发生反应的离子方程式_______ 。
(2)Na2O2的电子式
(3)用电子式表示MgCl2的形成过程
(4)写出铜与稀硝酸发生反应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】写出下列反应的离子反应方程式 :
(1)NaOH溶液和HCl溶液:___________ 。
(2)NaCl溶液和AgNO3溶液:___________ 。
(3)Ba(OH)2溶液和H2SO4溶液:___________ 。
(4)Fe与CuSO4溶液反应:___________ 。
(1)NaOH溶液和HCl溶液:
(2)NaCl溶液和AgNO3溶液:
(3)Ba(OH)2溶液和H2SO4溶液:
(4)Fe与CuSO4溶液反应:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】过氧化钠是一种淡黄色固体,它能与二氧化碳反应,在潜水艇中用作制氧剂,供人类呼吸之用。某学生为了验证这一实验,以足量 的大理石、足量 的盐酸和一定量过氧化钠样品为原料,制取O2,设计出如下实验装置:
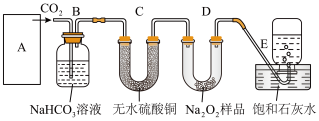
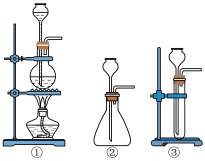
(1)A是制取CO2 的装置,应从下列图①、②、③中最好选哪个图:_______ ;
(2)B装置的作用是吸收A装置中产生的盐酸酸雾,C装置的作用是_______ ;C装置内可能出现什么现象?_______ ;
(3)在取出集气瓶后,如何检验E中收集到的气体_______ 。


(1)A是制取CO2 的装置,应从下列图①、②、③中最好选哪个图:
(2)B装置的作用是吸收A装置中产生的盐酸酸雾,C装置的作用是
(3)在取出集气瓶后,如何检验E中收集到的气体
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】按要求回答下列问题:
(1)钡餐的化学式_______ ,氨气的电子式_______ 。
(2)写出工业制粗硅的化学反应方程式_______ 。
(3)工业制乙醇的化学方程式_______ 。
(4)已知 有两种结构,其中一种是
有两种结构,其中一种是 ,另一种结构简式是
,另一种结构简式是_______ 。
(1)钡餐的化学式
(2)写出工业制粗硅的化学反应方程式
(3)工业制乙醇的化学方程式
(4)已知
 有两种结构,其中一种是
有两种结构,其中一种是 ,另一种结构简式是
,另一种结构简式是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】已知电负性Cl>H>Si, SiHCl3在浓NaOH溶液中发生反应的化学方程式为___________ 。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】元素单质及其化合物有广泛用途,请根据周期表中第三周期元素相关知识回答下列问题:
(1)按原子序数递增的顺序(稀有气体除外),以下说法正确的是___ 。
a.原子半径和离子半径均减小 b.金属性减弱,非金属性增强
c.氧化物对应的水化物碱性减弱,酸性增强 d.单质的熔点降低
(2)原子最外层电子数与次外层电子数相同的元素名称为___ ,氧化性最弱的简单阳离子是___ 。
(3)已知:
工业制镁时,电解MgCl2而不电解MgO的原因是___ ;制铝时,电解Al2O3而不电解AlCl3的原因是___ 。
(4)晶体硅(熔点1410℃)是良好的半导体材料。由粗硅制纯硅过程如下:Si(粗)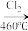 SiCl4
SiCl4 SiCl4(纯)
SiCl4(纯)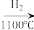 Si(纯)
Si(纯)
写出SiCl4的电子式:___ ;在上述由SiCl4制纯硅的反应中,测得每生成1.12kg纯硅需吸收akJ热量,写出该反应的热化学方程式:____ 。
(5)P2O5是非氧化性干燥剂,下列气体不能用浓硫酸干燥,可用P2O5干燥的是____ 。
a.NH3 b.HI c.SO2 d.CO2
(6)KClO3可用于实验室制O2,若不加催化剂,400℃时分解只生成两种盐,其中一种是无氧酸盐,另一种盐的阴阳离子个数比为1∶1。写出该反应的化学方程式:____ 。
(1)按原子序数递增的顺序(稀有气体除外),以下说法正确的是
a.原子半径和离子半径均减小 b.金属性减弱,非金属性增强
c.氧化物对应的水化物碱性减弱,酸性增强 d.单质的熔点降低
(2)原子最外层电子数与次外层电子数相同的元素名称为
(3)已知:
| 化合物 | MgO | Al2O3 | MgCl2 | AlCl3 |
| 类型 | 离子化合物 | 离子化合物 | 离子化合物 | 共价化合物 |
| 熔点/℃ | 2800 | 2050 | 714 | 191 |
工业制镁时,电解MgCl2而不电解MgO的原因是
(4)晶体硅(熔点1410℃)是良好的半导体材料。由粗硅制纯硅过程如下:Si(粗)
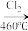 SiCl4
SiCl4 SiCl4(纯)
SiCl4(纯)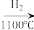 Si(纯)
Si(纯)写出SiCl4的电子式:
(5)P2O5是非氧化性干燥剂,下列气体不能用浓硫酸干燥,可用P2O5干燥的是
a.NH3 b.HI c.SO2 d.CO2
(6)KClO3可用于实验室制O2,若不加催化剂,400℃时分解只生成两种盐,其中一种是无氧酸盐,另一种盐的阴阳离子个数比为1∶1。写出该反应的化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】I.已知某链状烷烃分子中电子数为42。
(1)该烷烃的分子式为____ 。
(2)该烷烃共有____ 种同分异构体,其中:
①甲的一氯代物共有4种,则甲的名称是____ 。
②乙的所有H原子化学环境完全相同,则乙的结构简式为___ 。
③键线式是以线表示共价键,每个折点或端点表示一个碳原子,并省略书写氢原子的一种表示有机化合物结构的式子,如异丁烷(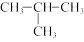 )可表示为“
)可表示为“ ”,请分析这一表示方式的要领,写出甲的键线式:
”,请分析这一表示方式的要领,写出甲的键线式:___ 。
(3)该烷烃的同系物中不存在同分异构体的共有___ 种。
II.乙烯是石油裂解气的主要成分,它的产量通常用来衡量一个国家的石油化工水平,请回答下列问题。
(4)乙烯的结构简式为____ ;分子中非极性键与极性键的数目之比为____ 。
(5)能鉴别和除去甲烷中混有的乙烯的试剂是____ (填序号)。
(6)乙烯常用于制造聚乙烯塑料,写出该反应的化学方程式____ 。
(1)该烷烃的分子式为
(2)该烷烃共有
①甲的一氯代物共有4种,则甲的名称是
②乙的所有H原子化学环境完全相同,则乙的结构简式为
③键线式是以线表示共价键,每个折点或端点表示一个碳原子,并省略书写氢原子的一种表示有机化合物结构的式子,如异丁烷(
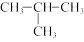 )可表示为“
)可表示为“ ”,请分析这一表示方式的要领,写出甲的键线式:
”,请分析这一表示方式的要领,写出甲的键线式:(3)该烷烃的同系物中不存在同分异构体的共有
II.乙烯是石油裂解气的主要成分,它的产量通常用来衡量一个国家的石油化工水平,请回答下列问题。
(4)乙烯的结构简式为
(5)能鉴别和除去甲烷中混有的乙烯的试剂是
| A.稀硫酸 | B.溴的四氯化碳溶液 | C.水 | D.酸性高锰酸钾溶液 |
您最近一年使用:0次
【推荐2】乙烯是石油裂解气的主要成分,它的产量通常用来衡量一个国家的石油化工水平。请回答下列问题。
(1)乙烯的电子式为___________ 。
(2)鉴别甲烷和乙烯的试剂是___________ (填字母)。
A.稀硫酸 B.溴的四氯化碳溶液
C.水 D.酸性高锰酸钾溶液
(3)下列物质中,可以通过乙烯加成反应得到的是___________ (填字母)。
A. B.
B.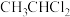 C.
C. D.
D.
(4)乙烯___________ (填“能”或“不能”)使溴的四氯化碳溶液褪色,若能,化学方程式为___________ ,反应类型是___________ 。
(1)乙烯的电子式为
(2)鉴别甲烷和乙烯的试剂是
A.稀硫酸 B.溴的四氯化碳溶液
C.水 D.酸性高锰酸钾溶液
(3)下列物质中,可以通过乙烯加成反应得到的是
A.
 B.
B.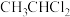 C.
C. D.
D.
(4)乙烯
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】三氯乙酸(CCl3COOH)是饮用水中常见污染物,难以直接氧化降解。通过Fe/Cu微电池法和芬顿法可将三氯乙酸除去。

(1)pH=4时,向含有三氯乙酸的水样中投入铁屑和铜屑,通过原电池反应生成的活性氢原子(H)将CCl3COOH脱氯后转化为CHCl2COOH。
①原电池反应时的负极反应式为______ 。
②写出活性氢原子(H)与CCl3COOH反应的离子方程式:______ 。
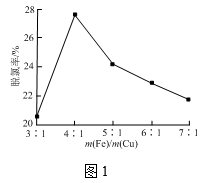
③铁屑和铜屑的总质量一定,改变铁屑和铜屑的质量比,水样中单位时间三氯乙酸的脱氯率如图1所示,当m(Fe)/m(Cu)大于4时,铁屑质量越大,脱氯率越低的原因是______ 。
(2)取上述反应后的溶液,向其中加入H2O2,发生图2所示转化,生成羟基自由基(·OH),·OH能将溶液中的CHCl2COOH等物质进一步脱氯除去。
①写出图2所示转化中反应II的离子方程式:______ 。
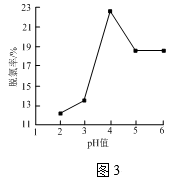
②控制水样的pH不同,所得脱氯率如图3所示,当pH>4后,脱氯率逐渐下降的原因是______ 。
③加入H2O2后需控制溶液的温度,温度过高时脱氯率减小的原因______ 。



(1)pH=4时,向含有三氯乙酸的水样中投入铁屑和铜屑,通过原电池反应生成的活性氢原子(H)将CCl3COOH脱氯后转化为CHCl2COOH。
①原电池反应时的负极反应式为
②写出活性氢原子(H)与CCl3COOH反应的离子方程式:
③铁屑和铜屑的总质量一定,改变铁屑和铜屑的质量比,水样中单位时间三氯乙酸的脱氯率如图1所示,当m(Fe)/m(Cu)大于4时,铁屑质量越大,脱氯率越低的原因是
(2)取上述反应后的溶液,向其中加入H2O2,发生图2所示转化,生成羟基自由基(·OH),·OH能将溶液中的CHCl2COOH等物质进一步脱氯除去。
①写出图2所示转化中反应II的离子方程式:
②控制水样的pH不同,所得脱氯率如图3所示,当pH>4后,脱氯率逐渐下降的原因是
③加入H2O2后需控制溶液的温度,温度过高时脱氯率减小的原因
您最近一年使用:0次



