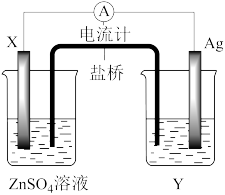
化学能在一定条件下可转化为电能。
(1)如图所示为“锌-铜-稀硫酸”原电池,请写出锌与稀硫酸反应的离子方程式是___________ 。
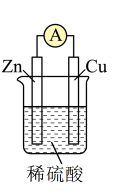
(2)装置中锌片上发生___________ (“氧化”或“还原”)反应,电极反应式是___________ ,铜片上发生反应的电极反应式是________ ,能证明化学能转化为电能的实验现象为_________ 。
(3)按照电化学装置的四个构成要素来看,Cu的作用是________ ,稀硫酸的作用是___________ 。
a.电极反应物 b.电极材料 c.离子导体 d.电子导体
(1)如图所示为“锌-铜-稀硫酸”原电池,请写出锌与稀硫酸反应的离子方程式是

(2)装置中锌片上发生
(3)按照电化学装置的四个构成要素来看,Cu的作用是
a.电极反应物 b.电极材料 c.离子导体 d.电子导体
更新时间:2023-04-23 17:45:21
|
相似题推荐
填空题
|
较易
(0.85)
解题方法
【推荐1】铜锌原电池的电极反应式
(1)锌片为_______ 极,发生___________ 反应,电极反应式为________________ ;
(2)铜片为_______ 极,发生__________ 反应,电极反应式为__________________ 。
(3)该反应的总化学方程式为___________________ 。
(1)锌片为
(2)铜片为
(3)该反应的总化学方程式为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】Ⅰ.某化学活动小组利用如图甲装置对原电池进行研究,请回答下列问题:(其中盐桥为含有饱和KCl溶液的琼脂)
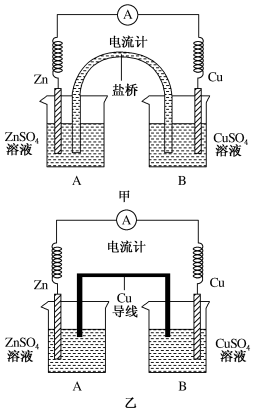
(1)在甲图装置中,当电流计中指针发生偏转时,盐桥中K+移向___________ (填“A”或“B”)烧杯。
(2)锌电极为电池的___________ 极,发生的电极反应式为___________ ;铜电极上发生的电极反应式为___________ 。
Ⅱ.该小组同学提出设想:如果将实验中的盐桥换为导线(铜制),电流表是否也发生偏转呢?带着疑问,该小组利用图乙装置进行了实验,发现电流计指针同样发生偏转。回答下列问题:
(3)对于实验中产生电流的原因,该小组进行了深入探讨,后经老师提醒注意到使用的是铜导线,烧杯A实际为原电池,B成了用电器。对于图乙,烧杯A实际是原电池的问题上,该小组成员发生了很大分歧。
①一部分同学认为是由于ZnSO4溶液水解显酸性,此时原电池实际是由Zn、Cu作电极,H2SO4溶液作为电解质溶液而构成的原电池。如果这个观点正确,那么原电池的正极反应为___________ 。
②另一部分同学认为是溶液酸性较弱,由于溶解在溶液中的氧气的作用,使得Zn、Cu之间形成原电池。如果这个观点正确,那么原电池的正极反应为___________ 。
(4)若第(3)问中②观点正确,则可以利用此原理设计电池为在偏远海岛工作的灯塔供电。其具体装置为以金属铝和石墨为电极,以海水为电解质溶液,最终铝变成氢氧化铝。请写出该电池工作时总反应的化学方程式:___________ 。

(1)在甲图装置中,当电流计中指针发生偏转时,盐桥中K+移向
(2)锌电极为电池的
Ⅱ.该小组同学提出设想:如果将实验中的盐桥换为导线(铜制),电流表是否也发生偏转呢?带着疑问,该小组利用图乙装置进行了实验,发现电流计指针同样发生偏转。回答下列问题:
(3)对于实验中产生电流的原因,该小组进行了深入探讨,后经老师提醒注意到使用的是铜导线,烧杯A实际为原电池,B成了用电器。对于图乙,烧杯A实际是原电池的问题上,该小组成员发生了很大分歧。
①一部分同学认为是由于ZnSO4溶液水解显酸性,此时原电池实际是由Zn、Cu作电极,H2SO4溶液作为电解质溶液而构成的原电池。如果这个观点正确,那么原电池的正极反应为
②另一部分同学认为是溶液酸性较弱,由于溶解在溶液中的氧气的作用,使得Zn、Cu之间形成原电池。如果这个观点正确,那么原电池的正极反应为
(4)若第(3)问中②观点正确,则可以利用此原理设计电池为在偏远海岛工作的灯塔供电。其具体装置为以金属铝和石墨为电极,以海水为电解质溶液,最终铝变成氢氧化铝。请写出该电池工作时总反应的化学方程式:
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】(1)有甲、乙两位同学均想利用原电池反应检测金属的活动性顺序,两人均用镁片和铝片作电极,但甲同学将电极放入1mol·L-1的H2SO4溶液中,乙同学将电极放入1mol·L-1的NaOH溶液中,如图所示。
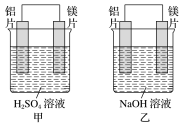
①写出甲中负极的电极反应式:___________ 。
②乙中负极反应式为___________ ,总反应的离子方程式为___________ 。
(2)将用导线相连的两个铂电极插入KOH溶液中,然后向两极分别通入CO和O2,则发生了原电池反应,该原电池中的负极反应式为___________ ;正极反应式为___________ 。

①写出甲中负极的电极反应式:
②乙中负极反应式为
(2)将用导线相连的两个铂电极插入KOH溶液中,然后向两极分别通入CO和O2,则发生了原电池反应,该原电池中的负极反应式为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】电子表和电子计算器的电池常用微型银—锌原电池,其电极分别为Zn和Ag2O,电解质溶液为KOH溶液,负极反应和总反应分别为:Zn+2OH - -2e==ZnO+H2O和Ag2O+Zn==ZnO+2Ag
(1)该原电池工作时负极区溶液的PH值_________ (上升、下降或不变)
(2)该原电池工作时电子由____ (Zn或Ag2O)极经外电路流向_______ (正或负)极。正极上发生的电极反应为__________________________________________________
(1)该原电池工作时负极区溶液的PH值
(2)该原电池工作时电子由
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】一种简单的原电池装置如图所示。

(1)锌是电池的___________ (填“正”或“负”)极,发生的电极反应式为___________ 。
(2)装置中稀硫酸的作用是___________ 。
a.电极材料 b.电极反应物 c.电子导体 d.离子导体
(3)该原电池外电路中电流方向为___________ (填“Zn→Cu”或者“Cu→Zn”)。从化学的角度分析,原电池产生电流的原因:___________ 。
(4)若将铜换成碳棒,电池总反应方程式为___________ 。
(5)下列反应通过原电池装置,可实现化学能直接转化为电能的是___________ 。
a.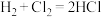
b.
c.

(1)锌是电池的
(2)装置中稀硫酸的作用是
a.电极材料 b.电极反应物 c.电子导体 d.离子导体
(3)该原电池外电路中电流方向为
(4)若将铜换成碳棒,电池总反应方程式为
(5)下列反应通过原电池装置,可实现化学能直接转化为电能的是
a.
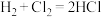
b.

c.

您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】I.某化学兴趣小组为了探索铝电极在原电池中的作用,设计并进行了以下一系列实验,实验结果记录如下:
根据上表中记录的实验现象,回答下列问题。
(1)实验1、2中Al电极的作用是否相同?___________ 。
(2)实验3中铝为___________ 极,电极反应式为 ;
;
(3)实验4中的铝为___________ 极,写出铝电极的电极反应式:___________ 。
(4)根据以上实验结果,在原电池中相对活泼的金属作正极还是作负极受到哪些因素的影响?___________ 。
Ⅱ.某种燃料电池的工作原理示意如图所示(a、b均为石墨电极)。
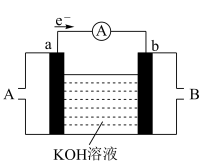
(5)假设使用的“燃料”是氢气( ),则b极的电极反应式为
),则b极的电极反应式为___________ 。
(6)假设使用的“燃料”是甲烷( ),则通入甲烷气体的电极反应式为:
),则通入甲烷气体的电极反应式为:___________ 电池工作一段时间后,电解液的碱性将___________ (填“增强”、“减弱”或“不变”)。
(7)若消耗标准状况下的甲烷4.48L,假设化学能完全转化为电能,则转移电子的数目为___________ (用 表示)。
表示)。
| 编号 | 电极材料 | 电解质溶液 | 电流表指针偏转方向 |
| 1 | Mg、Al | 稀盐酸 | 偏向Al |
| 2 | Al、Cu | 稀盐酸 | 偏向Cu |
| 3 | Al、石墨 | 稀盐酸 | 偏向石墨 |
| 4 | Mg、Al | NaOH溶液 | 偏向Mg |
(1)实验1、2中Al电极的作用是否相同?
(2)实验3中铝为
 ;
;(3)实验4中的铝为
(4)根据以上实验结果,在原电池中相对活泼的金属作正极还是作负极受到哪些因素的影响?
Ⅱ.某种燃料电池的工作原理示意如图所示(a、b均为石墨电极)。

(5)假设使用的“燃料”是氢气(
 ),则b极的电极反应式为
),则b极的电极反应式为(6)假设使用的“燃料”是甲烷(
 ),则通入甲烷气体的电极反应式为:
),则通入甲烷气体的电极反应式为:(7)若消耗标准状况下的甲烷4.48L,假设化学能完全转化为电能,则转移电子的数目为
 表示)。
表示)。
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】新冠肺炎最明显的症状就是出现发热,体温枪能快速检测人体体温。该体温枪所用的电池为一种银锌电池(如下图所示),该电池的总反应式为:Zn+Ag2O+ H2O=Zn(OH)2+ 2Ag。
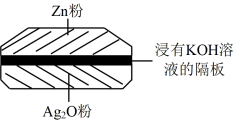
回答下列问题:
①在测体温时,电池将____ 转化为_____ (填“化学能”或“电能”) 。
②电池中电子的流向:由_______________ 到______ (填化学式),负极的电极反应式为__________ 。

回答下列问题:
①在测体温时,电池将
②电池中电子的流向:由
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】能源是现代文明的原动力,电池与我们的生活和生产密切相关。
(1)事实证明,能设计成原电池的反应通常是放热反应,下列化学反应在理论上可以设计成原电池的_____(填字母)。
(2)下图为原电池装置示意图:
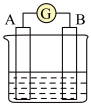
①若A为 片,B为石墨棒,电解质溶液为稀硫酸,写出负极的电极反应式:
片,B为石墨棒,电解质溶液为稀硫酸,写出负极的电极反应式:_____ ,反应过程中溶液的酸性_____ (填“增强”、“减弱”或“不变”)。一段时间后,当电池中放出2.24L(标准状况)气体时,电路中有_____ 个电子通过了导线(用 表示阿伏加德罗常数的值)。
表示阿伏加德罗常数的值)。
②若A为镁片,B为铝片,电解质为 溶液,则铝片为
溶液,则铝片为_____ (填“正极”或“负极”);写出该电极的电极反应式:_____ 。
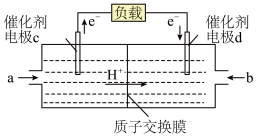
(3)燃料电池是一种具有应用前景的绿色电源, 和
和 组合形成的燃料电池的结构如图(电解质溶液是稀硫酸,质子交换膜只允许
组合形成的燃料电池的结构如图(电解质溶液是稀硫酸,质子交换膜只允许 通过)。则电极d是
通过)。则电极d是_____ (填“正极”或“负极”),则该燃料电池如下:
(4)为证明铁的金属活动性比铜强,某同学设计了如下一些方案。其中能证明铁的金属活动性比铜强的方案是
(1)事实证明,能设计成原电池的反应通常是放热反应,下列化学反应在理论上可以设计成原电池的_____(填字母)。
A. |
B.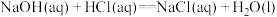 |
C.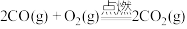 |
D.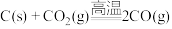 |

①若A为
 片,B为石墨棒,电解质溶液为稀硫酸,写出负极的电极反应式:
片,B为石墨棒,电解质溶液为稀硫酸,写出负极的电极反应式: 表示阿伏加德罗常数的值)。
表示阿伏加德罗常数的值)。②若A为镁片,B为铝片,电解质为
 溶液,则铝片为
溶液,则铝片为(3)燃料电池是一种具有应用前景的绿色电源,
 和
和 组合形成的燃料电池的结构如图(电解质溶液是稀硫酸,质子交换膜只允许
组合形成的燃料电池的结构如图(电解质溶液是稀硫酸,质子交换膜只允许 通过)。则电极d是
通过)。则电极d是
(4)为证明铁的金属活动性比铜强,某同学设计了如下一些方案。其中能证明铁的金属活动性比铜强的方案是
| 方案 | 现象或产物 |
A.将铁片置于 溶液中 溶液中 | 铁片上有亮红色物质析出 |
| B.将铁丝和铜丝分别在氯气燃烧 | 产物分别为 和 和 |
| C.将铁片和铜片分别置于稀硫酸溶液中 | 铁片上有气泡产生,铜片上无气泡产生 |
| D.将铁片和铜片置于盛有稀硫酸的烧杯中,并用导线连 | 铁片溶解,铜片上有气泡产生 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】将打磨光亮的镁条和铝片用导线和电流计连接,置于NaOH溶液中,观察到电流计指针先向右偏转,后立即返回,并向左偏转,此时两电极上均观察到有气体生成。
(1)电流方向表明起始时Mg作负极,原因是_______ 。
(2)电流计指针向左偏转后,Al电极上的电极反应式为_______ 。溶液中 的移动方向
的移动方向_______ 。
(1)电流方向表明起始时Mg作负极,原因是
(2)电流计指针向左偏转后,Al电极上的电极反应式为
 的移动方向
的移动方向
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】为满足不同的需要,人们应用原电池原理制作了多种电池。
(1)有人以化学反应2Zn+O2+4H+=2Zn2++2H2O为基础设计一种原电池,移入人体内作为心脏起搏器的能源,它们靠人体内血液中溶有一定浓度的O2、H+、Zn2+进行工作,则该原电池负极的电极反应为___________ 。
(2)FeCl3溶液常用于腐蚀印刷电路铜板,若将此反应设计成原电池,则负极所用电极材料为___________ ,正极反应为___________ 。
(1)有人以化学反应2Zn+O2+4H+=2Zn2++2H2O为基础设计一种原电池,移入人体内作为心脏起搏器的能源,它们靠人体内血液中溶有一定浓度的O2、H+、Zn2+进行工作,则该原电池负极的电极反应为
(2)FeCl3溶液常用于腐蚀印刷电路铜板,若将此反应设计成原电池,则负极所用电极材料为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】某同学进行如下实验,研究化学反应中的能量变化。
I.化学能与热能
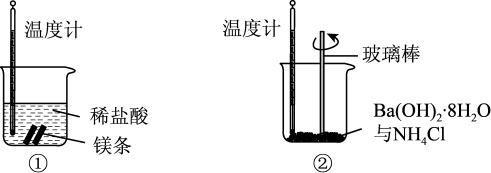
(1)反应后①中温度_______ ,②中温度_______ (填“升高”或“降低”)。由此判断①反应是_______ 反应(填“放热”或“吸热”),②中反应物总能量比生成物总能量_______ (填“高”或“低”)。
(2)②中反应的化学方程式是_______ 。
II.化学能与电能
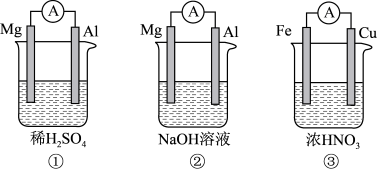
分析下图所示的四个原电池装置,回答问题
(3)①中负极材料是_______ ,正极反应式是_______ 。
(4)②中负极反应式是_______ 。
(5)③中Cu棒为_______ 极,正极反应式是_______ 。
I.化学能与热能

(1)反应后①中温度
(2)②中反应的化学方程式是
II.化学能与电能

分析下图所示的四个原电池装置,回答问题
(3)①中负极材料是
(4)②中负极反应式是
(5)③中Cu棒为
您最近一年使用:0次