依据氧化还原反应:2Ag+(aq)+Zn(s)=Zn2+(aq)+2Ag(s)设计的原电池如图所示。请回答下列问题:
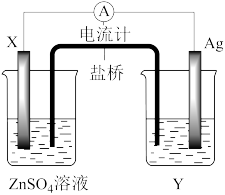
(1)电极X的材料是_______ ;电解质溶液Y是_______ ;
(2)银电极为电池的_______ 极(填“正”或“负”);X发生的电极反应为_______
(3)外电路中的电子是从_______ 电极流向_______ 电极。(填“X”或“银”)

(1)电极X的材料是
(2)银电极为电池的
(3)外电路中的电子是从
更新时间:2022-10-06 09:26:08
|
相似题推荐
填空题
|
较易
(0.85)
解题方法
【推荐1】由锌片、铜片和200 mL稀H2SO4组成的原电池如下图所示。

原电池示意图
(1)电流的方向是由___________ 极流向___________ 极。(填金属材料名称)
(2)原电池的负极反应式为___________ 。
(3)一段时间后,当在铜片上放出1.68 L(标准状况)气体时,H2SO4恰好消耗一半。有___________ 电子通过了导线。

原电池示意图
(1)电流的方向是由
(2)原电池的负极反应式为
(3)一段时间后,当在铜片上放出1.68 L(标准状况)气体时,H2SO4恰好消耗一半。有
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】(1)①0.1 mol/L (NH4)2SO4溶液中各种离子的浓度由大到小顺序为__________ 。
②用离子方程式表示NaHCO3溶液显碱性的原因:______________ 。实验室中配制FeCl3溶液时常加入________ 溶液以抑制其水解。
(2)常温下,pH=11的CH3COONa溶液中,水电离出来的c(OH-)=____________ mol/L,在pH=3的CH3COOH溶液中,水电离出的c(H+)=__________ mol/L。
(3)利用反应Cu + H2O2 + H2SO4 = CuSO4 + 2H2O设计一个原电池,回答下列问题:
①负极材料为____________ ;正极反应式为__________________________ 。
②反应过程中SO42-向_______ 极移动。
③当电路中转移0.1mol电子时,电解液质量(不含电极)增加了______ 克。
②用离子方程式表示NaHCO3溶液显碱性的原因:
(2)常温下,pH=11的CH3COONa溶液中,水电离出来的c(OH-)=
(3)利用反应Cu + H2O2 + H2SO4 = CuSO4 + 2H2O设计一个原电池,回答下列问题:
①负极材料为
②反应过程中SO42-向
③当电路中转移0.1mol电子时,电解液质量(不含电极)增加了
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】依据氧化还原反应:2Ag+(aq)+Cu(s)=Cu2+(aq)+2Ag(s)设计的原电池如图所示。请回答下列问题:

(1)电极X的上发生的电极反应为______ 反应(氧化或还原);电解质溶液Y是________ ;
(2)银电极为电池的_____ 极,发生的电极反应式为_______ ;
(3)外电路中的电子__________ (填“流出”或“流向”)Ag电极。
(4)当有1.6 g铜溶解时,银棒增重______ g。
(5)现有如下两个反应:(A))NaOH+HCl=NaCl+H2O (B)2FeCl3+Fe=3FeCl2
①根据两反应本质,分别判断能否用于设计原电池,如果不能,说明其原因_______________ 。
②如果可以,写出正极反应式:___________ 。

(1)电极X的上发生的电极反应为
(2)银电极为电池的
(3)外电路中的电子
(4)当有1.6 g铜溶解时,银棒增重
(5)现有如下两个反应:(A))NaOH+HCl=NaCl+H2O (B)2FeCl3+Fe=3FeCl2
①根据两反应本质,分别判断能否用于设计原电池,如果不能,说明其原因
②如果可以,写出正极反应式:
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】理论上讲,任何自发的氧化还原反应都可以设计成原电池 请你利用下列反应“
请你利用下列反应“ ”设计一个化学电池,并回答下列问题:
”设计一个化学电池,并回答下列问题:
①该电池的正极材料是______ ,负极材料是 ______ ,电解质溶液是 ______ 。
②在外电路中,电流方向是从______ 极到 ______ 极(填“正”或“负”)。
③正极上出现的现象是______ .负极上出现的现象是 ______ 。
 请你利用下列反应“
请你利用下列反应“ ”设计一个化学电池,并回答下列问题:
”设计一个化学电池,并回答下列问题:①该电池的正极材料是
②在外电路中,电流方向是从
③正极上出现的现象是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】有科学家预言,氢能将成为21世纪的主要能源,而且是一种理想的绿色能源。在101 kPa下,1 g氢气完全燃烧生成液态水放出142.9 kJ的热量。
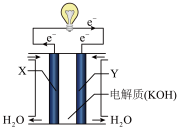
(1)请写出表示氢气燃烧热的热化学方程式__________________ 。
(2)将上述反应设计成下图所示的原电池,其中Y为________ 极(填“正”或“负”),该极电极反应式为___________________ 。

(1)请写出表示氢气燃烧热的热化学方程式
(2)将上述反应设计成下图所示的原电池,其中Y为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】电子表和电子计算器的电池常用微型银—锌原电池,其电极分别为Zn和Ag2O,电解质溶液为KOH溶液,负极反应和总反应分别为:Zn+2OH - -2e==ZnO+H2O和Ag2O+Zn==ZnO+2Ag
(1)该原电池工作时负极区溶液的PH值_________ (上升、下降或不变)
(2)该原电池工作时电子由____ (Zn或Ag2O)极经外电路流向_______ (正或负)极。正极上发生的电极反应为__________________________________________________
(1)该原电池工作时负极区溶液的PH值
(2)该原电池工作时电子由
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】完成下列问题。
(1)已知在2L的密闭容器中进行如下可逆反应,各物质的有关数据如下:
请回答下列问题。
①该可逆反应的化学方程式可表示为___________ 。
②从反应开始到2s末,A的转化率为___________ 。
③下列事实能够说明上述反应在该条件下已经达到化学平衡状态的是___________ (填序号)
A.υB(消耗)= υC(生成)
B.容器内气体的总压强保持不变
C.容器内气体的密度不变
D.υA:υB:υC=3:1:2
E.容器内气体C的物质的量分数保持不变
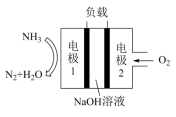
(2)①锌电池有望代替铅蓄电池,它的构成材料是锌、空气、某种电解质溶液,发生的总反应方程式是2Zn+O2=2ZnO。则该电池的负极材料是___________ 。
②瑞典ASES公司设计的曾用于驱动潜艇的液氨-液氧燃料电池的示意图如图,该燃料电池工作时,电池的总反应方程式为________ ;负极的电极反应式为________ 。
(1)已知在2L的密闭容器中进行如下可逆反应,各物质的有关数据如下:
aA(g)+bB(g)  cC(g) cC(g) | |
| 起始物质的量浓度/( mol∙L−1) | 1.5 1 0 |
| 2s末物质的量浓度/( mol∙L−1) | 0.9 0.8 0.4 |
①该可逆反应的化学方程式可表示为
②从反应开始到2s末,A的转化率为
③下列事实能够说明上述反应在该条件下已经达到化学平衡状态的是
A.υB(消耗)= υC(生成)
B.容器内气体的总压强保持不变
C.容器内气体的密度不变
D.υA:υB:υC=3:1:2
E.容器内气体C的物质的量分数保持不变
(2)①锌电池有望代替铅蓄电池,它的构成材料是锌、空气、某种电解质溶液,发生的总反应方程式是2Zn+O2=2ZnO。则该电池的负极材料是
②瑞典ASES公司设计的曾用于驱动潜艇的液氨-液氧燃料电池的示意图如图,该燃料电池工作时,电池的总反应方程式为

您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】我国首创的以铝、空气、海水为能源的新型海水标志灯已研制成功。这种灯以海水为电解质,靠空气中的氧气使铝不断氧化而产生电能,其正极电极反应式为:
 ,负极电极反应式为:
,负极电极反应式为: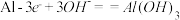 ,只要将灯放入海水中,数分钟后就会发出耀眼的光,其能量比电池高20~50倍。
,只要将灯放入海水中,数分钟后就会发出耀眼的光,其能量比电池高20~50倍。
(1)此种新型电池的负极材料是_______
(2)电池总反应式为_______

 ,负极电极反应式为:
,负极电极反应式为: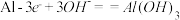 ,只要将灯放入海水中,数分钟后就会发出耀眼的光,其能量比电池高20~50倍。
,只要将灯放入海水中,数分钟后就会发出耀眼的光,其能量比电池高20~50倍。(1)此种新型电池的负极材料是
(2)电池总反应式为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】某化学小组探究不同条件下化学能转变为电能的装置如下图。回答问题:
(1)若电极a为 、电极b为
、电极b为 、电解质溶液为稀硫酸时,正极的电极反应式为:
、电解质溶液为稀硫酸时,正极的电极反应式为:_______ 。
(2)若电极a为 、电极b为
、电极b为 、电解质溶液为浓硝酸时,该装置
、电解质溶液为浓硝酸时,该装置_______ (填“能”或“不能”)形成原电池。
(3)燃料电池的工作原理是将燃料和氧化剂(如 )反应所放出的化学能直接转化为电能.现设计一燃料电池,以电极a为正极,电极b为负极,
)反应所放出的化学能直接转化为电能.现设计一燃料电池,以电极a为正极,电极b为负极, 为燃料,采用酸性溶液为电解液;则
为燃料,采用酸性溶液为电解液;则 应通入
应通入_______ 极(填a或b,下同),电子从_______ 极流出。电池的负极反应式为:_______ 。

(1)若电极a为
 、电极b为
、电极b为 、电解质溶液为稀硫酸时,正极的电极反应式为:
、电解质溶液为稀硫酸时,正极的电极反应式为:(2)若电极a为
 、电极b为
、电极b为 、电解质溶液为浓硝酸时,该装置
、电解质溶液为浓硝酸时,该装置(3)燃料电池的工作原理是将燃料和氧化剂(如
 )反应所放出的化学能直接转化为电能.现设计一燃料电池,以电极a为正极,电极b为负极,
)反应所放出的化学能直接转化为电能.现设计一燃料电池,以电极a为正极,电极b为负极, 为燃料,采用酸性溶液为电解液;则
为燃料,采用酸性溶液为电解液;则 应通入
应通入
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
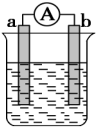
【推荐1】(1)如图是银锌原电池装置的示意图,请回答:
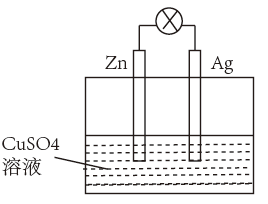
锌为___________ 极,该电极上发生___________ 反应(填“氧化”或“还原”),该电极的电极反应式为___________ ,总反应离子方程式为___________ 。
(2)如图为某原电池装置示意图,若A为Cu,B为石墨,电解质为FeCl3溶液,工作时的总反应为:2FeCl3+Cu=FeCl2+CuCl2。
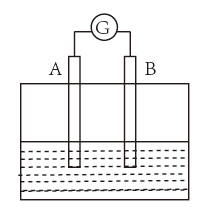
写出B的电极反应式___________ ;该电池在工作时,A电极的质量将___________ (填“增加”或“减少”或“不变”)。
(3)如图是一种氢气燃料电池的原理图:
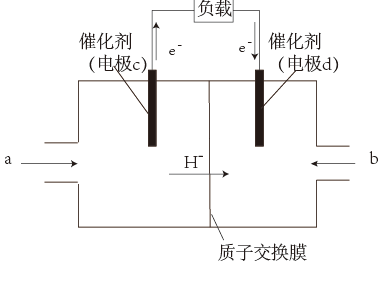
a极通入的气体是___________ ,正极的电极反应式为___________ 。

锌为
(2)如图为某原电池装置示意图,若A为Cu,B为石墨,电解质为FeCl3溶液,工作时的总反应为:2FeCl3+Cu=FeCl2+CuCl2。

写出B的电极反应式
(3)如图是一种氢气燃料电池的原理图:

a极通入的气体是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】氢氧燃料电池以KOH溶液作电解质溶液时,工作一段时间后,电解质溶液的浓度将________ (填“减小”、“增大”或“不变”,下同),溶液的pH________ 。
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】氢气是一种高效清洁的可再生能源,请回答:
(1)由氢气和氧气反应生成1mol水蒸气放热241.8kJ,写出该反应的热化学方程式:_____________ 。
(2)氢氧燃料电池一般是以惰性金属铂(Pt)或石墨做电极材料,若电解质溶液为KOH,则负极上的电极反应式为__________________________________ 。
(1)由氢气和氧气反应生成1mol水蒸气放热241.8kJ,写出该反应的热化学方程式:
(2)氢氧燃料电池一般是以惰性金属铂(Pt)或石墨做电极材料,若电解质溶液为KOH,则负极上的电极反应式为
您最近一年使用:0次



