完成下列问题。
(1)已知在2L的密闭容器中进行如下可逆反应,各物质的有关数据如下:
请回答下列问题。
①该可逆反应的化学方程式可表示为___________ 。
②从反应开始到2s末,A的转化率为___________ 。
③下列事实能够说明上述反应在该条件下已经达到化学平衡状态的是___________ (填序号)
A.υB(消耗)= υC(生成)
B.容器内气体的总压强保持不变
C.容器内气体的密度不变
D.υA:υB:υC=3:1:2
E.容器内气体C的物质的量分数保持不变
(2)①锌电池有望代替铅蓄电池,它的构成材料是锌、空气、某种电解质溶液,发生的总反应方程式是2Zn+O2=2ZnO。则该电池的负极材料是___________ 。
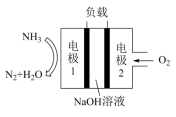
②瑞典ASES公司设计的曾用于驱动潜艇的液氨-液氧燃料电池的示意图如图,该燃料电池工作时,电池的总反应方程式为________ ;负极的电极反应式为________ 。
(1)已知在2L的密闭容器中进行如下可逆反应,各物质的有关数据如下:
aA(g)+bB(g)  cC(g) cC(g) | |
| 起始物质的量浓度/( mol∙L−1) | 1.5 1 0 |
| 2s末物质的量浓度/( mol∙L−1) | 0.9 0.8 0.4 |
①该可逆反应的化学方程式可表示为
②从反应开始到2s末,A的转化率为
③下列事实能够说明上述反应在该条件下已经达到化学平衡状态的是
A.υB(消耗)= υC(生成)
B.容器内气体的总压强保持不变
C.容器内气体的密度不变
D.υA:υB:υC=3:1:2
E.容器内气体C的物质的量分数保持不变
(2)①锌电池有望代替铅蓄电池,它的构成材料是锌、空气、某种电解质溶液,发生的总反应方程式是2Zn+O2=2ZnO。则该电池的负极材料是
②瑞典ASES公司设计的曾用于驱动潜艇的液氨-液氧燃料电池的示意图如图,该燃料电池工作时,电池的总反应方程式为

更新时间:2023-05-11 22:13:12
|
相似题推荐
填空题
|
较易
(0.85)
【推荐1】在一密闭的2L容器中装有4molSO2和2molO2,在一定条件下开始反应。2min末测得容器中有1.6molSO2,请计算:
(1)2min末SO3的浓度_______ ;
(2)2min内SO2的平均反应速率_______ 。
(3)2min内O2的转化率_______ 。
(1)2min末SO3的浓度
(2)2min内SO2的平均反应速率
(3)2min内O2的转化率
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】在一定温度下,向体积为2 L的恒容密闭容器中充入一定量的A、B发生化学反应(除物质D为固体外,其余的物质均为气体),各物质的含量随时间的变化情况如图所示,请回答下列问题:

(1)写出该反应的化学方程式_______ ,0~2 min内用C表示的化学反应速率v(C)=_______
(2)该反应在2 min时改变了某一条件,则该条件可能为_______ 。
(3)下列能说明反应达到平衡的是_______(填标号)。
(4)t时刻,此时压强与初始压强的比值为46:49,则此时A物质的转化率为_______ %,此时该反应_______ (填“是”或“否”)达到平衡。

(1)写出该反应的化学方程式
(2)该反应在2 min时改变了某一条件,则该条件可能为
(3)下列能说明反应达到平衡的是_______(填标号)。
| A.当有1mol A被消耗的同时有1mol D被消耗 |
| B.反应体系内气体的密度不再发生变化 |
| C.A与C的浓度之比为2:3 |
| D.反应体系内气体的压强不再发生变化 |
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】为减弱温室效应,除了减少CO2的排放、植树造林、将液态CO2注入深海等措施外,还有一种思路是将CO2转化成其它可燃物质。如工业上已实现CO2和H2反应生成甲醇的转化。已知:在一恒温、恒容密闭容器中充入l mol CO2和3mol H2,一定条件下发生反应:CO2(g)+3H2(g)  CH3OH(g)+H2O(g) △H= -49.0 kJ/mol,测得CO2和CH3OH(g)的浓度随时间变化如下图所示。请回答:
CH3OH(g)+H2O(g) △H= -49.0 kJ/mol,测得CO2和CH3OH(g)的浓度随时间变化如下图所示。请回答:
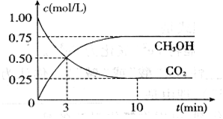
(1)达到平衡的时刻是____________ min(填“3”或“10”)。在前10min内,用CO2表示的反应速率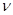 (CO2)=
(CO2)=________
(2)能判断该反应达到化学平衡状态的依据是____________ 。
a.容器压强不变 b.混合气体中c(CO2)不变
c.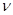 (CH3OH)=
(CH3OH)=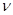 (H2O) d.c(CH3OH)=c(H2O)
(H2O) d.c(CH3OH)=c(H2O)
(3)为了提高H2的转化率,可采取__________ (填“增大”或“减小”)CO2浓度的措施。
(4)达平衡后,H2的转化率是_____________ 。平衡常数K=____________ 。(计算结果保留一位小数)
 CH3OH(g)+H2O(g) △H= -49.0 kJ/mol,测得CO2和CH3OH(g)的浓度随时间变化如下图所示。请回答:
CH3OH(g)+H2O(g) △H= -49.0 kJ/mol,测得CO2和CH3OH(g)的浓度随时间变化如下图所示。请回答:
(1)达到平衡的时刻是
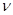 (CO2)=
(CO2)=(2)能判断该反应达到化学平衡状态的依据是
a.容器压强不变 b.混合气体中c(CO2)不变
c.
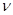 (CH3OH)=
(CH3OH)=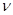 (H2O) d.c(CH3OH)=c(H2O)
(H2O) d.c(CH3OH)=c(H2O)(3)为了提高H2的转化率,可采取
(4)达平衡后,H2的转化率是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】化学在生活、科研中有重要的作用。
(1)将 转化为甲醇是实现碳中和途径之一,原理为:
转化为甲醇是实现碳中和途径之一,原理为: 。在恒温恒容条件下反应
。在恒温恒容条件下反应 ,能说明反应一定达到平衡状态的是_______。
,能说明反应一定达到平衡状态的是_______。
(2)在一定温度下,体积为1L的密闭容器中,充入2mol 和6mol
和6mol ,测得
,测得 和
和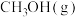 的浓度随时间变化如图所示。
的浓度随时间变化如图所示。

①2min时的
_______  (填写“大于”、“小于”、“等于”);
(填写“大于”、“小于”、“等于”);
②2min~5min的平均反应速率
_______ 。
(3)汽车尾气中含有的NO是造成城市空气污染的主要因素之一,通过NO传感器可监测汽车尾气中NO含量,其工作原理如图所示:

①NiO电极为_______ (填“正极”或“负极”)。
②Pt电极上发生的电极反应式为_______ 。
(4)一种新型催化剂能使NO和CO发生反应 。为验证温度和催化剂的比表面积对化学反应速率的影响规律,某同学设计了如下三组实验。
。为验证温度和催化剂的比表面积对化学反应速率的影响规律,某同学设计了如下三组实验。
①a=_______ ,b=_______ 。
②能验证温度对化学反应速率影响规律的实验是_______ (填实验编号)。
(1)将
 转化为甲醇是实现碳中和途径之一,原理为:
转化为甲醇是实现碳中和途径之一,原理为: 。在恒温恒容条件下反应
。在恒温恒容条件下反应 ,能说明反应一定达到平衡状态的是_______。
,能说明反应一定达到平衡状态的是_______。| A.氢气的浓度保持不变 |
| B.气体的压强不变 |
| C.体系的密度不变 |
D.生成1mol 同时反应1mol 同时反应1mol |
 和6mol
和6mol ,测得
,测得 和
和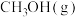 的浓度随时间变化如图所示。
的浓度随时间变化如图所示。
①2min时的

 (填写“大于”、“小于”、“等于”);
(填写“大于”、“小于”、“等于”);②2min~5min的平均反应速率

(3)汽车尾气中含有的NO是造成城市空气污染的主要因素之一,通过NO传感器可监测汽车尾气中NO含量,其工作原理如图所示:

①NiO电极为
②Pt电极上发生的电极反应式为
(4)一种新型催化剂能使NO和CO发生反应
 。为验证温度和催化剂的比表面积对化学反应速率的影响规律,某同学设计了如下三组实验。
。为验证温度和催化剂的比表面积对化学反应速率的影响规律,某同学设计了如下三组实验。| 实验编号 | T(℃) | NO初始浓度 (  ) ) | CO初始浓度( ) ) | 催化剂的比表面积(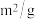 ) ) |
| I | 280 |  |  | 82 |
| II | 280 |  | b | 124 |
| III | 35 | a |  | 82 |
②能验证温度对化学反应速率影响规律的实验是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】(1)实验室用过量的锌和一定体积的盐酸制取氢气,如果反应太激烈,为了减缓反应速率而又不减少产生氢气的量,在盐酸中分别加入等体积的下列溶液,你认为可行的是__ (填字母)。
A.CH3COONa溶液 B.NaNO3溶液 C.KCl溶液 D.Na2CO3溶液
(2)下列说法可以证明H2(g)+I2(g) ⇌ 2HI(g)已达平衡状态的是__ 。
A.单位时间内生成nmolH2的同时,生成nmolHI
B.一个H—H键断裂的同时有两个H—I键断裂
C.温度和体积一定时,混合气体颜色不再变化
D.反应速率v(H2)=v(I2)= v(HI)
v(HI)
E.温度和体积一定时,容器内压强不再变化
F.温度和体积一定时,混合气体的密度不再变化
A.CH3COONa溶液 B.NaNO3溶液 C.KCl溶液 D.Na2CO3溶液
(2)下列说法可以证明H2(g)+I2(g) ⇌ 2HI(g)已达平衡状态的是
A.单位时间内生成nmolH2的同时,生成nmolHI
B.一个H—H键断裂的同时有两个H—I键断裂
C.温度和体积一定时,混合气体颜色不再变化
D.反应速率v(H2)=v(I2)=
 v(HI)
v(HI)E.温度和体积一定时,容器内压强不再变化
F.温度和体积一定时,混合气体的密度不再变化
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】某化学小组探究不同条件下化学能转变为电能的装置如下图。回答问题:
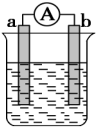
(1)若电极a为 、电极b为
、电极b为 、电解质溶液为稀硫酸时,正极的电极反应式为:
、电解质溶液为稀硫酸时,正极的电极反应式为:_______ 。
(2)若电极a为 、电极b为
、电极b为 、电解质溶液为浓硝酸时,该装置
、电解质溶液为浓硝酸时,该装置_______ (填“能”或“不能”)形成原电池。
(3)燃料电池的工作原理是将燃料和氧化剂(如 )反应所放出的化学能直接转化为电能.现设计一燃料电池,以电极a为正极,电极b为负极,
)反应所放出的化学能直接转化为电能.现设计一燃料电池,以电极a为正极,电极b为负极, 为燃料,采用酸性溶液为电解液;则
为燃料,采用酸性溶液为电解液;则 应通入
应通入_______ 极(填a或b,下同),电子从_______ 极流出。电池的负极反应式为:_______ 。

(1)若电极a为
 、电极b为
、电极b为 、电解质溶液为稀硫酸时,正极的电极反应式为:
、电解质溶液为稀硫酸时,正极的电极反应式为:(2)若电极a为
 、电极b为
、电极b为 、电解质溶液为浓硝酸时,该装置
、电解质溶液为浓硝酸时,该装置(3)燃料电池的工作原理是将燃料和氧化剂(如
 )反应所放出的化学能直接转化为电能.现设计一燃料电池,以电极a为正极,电极b为负极,
)反应所放出的化学能直接转化为电能.现设计一燃料电池,以电极a为正极,电极b为负极, 为燃料,采用酸性溶液为电解液;则
为燃料,采用酸性溶液为电解液;则 应通入
应通入
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】人们应用原电池原理制作了多种电池以满足不同的需要。在现代生活、生产和科学技术发展中,电池发挥着越来越重要的作用。请根据题中提供的信息,回答下列问题:
(1)直接提供电能的反应一般是放热反应,下列反应能设计成原电池的是_______(填字母,下同)。
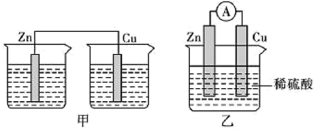
(2)为了探究原电池的工作原理,某研究性学习小组进行了如下实验。分别按图1中甲、乙所示装置进行实验,甲中两个烧杯中的溶液为同浓度的稀硫酸。_______ (填字母)。
A.甲中锌片是负极,乙中铜片是正极
B.两装置中铜片表面均有气泡产生
C.乙的外电路中电流方向Cu→Zn
D.如果将装置乙中锌片换成铁片,则电路中的电流方向不变
②在乙实验中,某同学发现不仅在铜片上有气泡产生,而且在锌片上也产生了气体,分析原因可能是_______ 。
③在乙实验中,如果把硫酸换成硫酸铜溶液,可观察到正极_______ (填实验现象),其对应的电极反应式为_______ 。
(3)某氢氧燃料电池装置如图所示,a、b均为惰性电极。_______ (填“A”或“B”)口通入。
②负极上的电极反应式为_______ ,当电路中转移 电子时,理论上负极通入的气体在标准状况下的体积为
电子时,理论上负极通入的气体在标准状况下的体积为_______ L。
(1)直接提供电能的反应一般是放热反应,下列反应能设计成原电池的是_______(填字母,下同)。
A. 与 与 反应 反应 | B.氢氧化钠与稀盐酸反应 |
C.灼热的炭与 反应 反应 | D. 与 与 燃烧反应 燃烧反应 |
A.甲中锌片是负极,乙中铜片是正极
B.两装置中铜片表面均有气泡产生
C.乙的外电路中电流方向Cu→Zn
D.如果将装置乙中锌片换成铁片,则电路中的电流方向不变
②在乙实验中,某同学发现不仅在铜片上有气泡产生,而且在锌片上也产生了气体,分析原因可能是
③在乙实验中,如果把硫酸换成硫酸铜溶液,可观察到正极
(3)某氢氧燃料电池装置如图所示,a、b均为惰性电极。
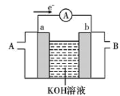
②负极上的电极反应式为
 电子时,理论上负极通入的气体在标准状况下的体积为
电子时,理论上负极通入的气体在标准状况下的体积为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】原电池的发明是化学对人类的一项重大贡献。
(1)一种新型燃料电池,它以多孔铂板为两个电极插入氢氧化钠溶液中,然后分别向两极通入氢气和氧气而获得电能。通入氢气的电极反应式为_____ 。放电一段时间后,负极附近溶液的pH_____ (填“升高”“降低”或“不变”)。
(2)电子工业上常利用FeCl3溶液腐蚀铜板制作印刷电路,其反应的离子方程式为_________________ 。请把该反应设计成一个原电池,在方框内面出原电池装置图(要求:标明电极材料和电解质溶液)。
_____
(3)常温下,将除去表面氧化膜的铝片、铜片插入浓HNO3中组成原电池装置如图甲所示, 测得原电池的电流强度(I)随时间(t)的变化如图乙所示,反应过程中有红棕色气体产生。

t1s 前,原电池的正极的电极反应式为____________________________ ,溶液中的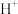 向
向_____________ (填“Al”或“Cu”)极移动。t1s后,外电路中电子流动方向发生改变,其原因是_____ 。
(1)一种新型燃料电池,它以多孔铂板为两个电极插入氢氧化钠溶液中,然后分别向两极通入氢气和氧气而获得电能。通入氢气的电极反应式为
(2)电子工业上常利用FeCl3溶液腐蚀铜板制作印刷电路,其反应的离子方程式为

(3)常温下,将除去表面氧化膜的铝片、铜片插入浓HNO3中组成原电池装置如图甲所示, 测得原电池的电流强度(I)随时间(t)的变化如图乙所示,反应过程中有红棕色气体产生。

t1s 前,原电池的正极的电极反应式为
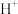 向
向
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】阿波罗宇宙飞船上使用的是氢氧燃料电池,其电池总反应为2H2+O2===2H2O。
若电解质溶液为KOH溶液,其电极反应式分别为:
负极_____________________ ,正极_______________________ 。
若电解质溶液为稀H2SO4,其电极反应式分别为:
负极_______________________ ,正极______________________ 。
若电解质溶液为KOH溶液,其电极反应式分别为:
负极
若电解质溶液为稀H2SO4,其电极反应式分别为:
负极
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】能源与人类的生存和发展息息相关,化学反应在人类利用能源的历史过程中充当重要的角色。回答下列问题:
(1)科学家最近研制出利用太阳能产生激光,使海水分解。太阳光分解海水时,水分解断裂的化学键是_______ (填“离子键”或“共价键”)。
(2)下列化学反应在理论上可以设计成原电池的是_______(填字母)。
(3)如图为某燃料电池的结构示意图,电解质溶液为NaOH溶液,电极材料为疏松多孔的石墨棒。回答下列问题:

若该燃料电池为氢氧燃料电池。
①a极通入的物质为_______ (填物质名称),电解质溶液中的OH-移向_______ (“负”或“正”)。
②写出此氢氧燃料电池工作时总反应方程式:_______ 。
(1)科学家最近研制出利用太阳能产生激光,使海水分解。太阳光分解海水时,水分解断裂的化学键是
(2)下列化学反应在理论上可以设计成原电池的是_______(填字母)。
A.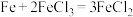 | B. |
C. | D.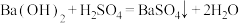 |

若该燃料电池为氢氧燃料电池。
①a极通入的物质为
②写出此氢氧燃料电池工作时总反应方程式:
您最近一年使用:0次

 2C2H5OH+2CO2。当C6H12O6减少的速率是0.5 mol·L−1·h−1时,C2H5OH增加的速率是
2C2H5OH+2CO2。当C6H12O6减少的速率是0.5 mol·L−1·h−1时,C2H5OH增加的速率是

