在一定温度下,向体积为2 L的恒容密闭容器中充入一定量的A、B发生化学反应(除物质D为固体外,其余的物质均为气体),各物质的含量随时间的变化情况如图所示,请回答下列问题:

(1)写出该反应的化学方程式_______ ,0~2 min内用C表示的化学反应速率v(C)=_______
(2)该反应在2 min时改变了某一条件,则该条件可能为_______ 。
(3)下列能说明反应达到平衡的是_______(填标号)。
(4)t时刻,此时压强与初始压强的比值为46:49,则此时A物质的转化率为_______ %,此时该反应_______ (填“是”或“否”)达到平衡。

(1)写出该反应的化学方程式
(2)该反应在2 min时改变了某一条件,则该条件可能为
(3)下列能说明反应达到平衡的是_______(填标号)。
| A.当有1mol A被消耗的同时有1mol D被消耗 |
| B.反应体系内气体的密度不再发生变化 |
| C.A与C的浓度之比为2:3 |
| D.反应体系内气体的压强不再发生变化 |
更新时间:2022-11-18 21:07:00
|
相似题推荐
填空题
|
较易
(0.85)
【推荐1】某实验小组探究H2O2分解的速率及影响因素,在相同温度下按照下表所示的方案完成实验。
(1)上述实验方案中,探究的变量因素只有催化剂的实验组合是_____ 和_____ 。
(2)实验④过程中氧气的生成速率和时间的趋势关系如图所示,判断该反应是反应(填“放热”或“吸热”)______ 。
(3)实验⑤:在试管中加入10mL 0.4mol/L H2O2溶液,加入固体催化剂,在一定温度下测得不同时刻生成O2的体积(以折算为标准状况)如下表所示(假设反应过程溶液的体积保持不变):
①反应6min,H2O2分解了_______ %。
②0至6min,以H2O2的浓度变化表示的反应速率为υ(H2O2)=________ mol▪L-1▪min-1。
实验编号 | 反应物 |
① | 10 mL 0.5 mol ▪ L-1 H2O2溶液 |
② | 10 mL 1.0 mol ▪ L-1 H2O2溶液 |
③ | 10 mL 1.0 mol ▪ L-1 H2O2溶液+1mL H2O |
④ | 10 mL 1.0 mol ▪ L-1 H2O2溶液+1 mL 0.1 mol ▪ L-1 FeCl3溶液 |
(1)上述实验方案中,探究的变量因素只有催化剂的实验组合是
(2)实验④过程中氧气的生成速率和时间的趋势关系如图所示,判断该反应是反应(填“放热”或“吸热”)

(3)实验⑤:在试管中加入10mL 0.4mol/L H2O2溶液,加入固体催化剂,在一定温度下测得不同时刻生成O2的体积(以折算为标准状况)如下表所示(假设反应过程溶液的体积保持不变):
t/min | 0 | 2 | 4 | 6 | 8 | 10 |
V(O2)/mL | 0 | 9.9 | 17.2 | 22.4 | 26.5 | 29.9 |
①反应6min,H2O2分解了
②0至6min,以H2O2的浓度变化表示的反应速率为υ(H2O2)=
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】在一体积为2L的密闭容器中A、B两种气体反应生成C、D两种气体的可逆反应3A+B xC+2D的体系中,若一开始在体系中冲入3molA和3molB气体,2min末反应达到平衡状态,生成1molD,并测得C的浓度为0.5mol/L。由此推断:
xC+2D的体系中,若一开始在体系中冲入3molA和3molB气体,2min末反应达到平衡状态,生成1molD,并测得C的浓度为0.5mol/L。由此推断:
(1)x值等于___ 。
(2)平衡时B的浓度为___ 。
(3)生成D的反应速率___ 。
(4)试计算反应前和平衡时气体压强之比为:___ 。
 xC+2D的体系中,若一开始在体系中冲入3molA和3molB气体,2min末反应达到平衡状态,生成1molD,并测得C的浓度为0.5mol/L。由此推断:
xC+2D的体系中,若一开始在体系中冲入3molA和3molB气体,2min末反应达到平衡状态,生成1molD,并测得C的浓度为0.5mol/L。由此推断:(1)x值等于
(2)平衡时B的浓度为
(3)生成D的反应速率
(4)试计算反应前和平衡时气体压强之比为:
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】反应2SO2(g)+O2(g)  2SO3(g)为工业上合成硫酸的非常重要的一步。
2SO3(g)为工业上合成硫酸的非常重要的一步。
(1)已知该反应在反应过程中体系温度会升高,下列有关说法正确的是 ___________。
(2)一定温度下,向体积为2L的刚性密闭容器中充入0.2molSO2和0.1molO2,发生反应:2SO2(g)+O2(g)  2SO3(g)。反应过程中容器内某物质的物质的量浓度随时间变化关系如图所示:
2SO3(g)。反应过程中容器内某物质的物质的量浓度随时间变化关系如图所示:
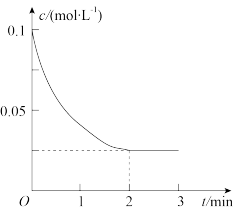
①图中曲线表示的是___________ (填“SO2”“O2”或“SO3”)的物质的量浓度随时间的变化,2min时O2的转化率为 ___________ 。
②0~2min内,用SO2表示该反应的速率为___________ mol•L-1•min-1。
 2SO3(g)为工业上合成硫酸的非常重要的一步。
2SO3(g)为工业上合成硫酸的非常重要的一步。(1)已知该反应在反应过程中体系温度会升高,下列有关说法正确的是 ___________。
| A.该反应为吸热反应 |
| B.该催化剂对任何反应均能加快反应速率 |
| C.该反应中,SO2不可能100%转化为SO3 |
| D.保持其他条件不变,升高温度可以增大生成SO3的速率 |
 2SO3(g)。反应过程中容器内某物质的物质的量浓度随时间变化关系如图所示:
2SO3(g)。反应过程中容器内某物质的物质的量浓度随时间变化关系如图所示:
①图中曲线表示的是
②0~2min内,用SO2表示该反应的速率为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】在10L密闭容器中充入4mol N2、12mol H2,控制条件发生反应:N2+3H2 2NH3,4min时测得c(NH3)=0.2mol·L-1,问:
2NH3,4min时测得c(NH3)=0.2mol·L-1,问:
(1)4min时c(N2)、c(H2)分别是多少?_________
(2)4min内该反应的反应速率有几种表示方式?它们之间的关系是怎样的?把结果填入下表中:
(3)所计算出的反应速率是否是4min时该反应的瞬时速率?为什么?_________
 2NH3,4min时测得c(NH3)=0.2mol·L-1,问:
2NH3,4min时测得c(NH3)=0.2mol·L-1,问:(1)4min时c(N2)、c(H2)分别是多少?
(2)4min内该反应的反应速率有几种表示方式?它们之间的关系是怎样的?把结果填入下表中:
| N2 | H2 | NH3 | |
| 变化浓度/mol·L-1 | |||
| 反应速率/mol·L-1·min-1 | |||
| 反应速率数值之间的关系 | |||
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】某温度时,在容积为3 L的密闭容器中,X、Y、Z三种气态物质的物质的量随时间变化的曲线如图所示。
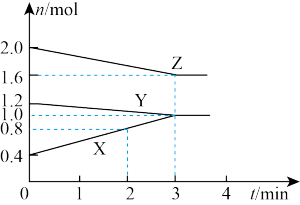
分析图中数据,回答下列问题:
(1)该反应的化学方程式为___________ 。
(2)反应开始至2 min末,X的反应速率为___________ 。

分析图中数据,回答下列问题:
(1)该反应的化学方程式为
(2)反应开始至2 min末,X的反应速率为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】能源是人类生活和社会发展的基础,研究化学反应中的能量变化,有助于更好地利用化学反应为生产和生活服务。阅读下列有关能源的材料,回答有关问题:
(1)已知断开1molH−H键、lmolN−H键、1molN≡N键分别需要吸收能量为436kJ、391kJ、945kJ,则H2与足量N2反应生成2molNH3需____ (填“吸收”或“放出”)能量____ kJ。
(2)科学家致力于二氧化碳的“组合转化”技术研究,如将CO2和H2以一定比例混合通入反应器,适当条件下可获得甲醇(CH3OH)。某温度下在1L的恒容密闭容器中,充入2molCO2和6molH2,发生如下反应:CO2(g)+3H2(g) CH3OH(g)+H2O(g)。
CH3OH(g)+H2O(g)。
①能判断该反应已达到化学反应限度标志的是____ (填字母)。
A.容器内压强保持不变
B.容器中H2浓度与CO2浓度之比为3:1
C.容器中混合气体的质量保持不变
D.CO2的生成速率与CH3OH的生成速率相等
②现测得CO2和CH3OH(g)的浓度随时间变化如图所示。从反应开始经过12min达到平衡,则这段时间氢气的平均反应速率υ(H2)=____ mol∙L−1∙min−1。

(1)已知断开1molH−H键、lmolN−H键、1molN≡N键分别需要吸收能量为436kJ、391kJ、945kJ,则H2与足量N2反应生成2molNH3需
(2)科学家致力于二氧化碳的“组合转化”技术研究,如将CO2和H2以一定比例混合通入反应器,适当条件下可获得甲醇(CH3OH)。某温度下在1L的恒容密闭容器中,充入2molCO2和6molH2,发生如下反应:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g)。
CH3OH(g)+H2O(g)。①能判断该反应已达到化学反应限度标志的是
A.容器内压强保持不变
B.容器中H2浓度与CO2浓度之比为3:1
C.容器中混合气体的质量保持不变
D.CO2的生成速率与CH3OH的生成速率相等
②现测得CO2和CH3OH(g)的浓度随时间变化如图所示。从反应开始经过12min达到平衡,则这段时间氢气的平均反应速率υ(H2)=

您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】一定温度下,在2 L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如下图所示:

(1)写出该反应的化学方程式__________ 。
(2)计算反应开始到10 s,用X表示的反应速率是__________ ,Y的转化率为______ 。
(3)下列叙述中能说明上述反应达到平衡状态的是____ 。
A.当X与Y的反应速率之比为1:1
B.在混合气体中X的质量百分数保持不变
C.混合气体的平均摩尔质量不随时间的变化而变化
D.混合气体的的密度不随时间的变化而变化
E.X、Y、Z的浓度之比为1:1:2
(4)当反应达到平衡时,用Y表示的正反应速率v(正)与用Z表示的逆反应速率v(逆)的关系是_____________ 。
(5)为使该反应的反应速率增大,可采取的措施是______ .
a.恒容时充入Ne b.适当升高温度
c.缩小容器的体积 d.选择高效催化剂

(1)写出该反应的化学方程式
(2)计算反应开始到10 s,用X表示的反应速率是
(3)下列叙述中能说明上述反应达到平衡状态的是
A.当X与Y的反应速率之比为1:1
B.在混合气体中X的质量百分数保持不变
C.混合气体的平均摩尔质量不随时间的变化而变化
D.混合气体的的密度不随时间的变化而变化
E.X、Y、Z的浓度之比为1:1:2
(4)当反应达到平衡时,用Y表示的正反应速率v(正)与用Z表示的逆反应速率v(逆)的关系是
(5)为使该反应的反应速率增大,可采取的措施是
a.恒容时充入Ne b.适当升高温度
c.缩小容器的体积 d.选择高效催化剂
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】Ⅰ.影响化学反应速率的因素有多种,请在横线上填入与下列各项关系最为密切的影响化学反应速率的因素(填“温度”、“浓度”、“催化剂”、“压强”、“物质本身的性质”或“固体表面积”):
(1)夏天的食品易变霉,在冬天不易发生该现象:_______ 。
(2)同浓度不同体积的盐酸中放入同样大小的锌块和镁块,产生气体有快有慢:_______ 。
(3)MnO2加入双氧水中放出气泡加快:__________ 。
Ⅱ.在一定温度下,4 L密闭容器内某一反应中气体M、气体N的物质的量浓度随时间变化的曲线如图所示。
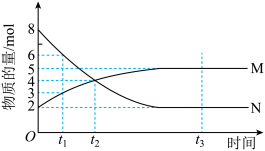
(1)比较t2时刻,正、逆反应速率大小:v(正)________ (填“>”“=”或“<”)v(逆)。
(2)若t2=2 min,反应开始至t2时刻,M的平均化学反应速率v(M)=______ mol·L-1·min-1。
(3)t1、t2、t3三个时刻中处于平衡状态的时刻为_________ (填“t1”“t2”或“t3”)。
(4)如果升高温度,则v(逆)________ (填“增大”“减小”或“不变”)。
(1)夏天的食品易变霉,在冬天不易发生该现象:
(2)同浓度不同体积的盐酸中放入同样大小的锌块和镁块,产生气体有快有慢:
(3)MnO2加入双氧水中放出气泡加快:
Ⅱ.在一定温度下,4 L密闭容器内某一反应中气体M、气体N的物质的量浓度随时间变化的曲线如图所示。

(1)比较t2时刻,正、逆反应速率大小:v(正)
(2)若t2=2 min,反应开始至t2时刻,M的平均化学反应速率v(M)=
(3)t1、t2、t3三个时刻中处于平衡状态的时刻为
(4)如果升高温度,则v(逆)
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】超音速飞机在平流层飞行时,尾气中的NO会破坏臭氧层。科学家正在研究利用催化技术将尾气中的NO和CO转变成CO2和N2,化学方程式如下:2NO+2CO 2CO2+N2.为了测定在某种催化剂作用下的反应速率,在某温度下用气体传感器测得不同时间的NO和CO浓度如下:
2CO2+N2.为了测定在某种催化剂作用下的反应速率,在某温度下用气体传感器测得不同时间的NO和CO浓度如下:
请回答下列问题(均不考虑温度变化对催化剂催化效率的影响):
(1)前2 s内的平均反应速率v(N2)=___________ 。
(2)达到平衡时NO的转化率为___________ 。
(3)若上述反应在密闭恒容容器中进行,判断该反应达到平衡的依据为___________(填字母)。
 2CO2+N2.为了测定在某种催化剂作用下的反应速率,在某温度下用气体传感器测得不同时间的NO和CO浓度如下:
2CO2+N2.为了测定在某种催化剂作用下的反应速率,在某温度下用气体传感器测得不同时间的NO和CO浓度如下:| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
| c(NO)/mol·L−1 | 1.00×10−3 | 4.50×10−4 | 2.50×10−4 | 1.50×10−4 | 1.00×10−4 | 1.00×10−4 |
| c(CO)/mol·L−1 | 3.60×10−3 | 3.05×10−3 | 2.85×10−3 | 2.75×10−3 | 2.70×10−3 | 2.70×10−3 |
(1)前2 s内的平均反应速率v(N2)=
(2)达到平衡时NO的转化率为
(3)若上述反应在密闭恒容容器中进行,判断该反应达到平衡的依据为___________(填字母)。
| A.c(N2)不随时间改变 | B.气体的密度不随时间改变 |
| C.压强不随时间改变 | D.单位时间内消耗2 mol NO的同时生成1 mol N2 |
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】一定温度下,在2 L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如下图所示:

回答下列问题:
[提示:物质的转化率(%)= ×100%]
×100%]
(1)反应开始到10 s时,用Z表示的反应速率为______ ;
(2)反应开始到10 s时,Y的转化率为______ ;
(3)反应的化学方程式为:______ 。

回答下列问题:
[提示:物质的转化率(%)=
 ×100%]
×100%](1)反应开始到10 s时,用Z表示的反应速率为
(2)反应开始到10 s时,Y的转化率为
(3)反应的化学方程式为:
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】Ⅰ.反应N2(g)+3H2(g) 2NH3(g) ΔH<0在等容条件下进行。改变其他反应条件,在Ⅰ、Ⅱ、Ⅲ阶段体系中各物质浓度随时间变化的曲线如下图所示:
2NH3(g) ΔH<0在等容条件下进行。改变其他反应条件,在Ⅰ、Ⅱ、Ⅲ阶段体系中各物质浓度随时间变化的曲线如下图所示:

回答问题:
(1)H2的平衡转化率αⅠ(H2)、αⅡ(H2)、αⅢ(H2)的大小关系是_________________________ 。
(2)由第一次平衡到第二次平衡,采取的措施是______________________ 。
Ⅱ.在一定温度下,向一容积为5L的恒容密闭容器中充入0.4mol SO2和0.2mol O2,发生反应: 2SO2(g)+O2(g) 2SO3(g) ΔH=-196kJ/mol。经2min后达到平衡,当反应达到平衡时,容器内压强变为起始时的0.7倍。请回答下列问题:
2SO3(g) ΔH=-196kJ/mol。经2min后达到平衡,当反应达到平衡时,容器内压强变为起始时的0.7倍。请回答下列问题:
(3)上述反应达到平衡时反应放出的热量为__________ 。
(4)如图表示平衡时SO2的体积分数随压强和温度变化的曲线。则温度关系:T1_____ T2(填“>”“<”或“=”)。

Ⅲ.一定温度下,在1L恒容密闭容器中充入一定量C2H4(g)和H2O(g),发生如下反应: C2H4(g)+H2O(g) CH3CH2OH(g) ΔH,测得C2H4(g)的转化率(α)与时间(t)的关系如图所示。其中T1、T2表示温度,速率方程:v正=k正·c(C2H4)·c(H2O),v逆=k逆·c(CH3CH2OH)(k是速率常数,只与温度有关)。
CH3CH2OH(g) ΔH,测得C2H4(g)的转化率(α)与时间(t)的关系如图所示。其中T1、T2表示温度,速率方程:v正=k正·c(C2H4)·c(H2O),v逆=k逆·c(CH3CH2OH)(k是速率常数,只与温度有关)。

(5)N点: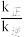
______  (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
(6)温度为T1时,测定平衡体系中c(H2O)=0.25 mol·L-1,则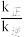 =
=______ L·mol -1。
 2NH3(g) ΔH<0在等容条件下进行。改变其他反应条件,在Ⅰ、Ⅱ、Ⅲ阶段体系中各物质浓度随时间变化的曲线如下图所示:
2NH3(g) ΔH<0在等容条件下进行。改变其他反应条件,在Ⅰ、Ⅱ、Ⅲ阶段体系中各物质浓度随时间变化的曲线如下图所示:
回答问题:
(1)H2的平衡转化率αⅠ(H2)、αⅡ(H2)、αⅢ(H2)的大小关系是
(2)由第一次平衡到第二次平衡,采取的措施是
Ⅱ.在一定温度下,向一容积为5L的恒容密闭容器中充入0.4mol SO2和0.2mol O2,发生反应: 2SO2(g)+O2(g)
 2SO3(g) ΔH=-196kJ/mol。经2min后达到平衡,当反应达到平衡时,容器内压强变为起始时的0.7倍。请回答下列问题:
2SO3(g) ΔH=-196kJ/mol。经2min后达到平衡,当反应达到平衡时,容器内压强变为起始时的0.7倍。请回答下列问题:(3)上述反应达到平衡时反应放出的热量为
(4)如图表示平衡时SO2的体积分数随压强和温度变化的曲线。则温度关系:T1

Ⅲ.一定温度下,在1L恒容密闭容器中充入一定量C2H4(g)和H2O(g),发生如下反应: C2H4(g)+H2O(g)
 CH3CH2OH(g) ΔH,测得C2H4(g)的转化率(α)与时间(t)的关系如图所示。其中T1、T2表示温度,速率方程:v正=k正·c(C2H4)·c(H2O),v逆=k逆·c(CH3CH2OH)(k是速率常数,只与温度有关)。
CH3CH2OH(g) ΔH,测得C2H4(g)的转化率(α)与时间(t)的关系如图所示。其中T1、T2表示温度,速率方程:v正=k正·c(C2H4)·c(H2O),v逆=k逆·c(CH3CH2OH)(k是速率常数,只与温度有关)。
(5)N点:
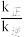
 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。(6)温度为T1时,测定平衡体系中c(H2O)=0.25 mol·L-1,则
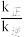 =
=
您最近一年使用:0次




