下图所示的是一些常见的单质、化合物之间的转化关系图,有些反应中的部分物质和反应条件被略去。常温常压下,化合物A是家庭生活中常用的一种调味品,A、C的焰色反应都呈黄色,B是无色无味的液体,D是黄绿色气体,E、F都是无色气体,F的水溶液是盐酸,H的水溶液具有漂白、杀菌性,J在水溶液中生成时为红褐色沉淀。
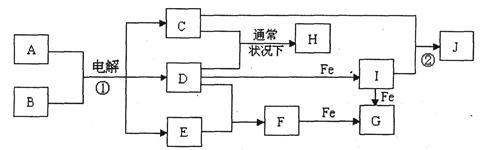
(1)H的化学式为___________________ 。
(2)F的电子式为___________________ 。
(3)反应①的化学方程式为____________________________________________ 。
(4)反应②的离子方程式为____________________________________________ 。

(1)H的化学式为
(2)F的电子式为
(3)反应①的化学方程式为
(4)反应②的离子方程式为
13-14高二上·江苏徐州·期末 查看更多[3]
2014-2015江苏省射阳县二中高二上学期期中化学(必修)试卷(已下线)2013-2014学年江苏省徐州市高二上学期期末考试化学试卷(必修)(已下线)2012-2013学年江苏省徐州市高二上学期期末考试化学试卷
更新时间:2016-12-08 21:14:16
|
相似题推荐
填空题
|
较难
(0.4)
【推荐1】饮用水中含有一定浓度的NO3一将对人类健康产生危害,NO3一能氧化人体血红蛋白中的Fe(II),使其失去携氧功能。为了降低饮用水中NO3一的浓度,某兴趣小组提出如下方案:

请回答下列问题:
⑴已知过滤后得到的滤渣是一种混合物,则在溶液中铝粉和NO3一反应的离子方程式为
__________________________________________ 。
⑵该方案中选用熟石灰调节pH,理由是_______________________ 、__________________ ,在调节pH时,若pH过大或过小都会造成____ 的利用率降低。
⑶用H2催化还原法也可降低饮用水中NO3-的浓度,已知反应中的还原产物和氧化产物均可参与大气循环,则催化还原法的离子方程式为____________________________________ 。
⑷饮用水中的NO3- 主要来自于NH4+。已知在微生物作用的条件下,NH4+ 经过两步反应被氧化成NO3- 。两步反应的能量变化示意图如下:

试写出1 mol NH4+ (aq)全部氧化成NO3- (aq)的热化学方程式是________________________ 。

请回答下列问题:
⑴已知过滤后得到的滤渣是一种混合物,则在溶液中铝粉和NO3一反应的离子方程式为
⑵该方案中选用熟石灰调节pH,理由是
⑶用H2催化还原法也可降低饮用水中NO3-的浓度,已知反应中的还原产物和氧化产物均可参与大气循环,则催化还原法的离子方程式为
⑷饮用水中的NO3- 主要来自于NH4+。已知在微生物作用的条件下,NH4+ 经过两步反应被氧化成NO3- 。两步反应的能量变化示意图如下:

试写出1 mol NH4+ (aq)全部氧化成NO3- (aq)的热化学方程式是
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐2】X、Y为短周期主族元素,X的主族序数是周期序数的两倍,Y的原子序数比X大l.
I.若X.Y是组成蛋白质的基础元素。
(1)X和Y的气态氢化物中热稳定性较强的是________ (填写化学式)。
(2)蛋白质和葡萄糖都是人体需要的有机物,检测葡萄糖存在的实验操作与现象是______ 。
(3)已知298K时,X和XO的标准燃烧热分别为 该温度下X转化为XO的热化学方程式为
该温度下X转化为XO的热化学方程式为_______________ 。
Ⅱ.若火山口附近常存在黄色的X单质。
(4)X2—的结构示意图为________ 。
(5)工业上常用含X元素的矿石制取H2XO4,某工厂利用100吨含X 40%的矿石为原料,制得98%H2XO4溶液100吨,则H2XO4的产率为__________ 。
(6)工业中常用Y2与石灰浆反应制取漂白粉,该反应的化学方程式为___________ 。
I.若X.Y是组成蛋白质的基础元素。
(1)X和Y的气态氢化物中热稳定性较强的是
(2)蛋白质和葡萄糖都是人体需要的有机物,检测葡萄糖存在的实验操作与现象是
(3)已知298K时,X和XO的标准燃烧热分别为
 该温度下X转化为XO的热化学方程式为
该温度下X转化为XO的热化学方程式为Ⅱ.若火山口附近常存在黄色的X单质。
(4)X2—的结构示意图为
(5)工业上常用含X元素的矿石制取H2XO4,某工厂利用100吨含X 40%的矿石为原料,制得98%H2XO4溶液100吨,则H2XO4的产率为
(6)工业中常用Y2与石灰浆反应制取漂白粉,该反应的化学方程式为
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐3】氢气还原氧化铜反应不完全时,得到的是Cu、Cu2O、CuO的固体混合物。某化学兴趣小组为了探究某次氢气还原CuO实验最终所得的产物的组成,进行了如下实验:
①取一定质量的均匀的上述固体混合物A,将其分成两等份。
②取其中一份用足量的氢气还原,测得反应后固体的质量减小了3.20g
③另一份加入500mL的稀硝酸,固体恰好完全溶解,且同时收集到标准状况下NO气体2.24L。
请回答以下问题:
(1)A中,所含氧元素的物质的量为_________ 。
(2)A中,n(Cu)+n(Cu2O)=_______________ 。
(3)所用稀硝酸的物质的量浓度为_______________ 。
①取一定质量的均匀的上述固体混合物A,将其分成两等份。
②取其中一份用足量的氢气还原,测得反应后固体的质量减小了3.20g
③另一份加入500mL的稀硝酸,固体恰好完全溶解,且同时收集到标准状况下NO气体2.24L。
请回答以下问题:
(1)A中,所含氧元素的物质的量为
(2)A中,n(Cu)+n(Cu2O)=
(3)所用稀硝酸的物质的量浓度为
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐1】有关物质存在如图所示的转化关系(部分产物已省略)。通常C为气体单质,G为紫黑色固体单质,且受热易升华。实验室中,常用固体E在B的催化下加热制取气体单质H,H能使带火星的木条复燃。

请回答下列问题:
(1)反应①的化学方程式为_______ 。
(2)反应②的离子方程式为_______ 。
(3)写出另外一种实验室制取H的化学方程式_______ 。
(4)已知D溶液与Pb(NO3)2溶液混合可形成沉淀,此沉淀的Ksp=7.0×10-9。若D的浓度为1.0×10-2mol/L,将等体积的D溶液与Pb(NO3)2溶液混合,则生成沉淀所需Pb(NO3)2溶液的最小浓度为_______ mol/L。

请回答下列问题:
(1)反应①的化学方程式为
(2)反应②的离子方程式为
(3)写出另外一种实验室制取H的化学方程式
(4)已知D溶液与Pb(NO3)2溶液混合可形成沉淀,此沉淀的Ksp=7.0×10-9。若D的浓度为1.0×10-2mol/L,将等体积的D溶液与Pb(NO3)2溶液混合,则生成沉淀所需Pb(NO3)2溶液的最小浓度为
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐2】I、在下列物质转化中A是一种正盐,D的相对分子质量比C的相对分子质量大16,E是酸,当X无论是强酸还是强碱时,都有如下的转化关系:





当X是强酸时,A、B、C、D、E均含同一种元素;当X是强碱时,A、B、C、D、E均含另外的同一种元素。请回答:
(1)A的化学式是______ , Z的电子式是______ 。
(2)当X是强酸时,写出C→D的化学方程式:_____ 。
(3)当X是强碱时,写出E的稀溶液和铜反应生成C的离子方程式:_____ 。
II、在FeSO4溶液中加入(NH4)2SO4固体可制备摩尔盐晶体[(NH4)2SO4·FeSO4·6H2O] (其相对分子质量为392),该晶体比一般亚铁盐稳定,不易被氧化,易溶于水,不溶于乙醇。
(4)为了洗涤(NH4)2SO4·FeSO4·6H2O粗产品,下列方法中最合适的是____ (填字母代号)。
A.用冷水洗 B.先用冷水洗,后用无水乙醇洗
C.用30%的乙醇溶液洗 D.用90%的乙醇溶液洗
(5)为了测定产品的纯度,称取a g产品溶于水,配制成500mL溶液,用浓度为c mol·L-1的酸性KMnO4溶液滴定。每次所取待测液体积均为25.00mL,实验结果记录如下:
①上表中第一次实验中记录数据明显大于后两次,其原因可能是_____ (填字母代号)。
A.滴定前滴定管尖嘴无气泡,滴定结束有气泡
B.第一次滴定用的锥形瓶用待装液润洗过,后两次未润洗
C.该酸性高锰酸钾标准液保存时间过长,有部分变质,浓度降低
D.实验结束时俯视刻度线读取滴定终点时酸性高锰酸钾溶液的体积
②通过实验数据计算的该产品纯度为_____ (用字母a、c表示)。





当X是强酸时,A、B、C、D、E均含同一种元素;当X是强碱时,A、B、C、D、E均含另外的同一种元素。请回答:
(1)A的化学式是
(2)当X是强酸时,写出C→D的化学方程式:
(3)当X是强碱时,写出E的稀溶液和铜反应生成C的离子方程式:
II、在FeSO4溶液中加入(NH4)2SO4固体可制备摩尔盐晶体[(NH4)2SO4·FeSO4·6H2O] (其相对分子质量为392),该晶体比一般亚铁盐稳定,不易被氧化,易溶于水,不溶于乙醇。
(4)为了洗涤(NH4)2SO4·FeSO4·6H2O粗产品,下列方法中最合适的是
A.用冷水洗 B.先用冷水洗,后用无水乙醇洗
C.用30%的乙醇溶液洗 D.用90%的乙醇溶液洗
(5)为了测定产品的纯度,称取a g产品溶于水,配制成500mL溶液,用浓度为c mol·L-1的酸性KMnO4溶液滴定。每次所取待测液体积均为25.00mL,实验结果记录如下:
| 实验次数 | 第一次 | 第二次 | 第三次 |
| 消耗高锰酸钾溶液体积/mL | 25.52 | 25.02 | 24.98 |
①上表中第一次实验中记录数据明显大于后两次,其原因可能是
A.滴定前滴定管尖嘴无气泡,滴定结束有气泡
B.第一次滴定用的锥形瓶用待装液润洗过,后两次未润洗
C.该酸性高锰酸钾标准液保存时间过长,有部分变质,浓度降低
D.实验结束时俯视刻度线读取滴定终点时酸性高锰酸钾溶液的体积
②通过实验数据计算的该产品纯度为
您最近一年使用:0次



