乙烯是重要的有机化工原料,其产量是衡量国家石油化工水平发展的标志。以乙烯和淀粉为原料可以实现下列转化:
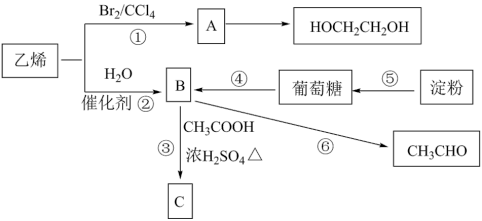
(1)乙烯的电子式________________ 。
(2)反应①的反应类型为_____________________ 。
(3)写出反应③的化学方程式:_____________________ 。
(4)写出反应④的化学方程式:_______________________________ 。
(5)上述物质中,能发生银镜反应的物质有__________________________ (写名称)。
(6)丙烯( )与乙烯具有相似的化学性质。
)与乙烯具有相似的化学性质。
①聚丙烯的结构简式为________________________ 。
②在一定条件下丙烯与H2O的加成产物可能为__________________________________ 。

(1)乙烯的电子式
(2)反应①的反应类型为
(3)写出反应③的化学方程式:
(4)写出反应④的化学方程式:
(5)上述物质中,能发生银镜反应的物质有
(6)丙烯(
 )与乙烯具有相似的化学性质。
)与乙烯具有相似的化学性质。①聚丙烯的结构简式为
②在一定条件下丙烯与H2O的加成产物可能为
更新时间:2023-05-18 21:56:43
|
相似题推荐
解答题-有机推断题
|
适中
(0.65)
【推荐1】A是一种常见的有机物,其产量可以作为衡量一个国家石油化工发展水平的标志,F是高分子化合物,有机物A可以实现如下转换关系。请回答下列问题:
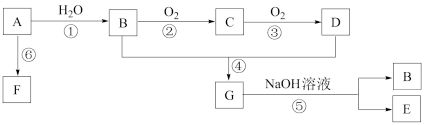
(1)A的结构式为_______ 。
(2)D中含氧原子团的名称为_______ ,④的化学反应类型为_______ 。
(3)请分别写出⑤、⑥的化学方程式_______ 、_______ 。
(4)在实验室中,可用下图所示装置制取少量G,①图中试剂a名称为_______ ,其作用是_______ 。用化学方程式表示试剂a参与的化学反应: _______ 。


(1)A的结构式为
(2)D中含氧原子团的名称为
(3)请分别写出⑤、⑥的化学方程式
(4)在实验室中,可用下图所示装置制取少量G,①图中试剂a名称为

您最近一年使用:0次
解答题-有机推断题
|
适中
(0.65)
【推荐2】已知:A是一种重要的化工原料,它的产量通常用来衡量一个国家石油化工水平。现以A为主要原料合成乙酸乙酯及高分子化合物E,其合成路线如下图所示:
请回答下列问题:
(1)B分子中的官能团名称是________ 。
(2)反应④的反应类型属于________ 。
(3)下列说法正确的是________ ;
A.高分子化合物E是一种常见的塑料,生活中可用于制造水杯、奶瓶、食物保鲜膜等用品
B.用新制碱性氢氧化铜悬浊液无法区分有机物B、C和D
C.通过直接蒸馏乙酸乙酯和有机物D的混合物,可分离得到纯的乙酸乙酯
D.相同条件下乙酸乙酯在氢氧化钠溶液中水解较在稀硫酸中更完全

请回答下列问题:
(1)B分子中的官能团名称是
(2)反应④的反应类型属于
(3)下列说法正确的是
A.高分子化合物E是一种常见的塑料,生活中可用于制造水杯、奶瓶、食物保鲜膜等用品
B.用新制碱性氢氧化铜悬浊液无法区分有机物B、C和D
C.通过直接蒸馏乙酸乙酯和有机物D的混合物,可分离得到纯的乙酸乙酯
D.相同条件下乙酸乙酯在氢氧化钠溶液中水解较在稀硫酸中更完全
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】已知 是化学实验室中最常见的有机物,它易溶于水并有特殊香味;
是化学实验室中最常见的有机物,它易溶于水并有特殊香味; 的产量可以衡量一个国家石油化工发展的水平,有关物质的转化关系如图所示(部分反应条件、产物省略):
的产量可以衡量一个国家石油化工发展的水平,有关物质的转化关系如图所示(部分反应条件、产物省略):
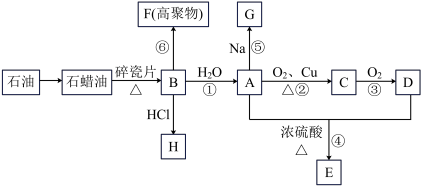
回答下列问题:
(1)从石油中获得石蜡油的方法称为石油的_______ 。
(2)①决定化合物D的化学特性的官能团名称为_______ ;②B到A的反应类型为_______ 。
(3)写出下列反应的化学方程式。
反应②:_______ 。
反应⑥:_______ 。
(4)下列说法正确的是_______(填字母)。
(5)水果成熟后会产生各种具有香味的物质,主要是酯类化合物,乙酸乙酯是其中较常见的一种,实验室制取乙酸乙酯时试剂的添加顺序为_______ 。
 是化学实验室中最常见的有机物,它易溶于水并有特殊香味;
是化学实验室中最常见的有机物,它易溶于水并有特殊香味; 的产量可以衡量一个国家石油化工发展的水平,有关物质的转化关系如图所示(部分反应条件、产物省略):
的产量可以衡量一个国家石油化工发展的水平,有关物质的转化关系如图所示(部分反应条件、产物省略):
回答下列问题:
(1)从石油中获得石蜡油的方法称为石油的
(2)①决定化合物D的化学特性的官能团名称为
(3)写出下列反应的化学方程式。
反应②:
反应⑥:
(4)下列说法正确的是_______(填字母)。
| A.B可使酸性高锰酸钾溶液褪色是发生了加成反应 |
B. 与 与 充分反应能生成 充分反应能生成 |
| C.F可用于制造食品包装袋 |
| D.塑料、合成纤维、合成橡胶等都是合成有机高分子材料 |
您最近一年使用:0次
【推荐1】已知A、B、C、D是中学化学常见物质,它们在一定条件下有A+B→C+D的转化关系。
(1)若A为金属铝,B为氧化铁,该反应的一种用途是_______________ 。
(2)若A是一种能使湿润的红色石蕊试纸变蓝的气体,且该反应是工业上制取硝酸的重要反应之一,该反应的化学反应方程式为____________________________ 。
(3)若A是淡黄色粉末,常用作供氧剂,C为强碱,则该反应的化学反应方程式为_______ 。
(4)若A、B、D都是有机化合物,其中A、B是家庭厨房中常见调味品的主要成分,且A 的相对分子质量比B大14。
①该反应的化学反应方程式为_____________________ 。
②某种以B为反应物的新型电池如图所示,该电池的负极的电极反应式为_________ 。
(5)ClO2可将弱酸性废水中的Mn2+转化为MnO2而除去,同时ClO2被还原为Cl-,该反应的离子方程式为________________________________ 。
(1)若A为金属铝,B为氧化铁,该反应的一种用途是
(2)若A是一种能使湿润的红色石蕊试纸变蓝的气体,且该反应是工业上制取硝酸的重要反应之一,该反应的化学反应方程式为
(3)若A是淡黄色粉末,常用作供氧剂,C为强碱,则该反应的化学反应方程式为
(4)若A、B、D都是有机化合物,其中A、B是家庭厨房中常见调味品的主要成分,且A 的相对分子质量比B大14。
①该反应的化学反应方程式为
②某种以B为反应物的新型电池如图所示,该电池的负极的电极反应式为
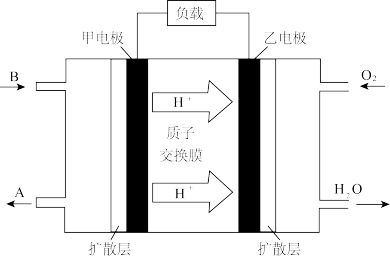
(5)ClO2可将弱酸性废水中的Mn2+转化为MnO2而除去,同时ClO2被还原为Cl-,该反应的离子方程式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】“酒是陈的香”,就是因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室我们也可以用如图所示的装置制取乙酸乙酯。回答下列问题:
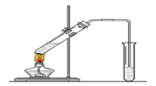
(1)写出制取乙酸乙酯的化学反应方程式:_____________
(2)在大试管中配制一定比例的乙醇、乙酸和浓硫酸的混合液的顺序是:________________ 。
(3)浓硫酸的作用是:①_________ ;②________ 。
(4)饱和碳酸钠溶液的主要作用是________ 、____ 、______ 。
(5)装置中通蒸气的导管要插在饱和碳酸钠溶液的液面上,不能插入溶液中,目的是___________ 。
(6)若要把制得的乙酸乙酯分离出来,应采用的实验操作是__________ 。
(7)做此实验时,有时还向盛乙酸和乙醇的试管里加入几块碎瓷片,其目的是_________ 。
(8)生成乙酸乙酯的反应是可逆反应,反应物不能完全变成生成物,反应一段时间后,就达到了该反应的限度,也即达到化学平衡状态。下列描述能说明乙醇与乙酸的酯化反应已达到化学平衡状态的有(填序号)________ 。
①单位时间里,生成1mol乙酸乙酯,同时生成1mol水
②单位时间里,生成1mol乙酸乙酯,同时生成1mol乙酸
③单位时间里,消耗1mol乙醇,同时消耗1mol乙酸
④正反应的速率与逆反应的速率相等
⑤混合物中各物质的浓度不再变化

(1)写出制取乙酸乙酯的化学反应方程式:
(2)在大试管中配制一定比例的乙醇、乙酸和浓硫酸的混合液的顺序是:
(3)浓硫酸的作用是:①
(4)饱和碳酸钠溶液的主要作用是
(5)装置中通蒸气的导管要插在饱和碳酸钠溶液的液面上,不能插入溶液中,目的是
(6)若要把制得的乙酸乙酯分离出来,应采用的实验操作是
(7)做此实验时,有时还向盛乙酸和乙醇的试管里加入几块碎瓷片,其目的是
(8)生成乙酸乙酯的反应是可逆反应,反应物不能完全变成生成物,反应一段时间后,就达到了该反应的限度,也即达到化学平衡状态。下列描述能说明乙醇与乙酸的酯化反应已达到化学平衡状态的有(填序号)
①单位时间里,生成1mol乙酸乙酯,同时生成1mol水
②单位时间里,生成1mol乙酸乙酯,同时生成1mol乙酸
③单位时间里,消耗1mol乙醇,同时消耗1mol乙酸
④正反应的速率与逆反应的速率相等
⑤混合物中各物质的浓度不再变化
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】乙酸乙酯是重要的有机合成中间体,广泛应用于化学工业。实验室利用如图的装置制备乙酸乙酯。

A.与教材采用的实验装置不同,此装置中采用了球形干燥管,其作用是:____________
B.按正确操作实验,该学生很快在小试管中收集到了乙酸乙酯、乙酸、乙醇的混合物。现拟分离 含乙酸、乙醇和水的乙酸乙酯粗产品,下图是分离操作步骤流程图。在图中圆括号表示加入适当的试剂,编号表示适当的分离方法。

(1)写出加入的试剂(a)是________________ ;试剂(b)是_______________ 。
(2)写出有关的操作分离方法:
①是____________ ,②是______________ ,③是_________________ 。
(3)在得到的A中加入生石灰,振荡,目的是_________________________ 。

A.与教材采用的实验装置不同,此装置中采用了球形干燥管,其作用是:
B.按正确操作实验,该学生很快在小试管中收集到了乙酸乙酯、乙酸、乙醇的混合物。现拟

(1)写出加入的试剂(a)是
(2)写出有关的操作分离方法:
①是
(3)在得到的A中加入生石灰,振荡,目的是
您最近一年使用:0次
解答题-有机推断题
|
适中
(0.65)
解题方法
【推荐1】以淀粉为主要原料可以制得多种有机物,其合成路线如图所示:
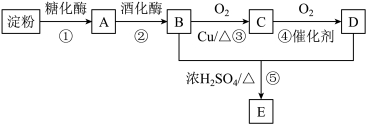
已知:A属于单糖,D能跟NaHCO3溶液反应产生CO2。
回答下列问题:
(1)A的分子式为_______ ,其中官能团的名称为_______ ;C的结构简式为_______ 。
(2)⑤的反应类型为_______ 。
(3)简述实验室中检验物质A的实验试剂、操作和现象_______ 。
(4)写出反应③的化学方程式:_______ 。
(5)与E具有相同官能团且互为同分异构体的有机物有3种,其中一种为HCOOCH2CH2CH3,另外两种物质的结构简式为_______ 。

已知:A属于单糖,D能跟NaHCO3溶液反应产生CO2。
回答下列问题:
(1)A的分子式为
(2)⑤的反应类型为
(3)简述实验室中检验物质A的实验试剂、操作和现象
(4)写出反应③的化学方程式:
(5)与E具有相同官能团且互为同分异构体的有机物有3种,其中一种为HCOOCH2CH2CH3,另外两种物质的结构简式为
您最近一年使用:0次
解答题-有机推断题
|
适中
(0.65)
解题方法
【推荐2】下列物质间有如下转化关系,请按要求填空。
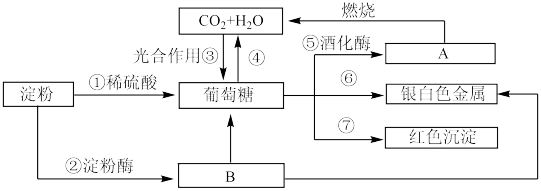
(1)在制镜工业和热水瓶胆镀银时,常利用上述反应________ (填序号)。
(2)反应①②的反应类型为_______ (填选项字母)。
A.氧化反应 B.加成反应 C.水解反应 D.消去反应
(3)反应⑦可用于检验糖尿病病人尿液中的含糖量,该反应的化学方程式为_________ 。

(1)在制镜工业和热水瓶胆镀银时,常利用上述反应
(2)反应①②的反应类型为
A.氧化反应 B.加成反应 C.水解反应 D.消去反应
(3)反应⑦可用于检验糖尿病病人尿液中的含糖量,该反应的化学方程式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】葡萄糖酸钙是一种常用的药物,临床上用于治疗骨质疏松症。某实验室对葡萄糖酸钙的制备工艺进行研究,先以葡萄糖[CH2OH(CHOH)4CHO]和H2O2为原料制备葡萄糖酸[CH2OH(CHOH)4COOH],再用葡萄糖酸与碳酸钙反应制备葡萄糖酸钙。已知:30%H2O2溶液的密度为1.1g·cm-3,回答下列问题:
I.制备葡萄糖酸(装置如图所示)。
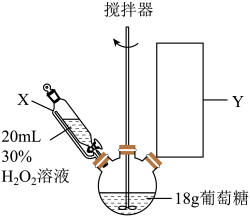
(1)仪器X的名称为___________ ,Y处为冷凝回流装置,下列仪器使用正确且效果最好的是___________ (填字母)。
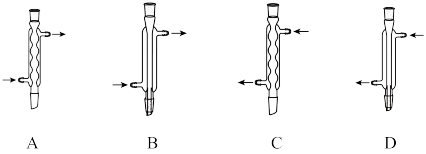
(2)滴入双氧水,水浴加热一段时间后,得到无色透明的葡萄糖酸溶液。反应的化学方程式为___________ 。
Ⅱ.测定葡萄糖的转化率,确定合适的反应温度。
(3)用移液管取出三口烧瓶中的反应液2.00mL置于锥形瓶中,以酚酞作为指示剂并加20mL蒸馏水稀释,用0.04mol·L-1NaOH标准溶液滴定。
①滴定管使用的正确的操作顺序为蒸馏水洗涤→标准液润洗→___________ →___________ →___________ →___________ →洗净→放回滴定管架(填字母)。
a.滴定结束后,记录刻度
b.调节液面至0刻度或0刻度略靠下,记录刻度
c.装入标准液并排净尖嘴处的气泡
d.将未滴定完的标准液回收
②达到滴定终点时的现象为___________ 。
③滴定过程消耗NaOH标准溶液的体积为V0mL,反应后三口烧瓶内溶液的体积为V1mL,实验条件下葡萄糖的转化率为___________ (用含V0和V1的代数式表示)。
④若滴定终点时俯视读数,对转化率的影响为___________ (填“偏高”“偏低”或“无影响”)。
Ⅲ.制备葡萄糖酸钙。
将CaCO3分散于适量蒸馏水中形成浊液,加入葡萄糖酸,至无CO2气体放出为止,煮沸,并趁热采用下图装置抽滤,滤掉未反应的CaCO3,得到澄清透明的葡萄糖酸钙溶液。
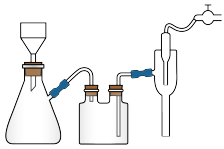
(4)抽滤时自来水流的作用是使瓶内与大气形成压强差,与普通过滤操作相比,抽滤的优点是___________ 。
I.制备葡萄糖酸(装置如图所示)。

(1)仪器X的名称为

(2)滴入双氧水,水浴加热一段时间后,得到无色透明的葡萄糖酸溶液。反应的化学方程式为
Ⅱ.测定葡萄糖的转化率,确定合适的反应温度。
(3)用移液管取出三口烧瓶中的反应液2.00mL置于锥形瓶中,以酚酞作为指示剂并加20mL蒸馏水稀释,用0.04mol·L-1NaOH标准溶液滴定。
①滴定管使用的正确的操作顺序为蒸馏水洗涤→标准液润洗→
a.滴定结束后,记录刻度
b.调节液面至0刻度或0刻度略靠下,记录刻度
c.装入标准液并排净尖嘴处的气泡
d.将未滴定完的标准液回收
②达到滴定终点时的现象为
③滴定过程消耗NaOH标准溶液的体积为V0mL,反应后三口烧瓶内溶液的体积为V1mL,实验条件下葡萄糖的转化率为
④若滴定终点时俯视读数,对转化率的影响为
Ⅲ.制备葡萄糖酸钙。
将CaCO3分散于适量蒸馏水中形成浊液,加入葡萄糖酸,至无CO2气体放出为止,煮沸,并趁热采用下图装置抽滤,滤掉未反应的CaCO3,得到澄清透明的葡萄糖酸钙溶液。

(4)抽滤时自来水流的作用是使瓶内与大气形成压强差,与普通过滤操作相比,抽滤的优点是
您最近一年使用:0次
解答题-有机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】环己烯常用于有机合成。现通过下列流程,以环己烯为原料合成环醚、聚酯、橡胶,其中F可以做内燃机的抗冻剂,J分子中无饱和碳原子,请根据一下流程图中的信息完成(1)-(7)小题

已知:
(1)F的名称是______ ,C中含有的官能团的名称是______ 。
(2)③的反应条件是______ :
(3)写出下列反应类型:⑥______ ,⑨______ 。
(4)写出②反应化学方程式:______ 。
(5)写出⑩反应化学方程式:______ 。
(6)试写出C与新制银氨溶液反应的化学方程式:______ 。
(7)D的一种同分异构体,可发生加成聚合反应,且能和NaHCO3反应,有三种氢原子,核磁共振氢谱面积比为1∶2∶3,试写出结构简式:______ 。

已知:

(1)F的名称是
(2)③的反应条件是
(3)写出下列反应类型:⑥
(4)写出②反应化学方程式:
(5)写出⑩反应化学方程式:
(6)试写出C与新制银氨溶液反应的化学方程式:
(7)D的一种同分异构体,可发生加成聚合反应,且能和NaHCO3反应,有三种氢原子,核磁共振氢谱面积比为1∶2∶3,试写出结构简式:
您最近一年使用:0次
解答题-有机推断题
|
适中
(0.65)
名校
【推荐2】由间苯甲酰基甲苯合成消炎镇痛药F(酮基布洛芬)的路线如图:
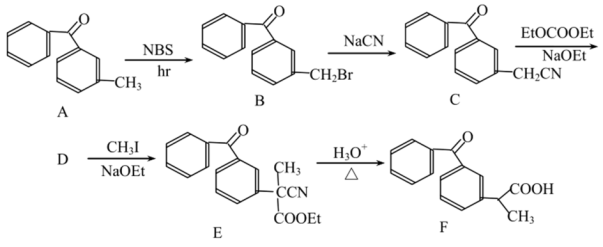
已知:乙醇钠的化学式为NaOEt。
(1)A分子中碳原子的杂化轨道类型为_______ 。
(2)B→C的反应类型为_______ 。
(3)D的分子式为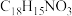 ,其结构简式为
,其结构简式为_______ 。
(4)F的一种同分异构体含有苯环且分子中含有3种不同化学环境的氢原子,写出该同分异构体的结构简式:_______ 。
(5)已知: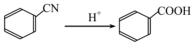 ,写出以
,写出以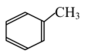 为原料制备的合成
为原料制备的合成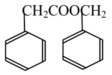 路线流程图(无机试剂和有机溶剂任用,合成路线流程图示例见本题题干)
路线流程图(无机试剂和有机溶剂任用,合成路线流程图示例见本题题干)____ 。

已知:乙醇钠的化学式为NaOEt。
(1)A分子中碳原子的杂化轨道类型为
(2)B→C的反应类型为
(3)D的分子式为
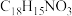 ,其结构简式为
,其结构简式为(4)F的一种同分异构体含有苯环且分子中含有3种不同化学环境的氢原子,写出该同分异构体的结构简式:
(5)已知:
 ,写出以
,写出以 为原料制备的合成
为原料制备的合成 路线流程图(无机试剂和有机溶剂任用,合成路线流程图示例见本题题干)
路线流程图(无机试剂和有机溶剂任用,合成路线流程图示例见本题题干)
您最近一年使用:0次
解答题-有机推断题
|
适中
(0.65)
解题方法
【推荐3】丙烯酰胺(H2C=CH—CONH2)具有中等毒性,它对人体可造成神经毒性和遗传毒性。丙烯酰胺主要是由高碳水化合物、低蛋白质的植物性食物在加热(120℃以上)烹调过程中形成,特别在烘烤、油炸时更易形成。丙烯酰胺可以进一步形成在工业上有用的聚丙烯酰胺类物质。

回答下列问题:
(1)D的结构简式为___ ,F的结构简式为___ 。
(2)指明下列反应类型:A→B___ ,C→D___ 。
(3)丙烯酰胺有多种同分异构体,写出分子中同时含有醛基和碳碳双键的同分异构体:___ 。
(4)写出D→E的化学方程式:__ 。2分子C在浓硫酸作用下可形成一个六元酯环,该反应的化学方程式为___ 。

回答下列问题:
(1)D的结构简式为
(2)指明下列反应类型:A→B
(3)丙烯酰胺有多种同分异构体,写出分子中同时含有醛基和碳碳双键的同分异构体:
(4)写出D→E的化学方程式:
您最近一年使用:0次



