含氮、磷、砷化合物的转化和处理是环境保护的重要课题。
(1)研究团队采用NaClO氧化法去除水中氨氮( 、
、 )。已知:HClO的氧化性比NaClO强;
)。已知:HClO的氧化性比NaClO强; 比
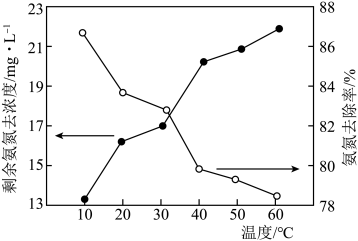
比 更容易被氧化。在相同时间内,反应温度对剩余氨氮浓度和氨氮去除率的影响如图所示。40~60℃时氨氮去除率持续下降,其原因为
更容易被氧化。在相同时间内,反应温度对剩余氨氮浓度和氨氮去除率的影响如图所示。40~60℃时氨氮去除率持续下降,其原因为___________ 。
(2)十八面体结构的 晶体是一种高效光催化剂,可用于实现“碳中和”,也可用于降解有机污染物。
晶体是一种高效光催化剂,可用于实现“碳中和”,也可用于降解有机污染物。 沉淀的生成速率会影响其结构和形貌,从而影响其光催化性能。
沉淀的生成速率会影响其结构和形貌,从而影响其光催化性能。
①向银氨溶液中加入 溶液,离心分离、洗涤干燥后可得到
溶液,离心分离、洗涤干燥后可得到 高效光催化剂,写出反应的离子方程式为
高效光催化剂,写出反应的离子方程式为___________ 。
② 和
和 在溶液中反应也可制得
在溶液中反应也可制得 固体,但制得的
固体,但制得的 固体光催化性能极差。从速率角度解释其原因是
固体光催化性能极差。从速率角度解释其原因是___________ 。
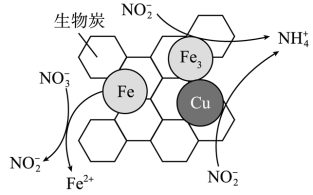
(3)将一定量纳米零价铁和少量铜粉附着在生物炭上,也可用于去除水体中 ,其部分反应原理如图所示。与不添加铜粉相比,添加少量铜粉时去除
,其部分反应原理如图所示。与不添加铜粉相比,添加少量铜粉时去除 的效率更高,其主要原因是
的效率更高,其主要原因是___________ ; 转化为
转化为 的反应机理可描述为
的反应机理可描述为___________ 。
(1)研究团队采用NaClO氧化法去除水中氨氮(
 、
、 )。已知:HClO的氧化性比NaClO强;
)。已知:HClO的氧化性比NaClO强; 比
比 更容易被氧化。在相同时间内,反应温度对剩余氨氮浓度和氨氮去除率的影响如图所示。40~60℃时氨氮去除率持续下降,其原因为
更容易被氧化。在相同时间内,反应温度对剩余氨氮浓度和氨氮去除率的影响如图所示。40~60℃时氨氮去除率持续下降,其原因为
(2)十八面体结构的
 晶体是一种高效光催化剂,可用于实现“碳中和”,也可用于降解有机污染物。
晶体是一种高效光催化剂,可用于实现“碳中和”,也可用于降解有机污染物。 沉淀的生成速率会影响其结构和形貌,从而影响其光催化性能。
沉淀的生成速率会影响其结构和形貌,从而影响其光催化性能。①向银氨溶液中加入
 溶液,离心分离、洗涤干燥后可得到
溶液,离心分离、洗涤干燥后可得到 高效光催化剂,写出反应的离子方程式为
高效光催化剂,写出反应的离子方程式为②
 和
和 在溶液中反应也可制得
在溶液中反应也可制得 固体,但制得的
固体,但制得的 固体光催化性能极差。从速率角度解释其原因是
固体光催化性能极差。从速率角度解释其原因是(3)将一定量纳米零价铁和少量铜粉附着在生物炭上,也可用于去除水体中
 ,其部分反应原理如图所示。与不添加铜粉相比,添加少量铜粉时去除
,其部分反应原理如图所示。与不添加铜粉相比,添加少量铜粉时去除 的效率更高,其主要原因是
的效率更高,其主要原因是 转化为
转化为 的反应机理可描述为
的反应机理可描述为
更新时间:2023-06-22 15:45:46
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】Ⅰ.现有甲、乙、丙三名同学分别进行Fe(OH)3胶体的制备实验。
①甲同学向1mol·L-1氯化铁溶液中加入少量的NaOH溶液;②乙同学直接加热饱和FeCl3溶液;③丙同学向25mL沸水中逐滴加入几滴FeCl3饱和溶液,继续煮沸至液体呈透明的红褐色,停止加热。
试回答下列问题:
(1)其中操作正确的同学是_____ 。写出此过程中的化学方程式:_____ 。
(2)证明有Fe(OH)3胶体生成的最简单的实验操作是_____ 。
(3)欲除去Fe(OH)3胶体中混有的NaCl,所用主要物品是_____ ;该操作名称是_____ 。
Ⅱ.有一瓶无色澄清溶液,其中可能含H+、Na+、Mg2+、Ba2+、Cl﹣、 、
、 离子。现进行以下实验:
离子。现进行以下实验:
A、用pH试纸检验溶液,发现溶液呈强酸性;
B、取部分溶液逐滴加入NaOH溶液,使溶液由酸性变为碱性,无沉淀产生;
C、取少量B中的碱性溶液,滴加Na2CO3溶液,有白色沉淀产生。
(4)根据上述事实确定:该溶液中肯定存在的离子有_____ ;肯定不存在的离子有_____ 。
(5)写出C中发生反应的离子方程式_____ 。
①甲同学向1mol·L-1氯化铁溶液中加入少量的NaOH溶液;②乙同学直接加热饱和FeCl3溶液;③丙同学向25mL沸水中逐滴加入几滴FeCl3饱和溶液,继续煮沸至液体呈透明的红褐色,停止加热。
试回答下列问题:
(1)其中操作正确的同学是
(2)证明有Fe(OH)3胶体生成的最简单的实验操作是
(3)欲除去Fe(OH)3胶体中混有的NaCl,所用主要物品是
Ⅱ.有一瓶无色澄清溶液,其中可能含H+、Na+、Mg2+、Ba2+、Cl﹣、
 、
、 离子。现进行以下实验:
离子。现进行以下实验:A、用pH试纸检验溶液,发现溶液呈强酸性;
B、取部分溶液逐滴加入NaOH溶液,使溶液由酸性变为碱性,无沉淀产生;
C、取少量B中的碱性溶液,滴加Na2CO3溶液,有白色沉淀产生。
(4)根据上述事实确定:该溶液中肯定存在的离子有
(5)写出C中发生反应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】有下列物质:①氢氧化钡固体②Na2CO3粉末③二氧化碳气体④稀硫酸⑤HNO3⑥Na2O2⑦NaClO溶液⑨熔融氯化钠⑩CuCl2固体。请用序号填空:
(1)上述状态下可导电的是___________ 。
(2)属于电解质的是___________ 。
(3)写出③与⑥反应的的化学方程式___________ ,当有4molCO2参加反应时,氧化产物的物质的量为___________ ,反应中电子转移的数目___________ 。
(4)写出⑦与过量CO2反应的的离子方程式___________ 。
(1)上述状态下可导电的是
(2)属于电解质的是
(3)写出③与⑥反应的的化学方程式
(4)写出⑦与过量CO2反应的的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】(1)请写出实验室制备Fe(OH)3胶体的离子方程式_______________ ;
请写出Cl2通入到澄清石灰水中的离子方程式_______________ 。
(2)向Ba(OH)2溶液中通入少量二氧化碳,请写出发生反应的离子方程式_______________ 。
(3)写出NH4HSO4 在水溶液中的电离方程式_______________ ;及其与NH4HCO3 在溶液中反应的离子方程式_____________________ 。
(4)写出过氧化钠与水反应的离子方程式:___________________________________ 。
(5)已知胃酸的主要成分是盐酸,请写出用小苏打片治疗胃酸过多的离子方程式______________ ;
如果病人同时患有胃溃疡,此时最好服用胃舒平【主要成分为Al(OH)3】,请写出相应的的离子方程式
_____________________________________
请写出Cl2通入到澄清石灰水中的离子方程式
(2)向Ba(OH)2溶液中通入少量二氧化碳,请写出发生反应的离子方程式
(3)写出NH4HSO4 在水溶液中的电离方程式
(4)写出过氧化钠与水反应的离子方程式:
(5)已知胃酸的主要成分是盐酸,请写出用小苏打片治疗胃酸过多的离子方程式
如果病人同时患有胃溃疡,此时最好服用胃舒平【主要成分为Al(OH)3】,请写出相应的的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】某氯水久置后不能使品红溶液褪色,可推测氯水中_______ 已分解。检验此久置氯水中 存在的操作及现象是
存在的操作及现象是_______ 。
 存在的操作及现象是
存在的操作及现象是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】Ⅰ.已知KMnO4在常温下与浓盐酸反应生成Cl2
2KMnO4+16HCl(浓)=2KCl+5Cl2↑+2MnCl2+8H2O
(1)被氧化的HCl的物质的量与实际被消耗的KMnO4的物质的量之比是___________ 。
(2)生成标准状况下3.36 L氯气,转移的电子的物质的量是___________ 。
(3)检验氯气存在可以用湿润的淀粉-KI试纸;若氯气存在,则试纸呈现___________ 色;该过程的离子方程式是___________ 。
Ⅱ.氯水是实验室中常用的液体试剂。
(4)氯气和水反应的化学方程式是___________ 。
(5)氯水中含有一种弱酸,该酸见光分解的化学方程式是___________ 。
2KMnO4+16HCl(浓)=2KCl+5Cl2↑+2MnCl2+8H2O
(1)被氧化的HCl的物质的量与实际被消耗的KMnO4的物质的量之比是
(2)生成标准状况下3.36 L氯气,转移的电子的物质的量是
(3)检验氯气存在可以用湿润的淀粉-KI试纸;若氯气存在,则试纸呈现
Ⅱ.氯水是实验室中常用的液体试剂。
(4)氯气和水反应的化学方程式是
(5)氯水中含有一种弱酸,该酸见光分解的化学方程式是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】化学在工农业生产和日常生活中有很重要的作用,完成以下问题:
(1)补血剂中铁的存在形式是二价铁,在亚铁离子中滴加氢氧化钠时生成的白色沉淀不稳定,用化学方程式说明不稳定的原因___________ 。
(2)钠盐中可用来治疗胃酸(主要成分为HCl)过多的是___________ (写化学式),用离子方程式表示其反应原理___________ 。
(3)工业上经常用绿矾(FeSO4⋅7H2O)做处理剂,清除工业废水中的重铬酸根离子 ,反应为:
,反应为: ,请用单线桥标明电子转移的方向和数目
,请用单线桥标明电子转移的方向和数目_____ 。
(4)过氧化钠经常用作航天和航海的供氧剂,其阴阳离子个数比为___________ ;200℃时,将5.8gCO2和水蒸气的混合气体与足量的Na2O2充分反应后,固体质量增加了1.8g,则原混合物中CO2和H2O的质量之比是___________ 。
(5)氯及其化合物在生产生活中应用广泛,可以运用“价—类”二维图从物质类别和核心元素的价态来学习元素及其化合物的性质。

①此二维图中所含物质属于非电解质的是___________ (填化学式)。
②从物质类别上看,HClO属于________ (填“强”或“弱”)酸,所以可与_________ (填序号)反应。
a.FeCl2 b.NaOH c.HCl
③氯水保存在___________ 中,原因是___________ (用化学方程式说明)。
(1)补血剂中铁的存在形式是二价铁,在亚铁离子中滴加氢氧化钠时生成的白色沉淀不稳定,用化学方程式说明不稳定的原因
(2)钠盐中可用来治疗胃酸(主要成分为HCl)过多的是
(3)工业上经常用绿矾(FeSO4⋅7H2O)做处理剂,清除工业废水中的重铬酸根离子
 ,反应为:
,反应为: ,请用单线桥标明电子转移的方向和数目
,请用单线桥标明电子转移的方向和数目(4)过氧化钠经常用作航天和航海的供氧剂,其阴阳离子个数比为
(5)氯及其化合物在生产生活中应用广泛,可以运用“价—类”二维图从物质类别和核心元素的价态来学习元素及其化合物的性质。

①此二维图中所含物质属于非电解质的是
②从物质类别上看,HClO属于
a.FeCl2 b.NaOH c.HCl
③氯水保存在
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】某课外小组利用原电池原理驱动某简易小车(用电动机表示)。

(1)初步设计的实验装置示意图如图1所示,CuSO4溶液在图1所示装置中的作用是_______ (答两点)。
实验发现:该装置不能驱动小车。
(2)该小组同学提出假设:
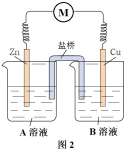
可能是氧化反应和还原反应没有完全隔开,降低了能量利用率,为进一步提高能量利用率,该小组同学在原有反应的基础上将氧化反应与还原反应隔开进行,优化的实验装置示意图如图2所示,图2中A溶液和B溶液分别是_______ 和_______ ,盐桥属于_______ (填“电子导体”或“离子导体”),盐桥中的Cl-移向_______ 溶液(填“A”或“B”)。为降低电池自重,该小组用阳离子交换膜代替盐桥,实验装置示意图如图3所示。
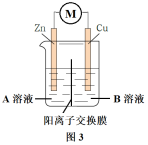
(3)利用改进后的实验装置示意图3,仍不能驱动小车,该小组同学再次提出假设:
可能是电压不够;可能是电流不够;可能是电压和电流都不够;
实验发现:1.5V的干电池能驱动小车,其电流为750μA;
实验装置示意图3的最大电压为1.0V,最大电流为200μA
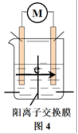
该小组从电极材料、电极反应、离子导体等角度对装置做进一步优化,请补全优化后的实验装置示意图4,并在图中标明阳离子的流向。_______

(1)初步设计的实验装置示意图如图1所示,CuSO4溶液在图1所示装置中的作用是
实验发现:该装置不能驱动小车。
(2)该小组同学提出假设:
可能是氧化反应和还原反应没有完全隔开,降低了能量利用率,为进一步提高能量利用率,该小组同学在原有反应的基础上将氧化反应与还原反应隔开进行,优化的实验装置示意图如图2所示,图2中A溶液和B溶液分别是


(3)利用改进后的实验装置示意图3,仍不能驱动小车,该小组同学再次提出假设:
可能是电压不够;可能是电流不够;可能是电压和电流都不够;
实验发现:1.5V的干电池能驱动小车,其电流为750μA;
实验装置示意图3的最大电压为1.0V,最大电流为200μA
该小组从电极材料、电极反应、离子导体等角度对装置做进一步优化,请补全优化后的实验装置示意图4,并在图中标明阳离子的流向。

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】现有如下两个反应:(A)NaOH+HCl===NaCl+H2O (B)2FeCl3+Cu===2FeCl2+CuCl2
(1)根据两反应本质,判断能否设计成原电池(填“能”或“不能”)(A)______ (B)________ ;
(2)如果(A或B)不能,说明其原因________________ ;
(3)如果(A或B)可以,则在下面方框中画出装置图并写出正、负极材料及电极反应式______

负极:________、_________________________ ;
正极:________、__________________________ 。
(1)根据两反应本质,判断能否设计成原电池(填“能”或“不能”)(A)
(2)如果(A或B)不能,说明其原因
(3)如果(A或B)可以,则在下面方框中画出装置图并写出正、负极材料及电极反应式

负极:________、
正极:________、
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】为验证不同化合价铁的氧化还原能力,利用下列电池装置进行实验。
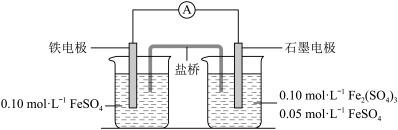
回答下列问题:
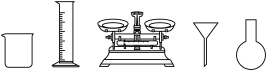
(1)由FeSO4·7H2O固体配制0.10 mol·L-1FeSO4溶液,需要的仪器有药匙、玻璃棒、________ (从下列图中选择,写出名称)。
(2)电池装置中,盐桥连接两电极电解质溶液。盐桥中阴、阳离子不与溶液中的物质发生化学反应,并且电迁移率(u∞)应尽可能地相近。根据下表数据,盐桥中应选择________ 作为电解质。
(3)电流表显示电子由铁电极流向石墨电极。可知,盐桥中的阳离子进入________ 电极溶液中。
(4)电池反应一段时间后,测得铁电极溶液中c(Fe2+)增加了0.02 mol·L-1。石墨电极上未见Fe析出。可知,石墨电极溶液中c(Fe2+)=________ 。
(5)根据(3)、(4)实验结果,可知石墨电极的电极反应式为________ ,铁电极的电极反应式为______________ 。因此,验证了Fe2+氧化性小于Fe3+还原性小于Fe。

回答下列问题:
(1)由FeSO4·7H2O固体配制0.10 mol·L-1FeSO4溶液,需要的仪器有药匙、玻璃棒、

(2)电池装置中,盐桥连接两电极电解质溶液。盐桥中阴、阳离子不与溶液中的物质发生化学反应,并且电迁移率(u∞)应尽可能地相近。根据下表数据,盐桥中应选择
| 阳离子 | u∞×108/(m2·s-1·V-1) | 阴离子 | u∞×108/(m2·s-1·V-1) |
| Li+ | 4.07 |  | 4.61 |
| Na+ | 5.19 |  | 7.40 |
| Ca2+ | 6.59 | Cl- | 7.91 |
| K+ | 7.62 |  | 8.27 |
(3)电流表显示电子由铁电极流向石墨电极。可知,盐桥中的阳离子进入
(4)电池反应一段时间后,测得铁电极溶液中c(Fe2+)增加了0.02 mol·L-1。石墨电极上未见Fe析出。可知,石墨电极溶液中c(Fe2+)=
(5)根据(3)、(4)实验结果,可知石墨电极的电极反应式为
您最近一年使用:0次



