现有如下两个反应:(A)NaOH+HCl===NaCl+H2O (B)2FeCl3+Cu===2FeCl2+CuCl2
(1)根据两反应本质,判断能否设计成原电池(填“能”或“不能”)(A)______ (B)________ ;
(2)如果(A或B)不能,说明其原因________________ ;
(3)如果(A或B)可以,则在下面方框中画出装置图并写出正、负极材料及电极反应式______

负极:________、_________________________ ;
正极:________、__________________________ 。
(1)根据两反应本质,判断能否设计成原电池(填“能”或“不能”)(A)
(2)如果(A或B)不能,说明其原因
(3)如果(A或B)可以,则在下面方框中画出装置图并写出正、负极材料及电极反应式

负极:________、
正极:________、
更新时间:2017-07-11 12:18:26
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】回答下列问题:
(1)通过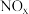 传感器可监测
传感器可监测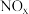 的含量,其工作原理示意图如下:
的含量,其工作原理示意图如下:
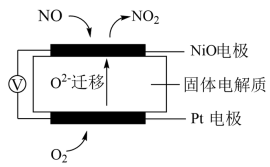
① 电极上发生的是
电极上发生的是_______ 反应(填“氧化”或“还原”)电极反应式_______ 。
②写出 电极的电极反应式:
电极的电极反应式:_______ 。
(2)用零价铁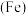 去除水体中的硝酸盐
去除水体中的硝酸盐 已成为环境修复研究的热点之一。
已成为环境修复研究的热点之一。 还原水体中
还原水体中 的反应原理如图所示。
的反应原理如图所示。
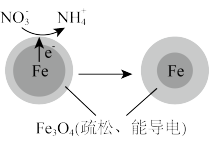
①作负极的物质是_______ 。
②正极的电极反应式是_______ 。
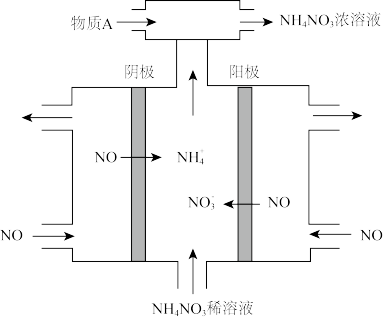
(3)电解 制备
制备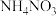 ,其工作原理如图所示,为使电解产物全部转化为
,其工作原理如图所示,为使电解产物全部转化为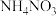 ,需补充物质A,A是
,需补充物质A,A是_______ ,说明理由:_______ 。
(1)通过
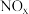 传感器可监测
传感器可监测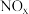 的含量,其工作原理示意图如下:
的含量,其工作原理示意图如下:
①
 电极上发生的是
电极上发生的是②写出
 电极的电极反应式:
电极的电极反应式:(2)用零价铁
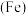 去除水体中的硝酸盐
去除水体中的硝酸盐 已成为环境修复研究的热点之一。
已成为环境修复研究的热点之一。 还原水体中
还原水体中 的反应原理如图所示。
的反应原理如图所示。
①作负极的物质是
②正极的电极反应式是
(3)电解
 制备
制备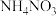 ,其工作原理如图所示,为使电解产物全部转化为
,其工作原理如图所示,为使电解产物全部转化为 ,需补充物质A,A是
,需补充物质A,A是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】通过化学方法可使能量按人们所期望的形式转化,从而开辟新能源和提高能量转化率。回答下列问题:
(1)根据构成原电池本质判断,如下反应可以设计成原电池的是_______(填标号)。
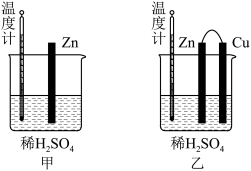
(2)为了探究化学反应中的能量变化,某同学设计了如图两个实验。有关实验现象,下列说法正确的是_______(填标号)。
(3)如图是甲烷燃料电池的工作原理示意图。

①电池的负极是_______ 电极(填“a”或“b”),该极的电极反应为_______ 。
②电池工作一段时间后,电解质溶液的
_______ (填“增大”“减小”或“不变”)。
(4)熔融盐燃料电池具有很高的发电效率,因而受到重视。可用碳酸锂和碳酸钠的熔融盐混合物作电解质,一氧化碳为负极燃气,空气与二氧化碳的混合气为正极助燃气,制得在 下工作的燃料电池,其负极反应为
下工作的燃料电池,其负极反应为 。
。
①正极反应式为_______ 。
②总反应式为_______ 。
(1)根据构成原电池本质判断,如下反应可以设计成原电池的是_______(填标号)。
A.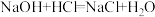 | B. |
C.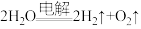 | D. |

| A.图甲和图乙的气泡均产生于锌棒表面 |
| B.图乙中产生气体的速率比图甲快 |
| C.图甲中温度计显示的最高温度高于图乙中温度计显示的最高温度 |
| D.图甲和图乙中温度计显示的温度相等,且均高于室温 |

①电池的负极是
②电池工作一段时间后,电解质溶液的

(4)熔融盐燃料电池具有很高的发电效率,因而受到重视。可用碳酸锂和碳酸钠的熔融盐混合物作电解质,一氧化碳为负极燃气,空气与二氧化碳的混合气为正极助燃气,制得在
 下工作的燃料电池,其负极反应为
下工作的燃料电池,其负极反应为 。
。①正极反应式为
②总反应式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】回答下列问题
(1)甲、乙两位同学想探究铝电极在原电池中的作用,两人均用镁片和铝片作电极,但甲同学将电极放入稀硫酸中,乙同学将电极放入NaOH溶液中,实验装置如图所示。
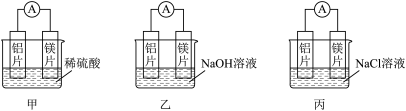
①写出甲中电池总反应的离子方程式:_______ 。
②乙中铝为_______ 极,写出铝电极的电极反应式:_______ 。
③甲同学后来继续按图丙进行实验,该装置_______ 产生电流。(填“会”或“不会”)。
(2)硅太阳能电池中用到硅。三氯甲硅烷( )还原法是当前制备高纯硅的主要方法,生产过程示意图如图:
)还原法是当前制备高纯硅的主要方法,生产过程示意图如图:
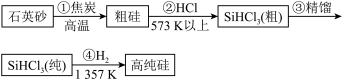
第①步制备粗硅的化学方程式为:_______ 。
 遇水剧烈反应生成
遇水剧烈反应生成 、HCl和另一种物质,写出
、HCl和另一种物质,写出 遇水的化学反应方程式:
遇水的化学反应方程式:_______ 。
(3)铜的电极可以用稀硝酸来用溶解,写出其反应的离子方程式_______ 。
(4)把盛有48mLNO和 混合气体的容器倒置于水中(保持同温同压),待液面稳定后,容器内气体的体积变为24mL,则原混合气中
混合气体的容器倒置于水中(保持同温同压),待液面稳定后,容器内气体的体积变为24mL,则原混合气中 是
是_______ mL。
(1)甲、乙两位同学想探究铝电极在原电池中的作用,两人均用镁片和铝片作电极,但甲同学将电极放入稀硫酸中,乙同学将电极放入NaOH溶液中,实验装置如图所示。

①写出甲中电池总反应的离子方程式:
②乙中铝为
③甲同学后来继续按图丙进行实验,该装置
(2)硅太阳能电池中用到硅。三氯甲硅烷(
 )还原法是当前制备高纯硅的主要方法,生产过程示意图如图:
)还原法是当前制备高纯硅的主要方法,生产过程示意图如图:
第①步制备粗硅的化学方程式为:
 遇水剧烈反应生成
遇水剧烈反应生成 、HCl和另一种物质,写出
、HCl和另一种物质,写出 遇水的化学反应方程式:
遇水的化学反应方程式:(3)铜的电极可以用稀硝酸来用溶解,写出其反应的离子方程式
(4)把盛有48mLNO和
 混合气体的容器倒置于水中(保持同温同压),待液面稳定后,容器内气体的体积变为24mL,则原混合气中
混合气体的容器倒置于水中(保持同温同压),待液面稳定后,容器内气体的体积变为24mL,则原混合气中 是
是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】目前,第三代混合动力车已经投入市场,成为能源改革的典范。
(1)混合动力车一般使用镍氢电池,碱液(主要为KOH溶液)为电解质溶液。镍氢电池的充放电反应式为H2+2NiOOH 2Ni(OH)2。请写出该电池放电时正极的电极反应方程式:
2Ni(OH)2。请写出该电池放电时正极的电极反应方程式:_____ 。
(2)为实现电池的安全性,科技工作者开发出利用稀土金属氧化物作为固体电解质的氢气—空气燃料电池。这种稀土金属氧化物在高温下能传导O2-。写出该电池放电时的负极反应方程式:_____ 。
(1)混合动力车一般使用镍氢电池,碱液(主要为KOH溶液)为电解质溶液。镍氢电池的充放电反应式为H2+2NiOOH
 2Ni(OH)2。请写出该电池放电时正极的电极反应方程式:
2Ni(OH)2。请写出该电池放电时正极的电极反应方程式:(2)为实现电池的安全性,科技工作者开发出利用稀土金属氧化物作为固体电解质的氢气—空气燃料电池。这种稀土金属氧化物在高温下能传导O2-。写出该电池放电时的负极反应方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】I.关于工业合成氨的反应,已知H-H键、N-H键、N≡N键的键能分别为436kJ·mol-1、391kJ·mol-1、946kJ·mol-1。请根据键能的数据判断下列问题。
(1)由N2和H2合成氨时,若有1molNH3生成,反应需要_______ (填“吸收”或“放出”)_______ kJ的能量。
II.符合某些特征的化学反应理论上都可以设计成原电池。
(2)下列化学反应_______ (填字母)可以设计成原电池。
①CH4+2O2=CO2+2H2O
②Fe+CuSO4=FeSO4+Cu
③2NaOH+H2SO4=Na2SO4+2H2O
④Pb+PbO2+2H2SO4=2PbSO4+2H2O
⑤Al2O3+2NaOH=2NaAlO2+H2O
(3)如图是一个简易的原电池装置。请回答下列问题:

①若a电极材料为Ag、b为硝酸银溶液,反应一段时间后,铜片质量_______ (填“增加”、“不变”或“减轻”),银片质量_______ (填“增加”、“不变”或“减轻”)。
②若a电极材料为碳、b为FeCl3溶液,写出正极的电极反应式_______ 。
III.肼(液态)—过氧化氢碱性燃料电池由于其较高的能量密度而备受关注,其工作原理如图所示。

(4)该电池的B极区发生_______ (填“氧化反应”或“还原反应”),电池工作过程中,OH-向_______ 极移动(填“A”或“B”)。
(5)该燃料电池的总反应式可表示为_______ 。在标准状况下,若A极区产生11.2LN2,则外电路中理论上通过的电子的物质的量是_______ mol。
(1)由N2和H2合成氨时,若有1molNH3生成,反应需要
II.符合某些特征的化学反应理论上都可以设计成原电池。
(2)下列化学反应
①CH4+2O2=CO2+2H2O
②Fe+CuSO4=FeSO4+Cu
③2NaOH+H2SO4=Na2SO4+2H2O
④Pb+PbO2+2H2SO4=2PbSO4+2H2O
⑤Al2O3+2NaOH=2NaAlO2+H2O
(3)如图是一个简易的原电池装置。请回答下列问题:

①若a电极材料为Ag、b为硝酸银溶液,反应一段时间后,铜片质量
②若a电极材料为碳、b为FeCl3溶液,写出正极的电极反应式
III.肼(液态)—过氧化氢碱性燃料电池由于其较高的能量密度而备受关注,其工作原理如图所示。

(4)该电池的B极区发生
(5)该燃料电池的总反应式可表示为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】在一定条件下,化学能与电能可以相互转化。
(1)二甲醚燃料电池工作原理如图所示
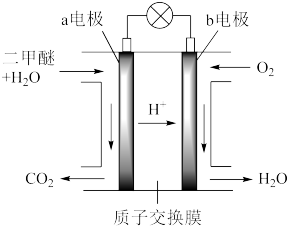
①电极a为电池的_____ (填“正”或“负”)极。
②电极b的电极反应式:_____ 。
③标准状况下,消耗11.2LO2时,转移的电子数为____ mol。
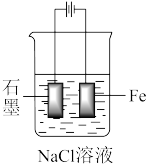
(2)①下图装置中石墨上发生_____ 反应,电极反应式为____ 。
②装置中Fe片____ (填“不易”或“容易”)被腐蚀,电极反应式为____ 。
③一段时间后,烧杯中的溶液的pH将____ (填“变大”、“变小”或“不变”)。
(1)二甲醚燃料电池工作原理如图所示

①电极a为电池的
②电极b的电极反应式:
③标准状况下,消耗11.2LO2时,转移的电子数为
(2)①下图装置中石墨上发生
②装置中Fe片
③一段时间后,烧杯中的溶液的pH将

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】詹姆斯·韦伯太空望远镜捕捉到第一批火星图像。火星本身不发光, 其红色的外观源于表层土壤中丰富的铁元素及反射的太阳光。
(1)火星反射的光线通过气态原子后经过棱镜色散分光后得到了一系列不连续的暗线,该光谱属于___________ (填“吸收”或“发射”)光谱。
(2)已知铁是第 26 号元素,铁在元素周期表中的位置是___________ ,基态铁原子价电子轨道表示式为___________ ,其核外有___________ 种不同运动状态的电子。
(3)某实验小组为探究 Fe 与 Fe3+能否发生氧化还原反应,试设计对应的双液原电池___________ 。
(1)火星反射的光线通过气态原子后经过棱镜色散分光后得到了一系列不连续的暗线,该光谱属于
(2)已知铁是第 26 号元素,铁在元素周期表中的位置是
(3)某实验小组为探究 Fe 与 Fe3+能否发生氧化还原反应,试设计对应的双液原电池
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】微生物燃料电池是一种利用微生物将有机物中的化学能直接转化成电能的装置。已知某种利用微生物的甲醇燃料电池中,电解质溶液为酸性,示意图如下:

(1)该电池外电路电子的流动方向为_______ (填“从A到B”或“从B到A”)。
(2)电池工作结束后,B电极室溶液的pH与工作前相比将_______ (填“增大”“减小”或“不变”,溶液体积变化忽略不计)。
(3)A电极附近甲醇发生的电极反应式为_______ 。

(1)该电池外电路电子的流动方向为
(2)电池工作结束后,B电极室溶液的pH与工作前相比将
(3)A电极附近甲醇发生的电极反应式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】电化学给人类的生活和工业生产带来极大的方便。回答下列问题:
(1)一种利用垃圾渗滤液中 、
、 发电的原理如图所示。
发电的原理如图所示。

①X为该装置的_______ 极。
②写出Y极的电极反应式:_______ 。
(2)电解池在生产中有广泛的应用。
①工业上电解精炼银的装置如图1所示,_______ (填“a”或“b”)极为含有杂质的粗银,b极的电极反应式为_______ ,若b极有少量红棕色气体产生,则生成该气体的电极反应式为_______ 。

②氯碱工业:用离子交换膜法电解饱和食盐水的装置如图2所示,①口有带刺激性气味的气体逸出,则A为外电源的_______ 极,与B相连的电极的电极反应式为_______ 。为了获得产品( 和
和 ),应选用
),应选用_______ (填“阴”或“阳”)离子交换膜。
(1)一种利用垃圾渗滤液中
 、
、 发电的原理如图所示。
发电的原理如图所示。
①X为该装置的
②写出Y极的电极反应式:
(2)电解池在生产中有广泛的应用。
①工业上电解精炼银的装置如图1所示,

②氯碱工业:用离子交换膜法电解饱和食盐水的装置如图2所示,①口有带刺激性气味的气体逸出,则A为外电源的
 和
和 ),应选用
),应选用
您最近一年使用:0次



