詹姆斯·韦伯太空望远镜捕捉到第一批火星图像。火星本身不发光, 其红色的外观源于表层土壤中丰富的铁元素及反射的太阳光。
(1)火星反射的光线通过气态原子后经过棱镜色散分光后得到了一系列不连续的暗线,该光谱属于___________ (填“吸收”或“发射”)光谱。
(2)已知铁是第 26 号元素,铁在元素周期表中的位置是___________ ,基态铁原子价电子轨道表示式为___________ ,其核外有___________ 种不同运动状态的电子。
(3)某实验小组为探究 Fe 与 Fe3+能否发生氧化还原反应,试设计对应的双液原电池___________ 。
(1)火星反射的光线通过气态原子后经过棱镜色散分光后得到了一系列不连续的暗线,该光谱属于
(2)已知铁是第 26 号元素,铁在元素周期表中的位置是
(3)某实验小组为探究 Fe 与 Fe3+能否发生氧化还原反应,试设计对应的双液原电池
更新时间:2024-01-03 15:14:52
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】Ⅰ.依据氧化还原反应: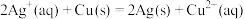 设计的原电池如下图所示,
设计的原电池如下图所示,
(1)电极X的材料是________ ;电解质溶液Y是________ ;
(2)银电极为原电池的_________ 极。(填“正”或“负”)
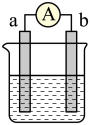
Ⅱ.如图是某化学兴趣小组探究不同条件下化学能转变为电能的装置。请回答下列问题:______ ,若初始时两电极质量相等,当电路中有0.2mole-通过时,两电极的质量差为______ g。
(4)当电极a为 ,电极b为Cu,电解质溶液为浓硝酸时,则电池的正极反应式为
,电极b为Cu,电解质溶液为浓硝酸时,则电池的正极反应式为______ ,对比(3)和(4),说明原电池中相对活泼的金属做正极还是负极,除了与金属本身的还原性有关外,还与______ 有关。
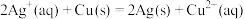 设计的原电池如下图所示,
设计的原电池如下图所示,
(1)电极X的材料是
(2)银电极为原电池的
Ⅱ.如图是某化学兴趣小组探究不同条件下化学能转变为电能的装置。请回答下列问题:
(4)当电极a为
 ,电极b为Cu,电解质溶液为浓硝酸时,则电池的正极反应式为
,电极b为Cu,电解质溶液为浓硝酸时,则电池的正极反应式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】能源是现代社会发展的三大支柱之一,化学在提高能源的利用率和开发新能源中起到了重要的作用。电能是现代社会中应用最广泛的二次能源。
(1)下列装置中能够实现化学能转化为电能的是______ (填字母)。
(2)该装置正极材料为______ (填电极的化学式),发生了______ 反应(氧化或还原)。
(3)若装置中转移了0.2mol电子,负极减少的质量是______ 。
(4)有甲、乙两位同学均想利用原电池反应检测金属的活动性强弱,两人均使用镁片与铝片作电极,但甲同学将电极放入6mol•L-1的H2SO4溶液中,乙同学将电极放入6mol•L-1的NaOH溶液中,如图所示:

写出甲池中正极参与反应的离子:______ ;写出乙池总反应的离子方程式______ 。
(5)科学家制造出了一种使用固体电解质的燃料电池,其效率很高,可用于航天航空。如图丙所示装置中,以稀土金属材料为惰性电极,在两极上分别通入CH4和空气,其中固体电解质是掺杂了Y2O3的ZrO2固体,它在高温下能传导O2-。则c电极的名称为______ (填“正极”或“负极”),d电极上的电极反应式为______ 。

(1)下列装置中能够实现化学能转化为电能的是
A. | B. | C. | D. |
(3)若装置中转移了0.2mol电子,负极减少的质量是
(4)有甲、乙两位同学均想利用原电池反应检测金属的活动性强弱,两人均使用镁片与铝片作电极,但甲同学将电极放入6mol•L-1的H2SO4溶液中,乙同学将电极放入6mol•L-1的NaOH溶液中,如图所示:

写出甲池中正极参与反应的离子:
(5)科学家制造出了一种使用固体电解质的燃料电池,其效率很高,可用于航天航空。如图丙所示装置中,以稀土金属材料为惰性电极,在两极上分别通入CH4和空气,其中固体电解质是掺杂了Y2O3的ZrO2固体,它在高温下能传导O2-。则c电极的名称为

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】化学电源在日常生活和工业生产中有着重要的应用。
Ⅰ.如图所示,某同学设计了一个燃料电池并探究氯碱工业原理和粗铜的精炼原理,其中乙装置中X为阳离子交换膜。请按要求回答相关问题:
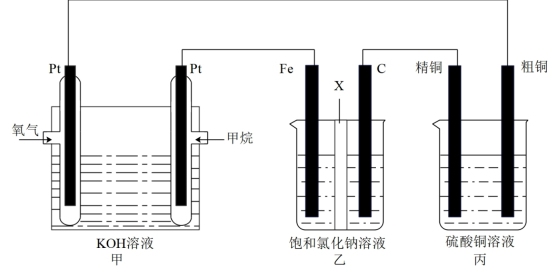
(1)甲烷燃料电池负极的电极反应式为___________ 。
(2)C极的电极反应式为___________ 。
(3)若有2.24L(标准状况下)氧气参加反应,则乙装置中铁极上生成的气体体积为___________ L(标准状况下);丙装置中阴极析出铜的质量为___________ g。
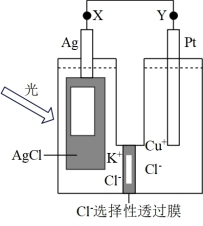
Ⅱ.科学家发明的一种光化学电池可充分利用太阳能,其结构如图所示,电池总反应为AgCl(s)+Cu+(aq)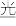 Ag(s)+Cu2+(aq)+Cl-(aq)
Ag(s)+Cu2+(aq)+Cl-(aq)
(4)①Cl-的迁移方向为___________ (填“正极到负极”或“负极到正极”)。
②正极的电极反应式为___________ 。
③若用该光化学电池为手机充电并将手机电池从零电量充满,若该手机电池容量为3200mA/h,则理论上消耗AgCl的质量为___________ g(保留一位小数)(已知:1库仑约为1.0×10-5mol电子所带的电量)。
Ⅰ.如图所示,某同学设计了一个燃料电池并探究氯碱工业原理和粗铜的精炼原理,其中乙装置中X为阳离子交换膜。请按要求回答相关问题:

(1)甲烷燃料电池负极的电极反应式为
(2)C极的电极反应式为
(3)若有2.24L(标准状况下)氧气参加反应,则乙装置中铁极上生成的气体体积为
Ⅱ.科学家发明的一种光化学电池可充分利用太阳能,其结构如图所示,电池总反应为AgCl(s)+Cu+(aq)
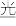 Ag(s)+Cu2+(aq)+Cl-(aq)
Ag(s)+Cu2+(aq)+Cl-(aq)
(4)①Cl-的迁移方向为
②正极的电极反应式为
③若用该光化学电池为手机充电并将手机电池从零电量充满,若该手机电池容量为3200mA/h,则理论上消耗AgCl的质量为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】锌锰干电池是应用最普遍的电池之一。其基本反应为:
X极:Zn-2e-=Zn2+
Y极:2MnO2+2NH +2e-=Mn2O3+2NH3+H2O
+2e-=Mn2O3+2NH3+H2O
(1)X是电池的_______ (填“正”或“负”,下同)极,Y是电池的_______ 极。
(2)该电池总反应的离子方程式为:_______ 。该反应中MnO2是_______ (填“还原剂”或“氧化剂”)。
(3)若反应消耗16.25gZn,则电池中转移电子的物质的量为_______ 。
X极:Zn-2e-=Zn2+
Y极:2MnO2+2NH
 +2e-=Mn2O3+2NH3+H2O
+2e-=Mn2O3+2NH3+H2O(1)X是电池的
(2)该电池总反应的离子方程式为:
(3)若反应消耗16.25gZn,则电池中转移电子的物质的量为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】已知电极材料:铁、铜、银、石墨、锌、铝;电解质溶液: 溶液、
溶液、 溶液、稀硫酸。按要求回答下列问题:
溶液、稀硫酸。按要求回答下列问题:
(1)电工操作上规定:不能把铜导线和铝导线连接在一起使用。请说明原因:________________ 。
(2)若电极材料选铜和石墨,电解质溶液选 溶液,外加导线,能否构成原电池?
溶液,外加导线,能否构成原电池?______ 。若能,请写出电极反应式,负极:__________________ ,正极:_________________ (若不能,后两空不填)。
(3)设计一种以铁和稀硫酸反应为原理的原电池,在下面的方框中画出装置图__________ (需标明电极材料及电池的正负极)。

 溶液、
溶液、 溶液、稀硫酸。按要求回答下列问题:
溶液、稀硫酸。按要求回答下列问题:(1)电工操作上规定:不能把铜导线和铝导线连接在一起使用。请说明原因:
(2)若电极材料选铜和石墨,电解质溶液选
 溶液,外加导线,能否构成原电池?
溶液,外加导线,能否构成原电池?(3)设计一种以铁和稀硫酸反应为原理的原电池,在下面的方框中画出装置图

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】双极膜由阳离子交换膜、催化剂层和阴离子交换膜组合而成,在直流电场作用下可将水解离,在双极膜的两侧分别得到H+和OH-,将其与阳离子交换膜(阳膜)、阴离子交换膜(阴膜)组合,可有多种应用。
(1)海水淡化:模拟海水淡化,并获得浓盐酸和浓氢氧化钠溶液。双极膜组合电解装置示意图如图。

①X极是___ 极。
②图中双极膜的右侧得到的是___ (填“H+”或“OH-”),电解后在___ 出口可获得较浓的盐酸(填“a”“b”或“c”)。
③电解过程中阳极区溶液中的n(OH-)___ (填“变大”“变小”或“基本不变”)。
(2)新型Zn—CO2水介质电池,为解决环境和能源问题提供了一种新途径。电池示意图如图,电极为金属锌和选择性催化材料。放电时温室气体CO2被转化为储氢物质甲酸等。

①放电时电池负极反应为___ 。
②放电时,1molCO2转化为HCOOH,转移的电子数为___ mol。
③充电时,电池总反应为___ 。
(1)海水淡化:模拟海水淡化,并获得浓盐酸和浓氢氧化钠溶液。双极膜组合电解装置示意图如图。

①X极是
②图中双极膜的右侧得到的是
③电解过程中阳极区溶液中的n(OH-)
(2)新型Zn—CO2水介质电池,为解决环境和能源问题提供了一种新途径。电池示意图如图,电极为金属锌和选择性催化材料。放电时温室气体CO2被转化为储氢物质甲酸等。

①放电时电池负极反应为
②放电时,1molCO2转化为HCOOH,转移的电子数为
③充电时,电池总反应为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】下表为元素周期表的一部分,表中所列字母编号分别代表对应的化学元素。完成下列填空:
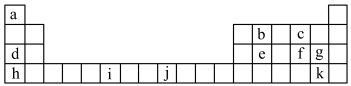
(1)图中所示元素形成的物质中,最高价氧化物对应水化物酸性最强的是_______ (填化学式),可用作半导体材料的是_______ (填元素符号),属于过渡元素的是_______ (填元素符号)。
(2)b元素可形成种类丰富的化合物,它在周期表中的第_______ 周期第_______ 族,其氧化物的随意排放可能导致的环境问题是_______ 。
(3)j元素化合物有着丰富的颜色,古罗马人曾利用它的化合物制造蓝色玻璃。该元素属于_______ 区元素,其基态原子的价电子轨道表示式为_______ 。
(4)d、h元素中,金属性更强的是_______ (填元素符号),请从原子结构角度解释其原因:_______ 。

(1)图中所示元素形成的物质中,最高价氧化物对应水化物酸性最强的是
(2)b元素可形成种类丰富的化合物,它在周期表中的第
(3)j元素化合物有着丰富的颜色,古罗马人曾利用它的化合物制造蓝色玻璃。该元素属于
(4)d、h元素中,金属性更强的是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】(1)A元素原子核外M层电子数是L层电子数的一半,请写出 A元素基态时核外电子排布式:_______ 。
(2)B原子的最外层电子排布式为nsnnp2n ,则B元素在元素周期表的中位置为第___ 周期___ 族。
(3)人们常将在同一原子轨道上运动的,自旋方向相反的2个电子,称为“电子对”;将在同一原子轨道上运动的单个电子,称为“未成对电子”。那么硫原子的“未成对电子” 有_____ 个。
(2)B原子的最外层电子排布式为nsnnp2n ,则B元素在元素周期表的中位置为第
(3)人们常将在同一原子轨道上运动的,自旋方向相反的2个电子,称为“电子对”;将在同一原子轨道上运动的单个电子,称为“未成对电子”。那么硫原子的“未成对电子” 有
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】回答下列问题:
(1) 元素基态原子的最外层有
元素基态原子的最外层有 个未成对电子,次外层有
个未成对电子,次外层有 个电子,其元素符号为
个电子,其元素符号为_______ ;其价电子排布图为_______ 。
(2) 元素的负一价离子和
元素的负一价离子和 元素的正一价离子的电子层结构都与氩相同,
元素的正一价离子的电子层结构都与氩相同, 的元素符号为
的元素符号为_______ , 离子的结构示意图为
离子的结构示意图为_______ 。
(3) 元素的正三价离子的
元素的正三价离子的 能级为半充满,
能级为半充满, 的元素符号为
的元素符号为_______ ,其基态原子的电子排布式为_______ ,其原子的结构示意图为_______ 。
(4) 元素基态原子的
元素基态原子的 层全充满,
层全充满, 层没有成对电子且只有一个未成对电子,
层没有成对电子且只有一个未成对电子, 的元素符号为
的元素符号为_______ ,其基态原子的电子排布式为_______ 。
(5) 元素的原子最外层电子排布式为
元素的原子最外层电子排布式为 ,则
,则
_______ ;原子中能量最高的是_______ 电子,核外电子排布图为_______ 。
(1)
 元素基态原子的最外层有
元素基态原子的最外层有 个未成对电子,次外层有
个未成对电子,次外层有 个电子,其元素符号为
个电子,其元素符号为(2)
 元素的负一价离子和
元素的负一价离子和 元素的正一价离子的电子层结构都与氩相同,
元素的正一价离子的电子层结构都与氩相同, 的元素符号为
的元素符号为 离子的结构示意图为
离子的结构示意图为(3)
 元素的正三价离子的
元素的正三价离子的 能级为半充满,
能级为半充满, 的元素符号为
的元素符号为(4)
 元素基态原子的
元素基态原子的 层全充满,
层全充满, 层没有成对电子且只有一个未成对电子,
层没有成对电子且只有一个未成对电子, 的元素符号为
的元素符号为(5)
 元素的原子最外层电子排布式为
元素的原子最外层电子排布式为 ,则
,则
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】日光等白光经棱镜折射后产生的是 __________ 光谱。原子光谱则与之不同,它是由不连续特征谱线组成的,称为 ____________ 光谱。根据原子光谱谱线的分析结果,可以得到的信息是原子轨道能量的变化是不连续的,这种情况又称为原子中电子的能量是 ___________ 的。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】阿散酸(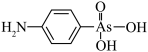 )是一种饲料添加剂,能溶于NaOH溶液中,常含有
)是一种饲料添加剂,能溶于NaOH溶液中,常含有 、NaCl等杂质。回答下列问题(用元表符号或化学式表示):
、NaCl等杂质。回答下列问题(用元表符号或化学式表示):
 原子核外电子占据的最高能级为
原子核外电子占据的最高能级为(2)As元素的第一电离能
(3)
 的中心原子的杂化方式为
的中心原子的杂化方式为 的空间构型为
的空间构型为(4)太阳电池材料中的很多金属或金属化合物在灼烧时会产生特殊的火焰颜色,请用原子结构的知识阐述产生此现象的原因是
(5)阿散酸分子中C和N的杂化类型分别是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】Ti、Na、Mg、C、N、O、Fe等元素单质及化合物在诸多领域都有广泛的应用。回答下列问题:
(1)钠在火焰上灼烧产生的黄光是一种_______ (填字母)。
A.吸收光谱 B.发射光谱
(2)下列Mg原子的核外电子排布式中,能量最高的是_______ ,能量最低的是_______ (填序号)
a.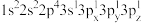 b.
b. c.
c. d.1s22s22p63s2
d.1s22s22p63s2
(3)Ti原子核外共有_______ 种运动状态不同的电子,最高能层电子的电子云轮廓形状为_______ 。与Ti同周期的所有过渡元素的基态原子中,写出任意一种最外层电子数与钛不同的元素外围电子排布式_______ 。
(4)N、O、Mg元素的前3级电离能如下表所示:X、Y、Z中为N元素的是_______ ,判断理由是_______ 。
(5)琥珀酸亚铁片是用于缺铁性贫血的预防和治疗的常见药物,临床建议服用维生素C促进“亚铁”的吸收,避免生成Fe3+,从结构角度来看,Fe2+易被氧化成Fe3+的原因是_______ 。Fe3+与Fe2+的离子半径大小关系为:Fe3+_______ Fe2+(填“大于”或“小于”),原因为:_______ 。
(1)钠在火焰上灼烧产生的黄光是一种
A.吸收光谱 B.发射光谱
(2)下列Mg原子的核外电子排布式中,能量最高的是
a.
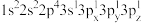 b.
b. c.
c. d.1s22s22p63s2
d.1s22s22p63s2(3)Ti原子核外共有
(4)N、O、Mg元素的前3级电离能如下表所示:X、Y、Z中为N元素的是
| 元素 | I1/kJ·mol-1 | I2/kJ·mol-1 | I3/kJ·mol-1 |
| X | 737.7 | 1 450.7 | 7 732.7 |
| Y | 1 313.9 | 3 388.3 | 5 300.5 |
| Z | 1 402.3 | 2 856.0 | 4 578.1 |
您最近一年使用:0次



