Ti、Na、Mg、C、N、O、Fe等元素单质及化合物在诸多领域都有广泛的应用。回答下列问题:
(1)钠在火焰上灼烧产生的黄光是一种_______ (填字母)。
A.吸收光谱 B.发射光谱
(2)下列Mg原子的核外电子排布式中,能量最高的是_______ ,能量最低的是_______ (填序号)
a.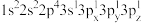 b.
b. c.
c. d.1s22s22p63s2
d.1s22s22p63s2
(3)Ti原子核外共有_______ 种运动状态不同的电子,最高能层电子的电子云轮廓形状为_______ 。与Ti同周期的所有过渡元素的基态原子中,写出任意一种最外层电子数与钛不同的元素外围电子排布式_______ 。
(4)N、O、Mg元素的前3级电离能如下表所示:X、Y、Z中为N元素的是_______ ,判断理由是_______ 。
(5)琥珀酸亚铁片是用于缺铁性贫血的预防和治疗的常见药物,临床建议服用维生素C促进“亚铁”的吸收,避免生成Fe3+,从结构角度来看,Fe2+易被氧化成Fe3+的原因是_______ 。Fe3+与Fe2+的离子半径大小关系为:Fe3+_______ Fe2+(填“大于”或“小于”),原因为:_______ 。
(1)钠在火焰上灼烧产生的黄光是一种
A.吸收光谱 B.发射光谱
(2)下列Mg原子的核外电子排布式中,能量最高的是
a.
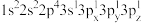 b.
b. c.
c. d.1s22s22p63s2
d.1s22s22p63s2(3)Ti原子核外共有
(4)N、O、Mg元素的前3级电离能如下表所示:X、Y、Z中为N元素的是
| 元素 | I1/kJ·mol-1 | I2/kJ·mol-1 | I3/kJ·mol-1 |
| X | 737.7 | 1 450.7 | 7 732.7 |
| Y | 1 313.9 | 3 388.3 | 5 300.5 |
| Z | 1 402.3 | 2 856.0 | 4 578.1 |
更新时间:2022-11-28 13:29:49
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】下图是元素周期表的一部分,表中的①~⑩中元素,用元素符号或化学式填空回答:
(1)在这些元素中,化学性质最不活泼的原子的原子结构示意图为_______ 。
(2)地壳中含量最多的金属元素是____ ,写出元素⑥的简单气态氢化物的化学式______ 。
(3)这些元素中的最高价氧化物对应的水化物中,碱性最强的是______ ,呈两性的氢氧化物是_______ 。
(4)写出②、③、⑤对应离子的离子半径由大到小的顺序是______ ,
(5)写出②、⑦、⑩对应阴离子还原性由强到弱的顺序是______ 。
(6)元素⑦与元素⑩相比,非金属性较强的是____ ,能证明这一事实的依据是_____ 。
族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 二 | ⑥ | ① | ② | |||||
| 三 | ③ | ④ | ⑤ | ⑪ | ⑦ | ⑧ | ||
| 四 | ⑨ | ⑩ |
(2)地壳中含量最多的金属元素是
(3)这些元素中的最高价氧化物对应的水化物中,碱性最强的是
(4)写出②、③、⑤对应离子的离子半径由大到小的顺序是
(5)写出②、⑦、⑩对应阴离子还原性由强到弱的顺序是
(6)元素⑦与元素⑩相比,非金属性较强的是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】如图是元素周期表的一部分,表中所列字母a、b、c、d、e、f、g分别代表某种化学元素。请依据这7种元素回答下列问题。
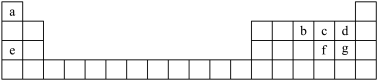
(1)上述7种元素中非金属性最强的是____ (填元素符号,下同)。
(2)由c、f两种元素形成的具有漂白作用的物质,把该物质通入盛有g单质的水溶液中发生反应的离子反应方程式____ 。
(3)g在元素周期表中的位置是____ ,其最高价氧化物为____ 。
(4)e、f、g的离子半径由小到大的顺序是___ 。c、e、g三种元素形成原子个数比为1:1:1的化合物的电子式____ 。
(5)c和f元素对应的气态氢化物的沸点更高的是____ ,原因是____ 。
(6)写出f的最高价氧化物对应的水化物的浓溶液与木炭在加热条件下发生反应的化学方程式____ 。

(1)上述7种元素中非金属性最强的是
(2)由c、f两种元素形成的具有漂白作用的物质,把该物质通入盛有g单质的水溶液中发生反应的离子反应方程式
(3)g在元素周期表中的位置是
(4)e、f、g的离子半径由小到大的顺序是
(5)c和f元素对应的气态氢化物的沸点更高的是
(6)写出f的最高价氧化物对应的水化物的浓溶液与木炭在加热条件下发生反应的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】下表是元素周期表的一部分,针对表中的①~⑩种元素,填写下列空白(填写序号不得分):
(1)⑦元素的离子半径__ S2-(填“>”或“<”),比较③与⑥的氢化物,___ 更稳定(填化学式),最不活泼的元素是___ (填元素符号)。
(2)在最高价氧化物的水化物中,酸性最强的化合物的化学式是____ ,碱性最强的化合物的化学式是:_____ 。
(3)比较①与⑤的最高价氧化物对应的水化物,_____ 的酸性强(填化学式),能证明两者酸性强弱的离子反应方程式为______
(4)实验室制取②的氢化物的化学方程式________
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑨ | ⑩ |
(1)⑦元素的离子半径
(2)在最高价氧化物的水化物中,酸性最强的化合物的化学式是
(3)比较①与⑤的最高价氧化物对应的水化物,
(4)实验室制取②的氢化物的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】按要求填空
(1)写出溴原子的核外电子排布式_______
(2)写出氮原子的轨道表示式_________
(3)请解释Fe3+比Fe2+稳定的原因________
(4)由23Na、35Cl、37Cl构成的15g氯化钠中,37Cl的质量为_______
(1)写出溴原子的核外电子排布式
(2)写出氮原子的轨道表示式
(3)请解释Fe3+比Fe2+稳定的原因
(4)由23Na、35Cl、37Cl构成的15g氯化钠中,37Cl的质量为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】铁镁合金是一种性能优异的储氢材料。关于铁镁两种元素,请回答下列问题:
(1)同周期元素中,第一电离能小于镁的元素有___________ 种。
(2)基态Fe原子的简化电子排布式为___________ ,其中电子的空间运动状态有___________ 种,Fe位于元周期表的___________ 区。
(3)与Fe元素同周期,基态原子有2个未成对电子的金属元素有___________ 种,下列状态的铁中,电离最外层一个电子所需能量最大的是___________ (填标号)。 易被氧化为
易被氧化为
___________ 。
(1)同周期元素中,第一电离能小于镁的元素有
(2)基态Fe原子的简化电子排布式为
(3)与Fe元素同周期,基态原子有2个未成对电子的金属元素有
a.[Ar] 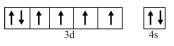 b.[Ar]
b.[Ar]
c.[Ar] d.[Ar]
d.[Ar]
 易被氧化为
易被氧化为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】现有六种元素,其中A、B、C、D、E为短周期主族元素,F为第4周期元素,它们的原子序数依次增大。请根据下列相关信息回答问题。
(1)B元素基态原子具有_______ 种运动状态不同的电子,能量最高的电子,其电子云在空间有_______ 个伸 展方向。
(2)根据上述信息,画出C元素基态原子的轨道表示式_______ 。
(3)F在元素周期表中属于_______ 区元素,其基态原子核外共有_______ 个未成对电子。
(4)D、E两元素的第一电离能大小关系是_______ (用元素符号表示,下同),B、D两元素的电负性大小关系是_______ 。
(5)写出DA3的电子式:_______ (用元素符号表示)。
| 元素 | 相关信息 |
| A | 元素的原子核外电子数和电子层数相等,也是宇宙中最丰富的元素 |
| B | 元素原子的核外p电子数比s电子数少1 |
| C | 元素的第一至第四电离能分别是I1=738 kJ/mol、I2=1451 kJ/mol、I3= 7733 kJ/mol、I4= 10540 kJ/mol |
| D | 原子核外填充电子的所有p轨道全满或半满 |
| E | 元素的主族序数与周期序数的差为3 |
| F | 在元素周期表的第6列 |
(2)根据上述信息,画出C元素基态原子的轨道表示式
(3)F在元素周期表中属于
(4)D、E两元素的第一电离能大小关系是
(5)写出DA3的电子式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】太阳能电池材料的很多金属或金属化合物在灼烧时会产生特殊的火焰颜色,请用原子结构的知识阐述产生此现象的原因:___________ 。
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】日光等白光经棱镜折射后产生的是 __________ 光谱。原子光谱则与之不同,它是由不连续特征谱线组成的,称为 ____________ 光谱。根据原子光谱谱线的分析结果,可以得到的信息是原子轨道能量的变化是不连续的,这种情况又称为原子中电子的能量是 ___________ 的。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】詹姆斯·韦伯太空望远镜捕捉到第一批火星图像。火星本身不发光, 其红色的外观源于表层土壤中丰富的铁元素及反射的太阳光。
(1)火星反射的光线通过气态原子后经过棱镜色散分光后得到了一系列不连续的暗线,该光谱属于___________ (填“吸收”或“发射”)光谱。
(2)已知铁是第 26 号元素,铁在元素周期表中的位置是___________ ,基态铁原子价电子轨道表示式为___________ ,其核外有___________ 种不同运动状态的电子。
(3)某实验小组为探究 Fe 与 Fe3+能否发生氧化还原反应,试设计对应的双液原电池___________ 。
(1)火星反射的光线通过气态原子后经过棱镜色散分光后得到了一系列不连续的暗线,该光谱属于
(2)已知铁是第 26 号元素,铁在元素周期表中的位置是
(3)某实验小组为探究 Fe 与 Fe3+能否发生氧化还原反应,试设计对应的双液原电池
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】(1)与铜同周期、基态原子最外层电子数相同的过渡元素,其基态原子的电子排布式______________ 。
(2)下图曲线表示部分短周期元素的原子序数(按递增顺序排列)和其常见单质沸点的关系。其中A点表示的单质是________ (填化学式)。

(3)三氟化硼分子的空间构型是__________ ;三溴化硼、三氯化硼分子结构与三氟化硼相似,如果把B—X键都当作单键考虑来计算键长,理论值与实测键长结果如下表。硼卤键长实测值比计算值要短得多,可能的原因是____________________________________________ 。

(4)CuCl的盐酸溶液能吸收CO生成复合物氯化羰基亚铜【Cu2C12(CO)2·2H20】,其结构如图。

①该复合物中Cl原子的杂化类型为_______________ 。
②该复合物中的配位体有________________ 种。
(5)已知HF与Fˉ通过氢键结合成 。判断
。判断 和
和 微粒间能否形成氢键,并说明理由。
微粒间能否形成氢键,并说明理由。____________________________________ 。
(2)下图曲线表示部分短周期元素的原子序数(按递增顺序排列)和其常见单质沸点的关系。其中A点表示的单质是

(3)三氟化硼分子的空间构型是

(4)CuCl的盐酸溶液能吸收CO生成复合物氯化羰基亚铜【Cu2C12(CO)2·2H20】,其结构如图。

①该复合物中Cl原子的杂化类型为
②该复合物中的配位体有
(5)已知HF与Fˉ通过氢键结合成
 。判断
。判断 和
和 微粒间能否形成氢键,并说明理由。
微粒间能否形成氢键,并说明理由。
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】下表为元素周期表的一部分,其中编号代表对应的元素。
请回答下列问题:
(1)写出元素⑦的价电子排布图__________ ,⑧的原子结构示意图__________ 。71号元素属于_______ 周期,________ 族,_______ 区。
(2)若元素①③⑤形成的某化合物中三种元素的质量比为1:6:8,该化合物对氢气的相对密度为15,该分子中心原子的杂化方式为______________ 。
(3)④和⑥形成的分子构型___________ 。
(4)③的某种同素异形体被称为混合型晶体,具有平面层状结构。该晶体中含有的作用力为______________________________________ 。
(5)②与⑤形成的化合物的熔点___________ ②与⑨形成化合物的熔点(填“高于”或“低于”)
(6)⑩的第一次出现突变的电离能数据是I2,则它的下一个出现突变的电离能数据是_______ 。
| ① | |||||||||||||||||||||
| ② | ③ | ④ | ⑤ | ⑥ | |||||||||||||||||
| ⑩ | ⑨ | ||||||||||||||||||||
| ⑦ | ⑧ | ||||||||||||||||||||
请回答下列问题:
(1)写出元素⑦的价电子排布图
(2)若元素①③⑤形成的某化合物中三种元素的质量比为1:6:8,该化合物对氢气的相对密度为15,该分子中心原子的杂化方式为
(3)④和⑥形成的分子构型
(4)③的某种同素异形体被称为混合型晶体,具有平面层状结构。该晶体中含有的作用力为
(5)②与⑤形成的化合物的熔点
(6)⑩的第一次出现突变的电离能数据是I2,则它的下一个出现突变的电离能数据是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】回答下列问题:
(1)用“>”或“<”填写下表。
(2)一种制取NH2OH的反应为2NO2-+4SO2 + 6H2O+ 6NH3 = 4SO +6NH4++2NH2OH。
+6NH4++2NH2OH。
①N、H、O的电负性从小 到大 的顺序为____ 。
②NH3分子的空间构型为____ 。
③NH2OH极易溶于H2O,除因为它们都是极性分子外,还因为____ 。
(3)配合物K[PtCl3(NH3)]中[PtCl3(NH3)]-的结构可用示意图表示为____ (不考虑空间构型)。
(1)用“>”或“<”填写下表。
| 第一电离能 | 熔点 | 沸点(同压) | 键能 |
| P | MgO | CF4 | H-Cl |
(2)一种制取NH2OH的反应为2NO2-+4SO2 + 6H2O+ 6NH3 = 4SO
 +6NH4++2NH2OH。
+6NH4++2NH2OH。①N、H、O的电负性从
②NH3分子的空间构型为
③NH2OH极易溶于H2O,除因为它们都是极性分子外,还因为
(3)配合物K[PtCl3(NH3)]中[PtCl3(NH3)]-的结构可用示意图表示为
您最近一年使用:0次



