19. 甲醇(CH
3OH)是重要的溶剂和替代燃料,工业上用CO和H
2在一定条件下制备CH
3OH的反应为CO(g)+2H
2(g)

CH
3OH(g) ΔH。
(1)在体积为1L的恒容密闭容器中,充入2molCO和4molH
2,一定条件下发生上述反应,测得CO(g)和CH
3OH(g)的浓度随时间变化如图所示。
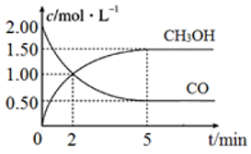
①从反应开始到2 min,用氢气表示的平均反应速率
v(H
2)=
__________。
②下列说法正确的是
______________(填字母序号)。
A.达到平衡时,H
2的转化率为75%
B.5min后容器中压强不再改变
C.达到平衡后,再充入氩气,反应速率增大
D.2min前v(正)>v(逆),2min后v(正)<v(逆)
(2)某温度下,在一恒压容器中分别充入1.2molCO和1molH
2,达到平衡时容器体积为2L,且含有0.4molCH
3OH(g),则该反应平衡常数的值为
_______,此时向容器中再通入0.35molCO气体,则此平衡将
______________(填“向正反应方向”、“不”或“向逆反应方向”)移动。
(3)工业上另一种合成甲醇的方法是利用CO
2和H
2,已知:CH
3OH、H
2的燃烧热(ΔH)分别为-726.5kJ/mol、-285.8kJ/mol,则常温下CO
2和H
2反应生成CH
3OH和H
2O的热化学方程式是
______________________。
(4)CH
3OH(l)作为一种燃料还可用于燃料电池。在温度为650℃的熔融盐燃料电池中用甲醇、空气与CO
2的混合气体作反应物,镍作电极,用Li
2CO
3和Na
2CO
3混合物作电解质。该电池的负极反应式为
______________________。