氮是自然界各种生命活动不可缺少的重要元素。
I.自然界中氮的循环(如图所示)

(1)豆科植物的根瘤进行固氮的过程属于______ (填“化学”或“物理)变化;通过雷电作用进行固氮过程中,第一步反应的化学方程式为______ 。
(2)某氮肥厂产生的氨氮废水中的氮元素多以 和
和 的形式存在,设计如下处理流程:
的形式存在,设计如下处理流程:

①过程I:加NaOH溶液,调节pH至9后,升温至30℃,通入空气将氨赶出并回收。加入NaOH溶液时,所发生反应的离子方程式为______ 。
②过程II:在微生物作用下实现 的转化,称为硝化过程。在碱性条件下,
的转化,称为硝化过程。在碱性条件下, 被氧气氧化为
被氧气氧化为 的总反应的离子方程式为
的总反应的离子方程式为______ 。
II.实验室制氨气
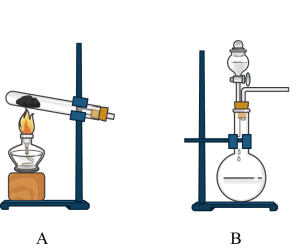
(3)实验室制备氨气可以选择A或B装置,如果选择A装置,则发生反应的化学方程式为______ ;如果选择B装置,则分液漏斗中盛装的物质为______ (填名称):干燥氨气时,可选用的干燥剂为______ ;收集氨气采用______ 法。
III.浓硝酸和稀硝酸氧化性强弱比较
(4)按如图所示装置进行实验(加持装置已略去),实验证明浓硝酸的氧化性强于稀硝酸,依据为浓硝酸能将NO氧化为NO2,而稀硝酸不能。
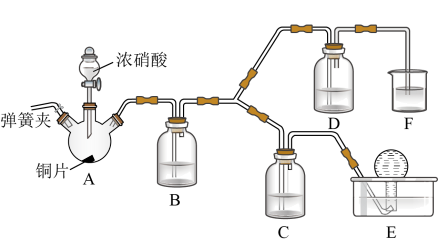
已知:NaOH溶液不与NO反应,能与NO2反应。
①浓硝酸应保存在棕色试剂瓶中,用化学方程式解释其原因为______ 。
②装置A中发生反应的化学方程式为______ ;装置B的作用为______ 。
③装置D中的现象为______ ;C中盛放的试剂为______ 。
I.自然界中氮的循环(如图所示)

(1)豆科植物的根瘤进行固氮的过程属于
(2)某氮肥厂产生的氨氮废水中的氮元素多以
 和
和 的形式存在,设计如下处理流程:
的形式存在,设计如下处理流程:
①过程I:加NaOH溶液,调节pH至9后,升温至30℃,通入空气将氨赶出并回收。加入NaOH溶液时,所发生反应的离子方程式为
②过程II:在微生物作用下实现
 的转化,称为硝化过程。在碱性条件下,
的转化,称为硝化过程。在碱性条件下, 被氧气氧化为
被氧气氧化为 的总反应的离子方程式为
的总反应的离子方程式为II.实验室制氨气
(3)实验室制备氨气可以选择A或B装置,如果选择A装置,则发生反应的化学方程式为

III.浓硝酸和稀硝酸氧化性强弱比较
(4)按如图所示装置进行实验(加持装置已略去),实验证明浓硝酸的氧化性强于稀硝酸,依据为浓硝酸能将NO氧化为NO2,而稀硝酸不能。

已知:NaOH溶液不与NO反应,能与NO2反应。
①浓硝酸应保存在棕色试剂瓶中,用化学方程式解释其原因为
②装置A中发生反应的化学方程式为
③装置D中的现象为
更新时间:2023-06-30 15:23:01
|
相似题推荐
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】氮及其化合物是工农业生产中的重要原料。请按要求回答下列问题。
(1)氮气的电子式为____ ;构成氨分子的原子中电负性较大的是____ ;氨分子的空间构型为___ 。
(2)自然界中氮循环涉及以下过程。
①NH 转化为可被植物吸收NO
转化为可被植物吸收NO 的过程如图:
的过程如图:
NH
 NO
NO
 NO
NO
此过程中的氧化剂是___ 。
②N2和H2在固氮酶的作用下得到NH3,被水吸收生成被植物吸收的NH ,其中固氮酶的作用是
,其中固氮酶的作用是____ 。工业固氮路径与之有些相似,请完善如下转化过程(写化学式):___ 、___ 。
N2 NH3
NH3 ( )
( )
雷雨发庄稼的固氮过程如下,补充中间物质的化学式:___ 、___ 、___ 。
N2→( )→( )→( )→NO (硝酸盐)
(硝酸盐)
(3)氨气水溶性的探究
①根据氨的分子结构预测其水溶性:____ ,预测依据的是(写一条)____ 。
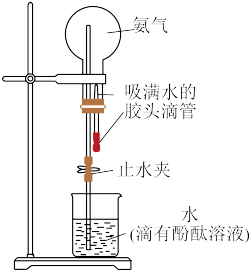
②利用如图装置进行实验,观察的现象是_____ ;合理的验证操作为____ 。
③新制的氨水中含氮元素的微粒有NH3、_____ 、____ ,用合理的化学用语解释:____ 。
(1)氮气的电子式为
(2)自然界中氮循环涉及以下过程。
①NH
 转化为可被植物吸收NO
转化为可被植物吸收NO 的过程如图:
的过程如图:NH

 NO
NO
 NO
NO
此过程中的氧化剂是
②N2和H2在固氮酶的作用下得到NH3,被水吸收生成被植物吸收的NH
 ,其中固氮酶的作用是
,其中固氮酶的作用是N2
 NH3
NH3 ( )
( )雷雨发庄稼的固氮过程如下,补充中间物质的化学式:
N2→( )→( )→( )→NO
 (硝酸盐)
(硝酸盐)(3)氨气水溶性的探究
①根据氨的分子结构预测其水溶性:
②利用如图装置进行实验,观察的现象是
③新制的氨水中含氮元素的微粒有NH3、

您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐2】氮元素在海洋中的循环,是整个海洋生态系统的基础和关键。海洋中无机氮的循环过程可用图表示。

(1)海洋中的氮循环起始于氮的固定,其中属于固氮作用的一步是______ (填图中数字序号)
(2)下列关于海洋氮循环的说法正确的是______ (填字母序号)
a.海洋中存在游离态的氮
b.海洋中的氮循环起始于氮的氧化
c.海洋中的反硝化作用一定有氧气的参与
d.向海洋排放含 的废水会影响海洋中
的废水会影响海洋中 的含量
的含量
(3)有氧时,在硝化细菌作用下, 可实现过程④的转化,将过程④的离子方程式补充完整:
可实现过程④的转化,将过程④的离子方程式补充完整:___  +5O2=2
+5O2=2 +
+___ H++______ +______
(4)为了避免含氮废水对海洋氮循环系统的影响,需经处理后排放。如图是电解产物氧化工业废水中氨氮( )的示意图。
)的示意图。
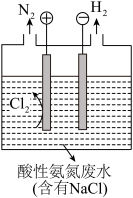
①阳极的电极反应式:______ ;
②写出电解产物氧化去除氨氮的离子方程式:______ ;
③若生成H2和N2的物质的量之比为3:1,则处理后废水的c(H+)将______ (填“增大”“不变”或“减小”)。

(1)海洋中的氮循环起始于氮的固定,其中属于固氮作用的一步是
(2)下列关于海洋氮循环的说法正确的是
a.海洋中存在游离态的氮
b.海洋中的氮循环起始于氮的氧化
c.海洋中的反硝化作用一定有氧气的参与
d.向海洋排放含
 的废水会影响海洋中
的废水会影响海洋中 的含量
的含量(3)有氧时,在硝化细菌作用下,
 可实现过程④的转化,将过程④的离子方程式补充完整:
可实现过程④的转化,将过程④的离子方程式补充完整: +5O2=2
+5O2=2 +
+(4)为了避免含氮废水对海洋氮循环系统的影响,需经处理后排放。如图是电解产物氧化工业废水中氨氮(
 )的示意图。
)的示意图。
①阳极的电极反应式:
②写出电解产物氧化去除氨氮的离子方程式:
③若生成H2和N2的物质的量之比为3:1,则处理后废水的c(H+)将
您最近一年使用:0次
【推荐3】氮元素在海洋中的循环,是整个海洋生态系统的基础和关键。海洋中无机氮的循环过程可用下图表示。

(1)海洋中的氮循环起始于氮的固定,其中属于固氮作用的一步是_____ (填图中数字序号)。
(2)下列关于海洋氮循环的说法正确的是_____ (填字母序号)。
a.海洋中存在游离态的氮
b.海洋中的氮循环起始于氮的氧化
c.海洋中的反硝化作用一定有氧气的参与
d.向海洋排放含NO 的废水会影响海洋中NH
的废水会影响海洋中NH 的含量
的含量
(3)有氧时,在硝化细菌作用下,NH 可实现过程④的转化,将过程④的离子方程式补充完整:4NH
可实现过程④的转化,将过程④的离子方程式补充完整:4NH +5O2 =2NO
+5O2 =2NO +_____H++_____+
+_____H++_____+
____________________________________________________________
(4)为避免含氮废水对海洋氮循环系统的影响,需经处理后排放。右图是间接氧化工业废水中氨氮(NH )示意图。
)示意图。

①结合电极反应式简述间接氧化法去除氨氮的原理:_____ 。
② 若生成H2和N2的物质的量之比为3:1,则处理后废水的pH将______ 填“增大”“不变”或“减小”)。

(1)海洋中的氮循环起始于氮的固定,其中属于固氮作用的一步是
(2)下列关于海洋氮循环的说法正确的是
a.海洋中存在游离态的氮
b.海洋中的氮循环起始于氮的氧化
c.海洋中的反硝化作用一定有氧气的参与
d.向海洋排放含NO
 的废水会影响海洋中NH
的废水会影响海洋中NH 的含量
的含量(3)有氧时,在硝化细菌作用下,NH
 可实现过程④的转化,将过程④的离子方程式补充完整:4NH
可实现过程④的转化,将过程④的离子方程式补充完整:4NH +5O2 =2NO
+5O2 =2NO +_____H++_____+
+_____H++_____+ (4)为避免含氮废水对海洋氮循环系统的影响,需经处理后排放。右图是间接氧化工业废水中氨氮(NH
 )示意图。
)示意图。
①结合电极反应式简述间接氧化法去除氨氮的原理:
② 若生成H2和N2的物质的量之比为3:1,则处理后废水的pH将
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】已知:A、B、C、D四种短周期元素,A与D的原子序数之和等于B与C的原子序数之和,由D元素组成的单质在通常状况下呈黄绿色,B、C、D三种元素位于同一周期,A、B、C三种元素的最高价氧化物对应的水化物分别为X、Y、Z,且存在如下图转化关系,试推断回答下列问题。

(1)D元素原子的结构示意图为_____________ ;
(2)A、B、C三种元素的原子半径由小到大的顺序为______________ (用元素符号表示);
(3)Y与C元素的最高价氧化物可以发生反应,该反应的离子方程式为_______________ ;
(4)A的气态氢化物的电子式___________________ ;
(5)实验室中,制取A的气态氢化物的化学方程式_________________________________ 。

(1)D元素原子的结构示意图为
(2)A、B、C三种元素的原子半径由小到大的顺序为
(3)Y与C元素的最高价氧化物可以发生反应,该反应的离子方程式为
(4)A的气态氢化物的电子式
(5)实验室中,制取A的气态氢化物的化学方程式
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐2】I.铝土矿(主要成分为Al2O3,还含有SiO2、Fe2O3)是工业上制备氧化铝的主要原料.工业上提取氧化铝的工艺流程如下:

(1)沉淀A的成分是(填化学式)_________ 。
(2)步骤②中加入过量NaOH溶液发生反应的离子方程式,除了H++OH﹣=H2O、Fe3++3OH﹣=Fe(OH)3↓还有:______________________________ ;
(3)步骤③中通入过量CO2气体,除发生CO2+OH-=HCO3-外,还发生的离子方程式有___________________________________________________________________ 。
II.工业上在一定温度和催化剂条件下用NH3将NO2还原生成N2,某同学在实验室中对NH3与NO2反应进行了探究。


①实验室可以用A、B或C装置制取氨气,如果用C装置,则该装置中烧瓶所盛放的试剂为________ (写名称)。如果用B装置,反应的化学方程式是____________________________ 。
②预收集一瓶干燥的氨气,选择上图中的装置,其气体收集和尾气处理装置连接顺序依次为发生装置→________________ (用字母表示)。
③将上述收集到的NH3充入注射器X中,硬质玻璃管Y中加入少量催化剂,充入NO2(两端用夹子K1、K2夹好)。在一定温度下按图装置进行实验。打开K1,推动注射器活塞,使X中的气体缓慢通入Y管中,Y管观察到的实验现象是_____________________________ ,反应的化学方程式为__________________ 。


(1)沉淀A的成分是(填化学式)
(2)步骤②中加入过量NaOH溶液发生反应的离子方程式,除了H++OH﹣=H2O、Fe3++3OH﹣=Fe(OH)3↓还有:
(3)步骤③中通入过量CO2气体,除发生CO2+OH-=HCO3-外,还发生的离子方程式有
II.工业上在一定温度和催化剂条件下用NH3将NO2还原生成N2,某同学在实验室中对NH3与NO2反应进行了探究。


①实验室可以用A、B或C装置制取氨气,如果用C装置,则该装置中烧瓶所盛放的试剂为
②预收集一瓶干燥的氨气,选择上图中的装置,其气体收集和尾气处理装置连接顺序依次为发生装置→
③将上述收集到的NH3充入注射器X中,硬质玻璃管Y中加入少量催化剂,充入NO2(两端用夹子K1、K2夹好)。在一定温度下按图装置进行实验。打开K1,推动注射器活塞,使X中的气体缓慢通入Y管中,Y管观察到的实验现象是

您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】甲、乙、丙三位同学分别用下图所示实验装置制取氨气。请你根据实验探究的过程,回答下列有关问题。___________ 。
(2)三位同学用上述装置制取氨气时,其中有一位同学没有收集到氨气(实验操作都正确),你认为没有收集到氨气的同学是___________ (填“甲”、“乙”或“丙”)。
(3)为确定试管内是否已收集满氨气,将蘸有浓盐酸的玻璃棒接近试管口,观察的现象是___________ ,该反应的化学方程式是___________ 。
(4)三位同学都认为他们的实验装置还可用于加热碳酸氢铵固体来制取纯净的氨气,你判断能够达到实验目的同学是___________ (填“甲”、“乙”或“丙”)。
(5)氨是一种重要的化工产品,经过一系列反应可以得到硝酸,其中氨被氧化生成一氧化氮的化学方程式为___________ 。
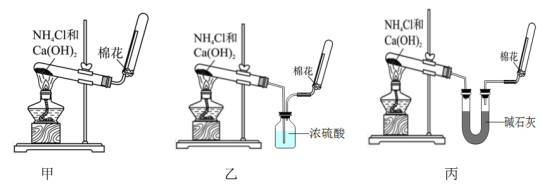
(2)三位同学用上述装置制取氨气时,其中有一位同学没有收集到氨气(实验操作都正确),你认为没有收集到氨气的同学是
(3)为确定试管内是否已收集满氨气,将蘸有浓盐酸的玻璃棒接近试管口,观察的现象是
(4)三位同学都认为他们的实验装置还可用于加热碳酸氢铵固体来制取纯净的氨气,你判断能够达到实验目的同学是
(5)氨是一种重要的化工产品,经过一系列反应可以得到硝酸,其中氨被氧化生成一氧化氮的化学方程式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】亚硝酸钠(NaNO2)在漂白、电镀等方面应用广泛。以木炭浓硝酸、水和铜为原料制备亚硝酸钠的装置如图所示:
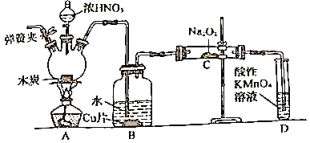
已知:
室温下,①2NO+Na2O2===2NaNO2
②3NaNO2+3HCl===3NaCl+HNO3+2NO↑+H2O
③酸性条件下,NO或NO2ˉ都能与MnO4ˉ反应生成NO3ˉ和Mn2+
回答下列问题:
(1)检查完该装置的气密性,装入药品后,实验开始前通入一段时间N2,然后关闭弹簧夹,再滴加浓硝酸,加热。通入N2的作用是________________________________________ 。
(2)装置B中观察到的主要现象为________________________________________ ,发生反应离子方程式是_____________ 。
(3)装置D的作用是______________________________ ,发生反应的离子方程式是________________________________________ 。
(4)预测C中反应开始阶段,固体产物除NaNO2外,还含有的副产物有Na2CO3和__________ (写化学式)。为避免产生这些副产物,应在装置B、C间增加干燥管,则干燥管中盛放的试剂为__________ (写名称)。
(5)利用改进后的装置将3.12gNa2O2完全转化为NaNO2,理论上至少需要木炭__________ g

已知:
室温下,①2NO+Na2O2===2NaNO2
②3NaNO2+3HCl===3NaCl+HNO3+2NO↑+H2O
③酸性条件下,NO或NO2ˉ都能与MnO4ˉ反应生成NO3ˉ和Mn2+
回答下列问题:
(1)检查完该装置的气密性,装入药品后,实验开始前通入一段时间N2,然后关闭弹簧夹,再滴加浓硝酸,加热。通入N2的作用是
(2)装置B中观察到的主要现象为
(3)装置D的作用是
(4)预测C中反应开始阶段,固体产物除NaNO2外,还含有的副产物有Na2CO3和
(5)利用改进后的装置将3.12gNa2O2完全转化为NaNO2,理论上至少需要木炭
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】某研究小组为了探究硝酸的性质,进行如下实验操作。
(1)从试剂柜中取一瓶浓硝酸,发现其保存在_______ 色试剂瓶中,取少量浓硝酸于试管中,发现其溶液呈“黄色”,其原因是_______ (用化学方程式解释)。该研究小组尝试将显“黄色”的浓硝酸恢复到原本的无色。下列措施合理的是_______ (填字母)。
a.向浓硝酸中加水
b.向浓硝酸中通入适量空气
c.加热浓硝酸
d.向浓硝酸中加入适量的NaOH固体
(2)向浓硝酸中加入稍过量铜片,该小组同学发现,生成的气体开始呈红棕色后逐渐变浅,最终气体变为无色。试写出上述反应中刚开始产生红棕色气体的化学式:_______ ,在上述反应中,硝酸体现的性质为_______ 。
(3)当实验完毕,该小组同学向试管中滴入少量稀 ,发现铜片又逐渐溶解,产生无色气体,试写出上述反应的离子方程式:
,发现铜片又逐渐溶解,产生无色气体,试写出上述反应的离子方程式:_______ 。
(4)该小组同学向浓硝酸中加入少量碳粉,无明显现象,缓慢加热,发现碳粉逐渐溶解,产生红棕色气体,试写出上述反应的化学方程式:_______ ,在该反应中硝酸体现的性质为_______ 。
(1)从试剂柜中取一瓶浓硝酸,发现其保存在
a.向浓硝酸中加水
b.向浓硝酸中通入适量空气
c.加热浓硝酸
d.向浓硝酸中加入适量的NaOH固体
(2)向浓硝酸中加入稍过量铜片,该小组同学发现,生成的气体开始呈红棕色后逐渐变浅,最终气体变为无色。试写出上述反应中刚开始产生红棕色气体的化学式:
(3)当实验完毕,该小组同学向试管中滴入少量稀
 ,发现铜片又逐渐溶解,产生无色气体,试写出上述反应的离子方程式:
,发现铜片又逐渐溶解,产生无色气体,试写出上述反应的离子方程式:(4)该小组同学向浓硝酸中加入少量碳粉,无明显现象,缓慢加热,发现碳粉逐渐溶解,产生红棕色气体,试写出上述反应的化学方程式:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】某化学小组按下图所示实验流程比较浓硝酸和稀硝酸的氧化性强弱,其中B为一种紫红色金属,C为红棕色气体。

请回答下列问题:
(1)A与B反应的化学方程式是___________ ;
(2)实验时在装置Ⅰ中加入B后,在加入A之前需向整套装置中通入足量的CO2气体,该操作的目的是___________ 。
(3)装置Ⅱ中发生反应的化学方程式是___________ 。
(4)通过实验可得出:浓硝酸的氧化性比稀硝酸___________ (填“强”或“弱”),判断的依据是___________ 。
(5)小组内有同学指出该流程中装置V可有可无,你认为装置Ⅴ是否需要___________ (填“是”或“否”),理由是___________ 。

请回答下列问题:
(1)A与B反应的化学方程式是
(2)实验时在装置Ⅰ中加入B后,在加入A之前需向整套装置中通入足量的CO2气体,该操作的目的是
(3)装置Ⅱ中发生反应的化学方程式是
(4)通过实验可得出:浓硝酸的氧化性比稀硝酸
(5)小组内有同学指出该流程中装置V可有可无,你认为装置Ⅴ是否需要
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】X、Y、Z均为短周期元素,原子序数依次增大,X和Y同主族,Y和Z同周期,Y与Z能形成离子个数比为1︰1的离子化合物A,X与Z能形成原子个数比为1︰1的共价化合物B,它们之间转化关系如下图(部分产物已略去):

(1)反应①的化学方程式为___________ 。
(2)D溶液呈碱性的原因是(用离子方程式表示)___________ 。
(3)反应②的离子方程式为___________ 。
(4)工业上常将C溶液置于铁锅内直接加热得到固体C,此过程中会生成氢氧化亚铁等杂质,可加入硝酸钠使氢氧化亚铁氧化,然后脱水变成氧化铁沉降得到较纯的固体C,写出加入硝酸钠除杂的化学方程式___________ 。

(1)反应①的化学方程式为
(2)D溶液呈碱性的原因是(用离子方程式表示)
(3)反应②的离子方程式为
(4)工业上常将C溶液置于铁锅内直接加热得到固体C,此过程中会生成氢氧化亚铁等杂质,可加入硝酸钠使氢氧化亚铁氧化,然后脱水变成氧化铁沉降得到较纯的固体C,写出加入硝酸钠除杂的化学方程式
您最近一年使用:0次


 均为中学常见的纯净物,它们之间有转化关系(其它产物及反应条件已略去,反应可以在水溶液中进行)。
均为中学常见的纯净物,它们之间有转化关系(其它产物及反应条件已略去,反应可以在水溶液中进行)。 ,若A为有刺激性气味的气体,溶液呈碱性;C为红棕色气体,与水反应生成一元强酸D,D具有强氧化性。
,若A为有刺激性气味的气体,溶液呈碱性;C为红棕色气体,与水反应生成一元强酸D,D具有强氧化性。 的化学方程式为
的化学方程式为 与D稀溶液反应生成B的离子方程式
与D稀溶液反应生成B的离子方程式

