锌铜原电池的工作原理
(1)ZnZnSO4半电池:在ZnSO4溶液中,锌片逐渐溶解,即Zn被_______ ,锌原子失去电子,形成Zn2+进入溶液,即Zn-2e-=Zn2+;从锌片上释放出的_______ ,经过导线流向铜片。
(2)CuCuSO4半电池:CuSO4溶液中的Cu2+从铜片上得到_______ ,_______ 为铜单质并沉积在铜片上,即Cu2++2e-=Cu。
(3)盐桥的作用:电池工作时,盐桥中的_______ 会移向ZnSO4溶液,_______ 移向CuSO4溶液,使两溶液均保持电中性。当取出盐桥后,形成断路,反应停止。
| 装置示意图 | 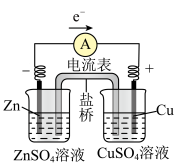 注:盐桥中装有含KCl饱和溶液的琼胶 |
| 现象 | 锌片 |
| 能量转换 | |
| 微观探析 | 在硫酸锌溶液中,负极一端的 在硫酸铜溶液中,正极一端的 |
| 电子或离子移动方向 | 电子: 盐桥: |
| 工作原理,电极反应式 | 负极:Zn-2e-=Zn2+( 正极:Cu2++2e-=Cu( |
| 总反应:Zn+Cu2+=Zn2++Cu |
(2)CuCuSO4半电池:CuSO4溶液中的Cu2+从铜片上得到
(3)盐桥的作用:电池工作时,盐桥中的
2023高二上·全国·专题练习 查看更多[1]
(已下线)【知识图鉴】单元讲练测选择性必修1第4单元01讲核心
更新时间:2023-07-06 20:44:47
|
相似题推荐
填空题
|
较易
(0.85)
解题方法
【推荐1】依据氧化还原反应Zn(s)+Cu2+(aq)===Zn2+(aq)+Cu(s)设计的原电池如下图所示。

请回答下列问题:
(1)电极X的材料是____________ ;电解质溶液Y是__________________ 。
(2)铜电极为电池的________ 极,发生的电极反应为_______________________ X极上发生的电极反应为______________ 。
(3)外电路中的电子是从________ 极流向__________ 极(填名称)。
(4)盐桥中的Cl-向________ 极移动,如将盐桥撤掉,电流计的指针将________ 偏转。

请回答下列问题:
(1)电极X的材料是
(2)铜电极为电池的
(3)外电路中的电子是从
(4)盐桥中的Cl-向
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】一种以铝-空气电池为电源的航标灯,只要把灯放入海水几分钟,就会发出耀眼的光。海水为电解质溶液,该电池靠空气中的氧气使铝氧化而源源不断地产生电流,其能量比干电池高20~50倍。请写出该电池的电极反应及总反应_____ 。
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】某校化学兴趣小组进行探究性活动:将氧化还原反应2Fe3++2I-=2Fe2++I2设计成带盐桥的原电池。提供的试剂:FeCl3溶液、KI溶液;其他用品任选。回答下列问题:
(1)画出设计的原电池装置图,并标出电极材料、电极名称及电解质溶液。
(2)发生氧化反应的电极反应式为_______ 。
(3)反应达到平衡时,外电路导线中_______ (填“有”或“无”)电流通过。
(4)平衡后向FeCl3溶液中加入少量FeCl2固体,当固体全部溶解后,此时该溶液中的电极为_______ (填“正”或“负”)极。
(1)画出设计的原电池装置图,并标出电极材料、电极名称及电解质溶液。
(3)反应达到平衡时,外电路导线中
(4)平衡后向FeCl3溶液中加入少量FeCl2固体,当固体全部溶解后,此时该溶液中的电极为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】相对分子质量为44的烷烃和O2气在KOH溶液中可以组成燃料电池,装置如图所示。在石墨1极上发生的电极反应为O2 +2e-+2 H2O= 4OH-
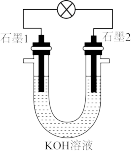
(1)石墨1极为_______ (填“负”或“正”)极。在石墨2极上发生的电极反应为_______
(2)放电时,电子流向是_______ (填字母)。
a.由石墨1极流出,经外电路流向石墨2极
b.由石墨2极流出,经电解质溶液流向石墨1极
c.由石墨1极流出,经电解质溶液流向石墨2极
d.由石墨2极流出,经外电路流向石墨1极

(1)石墨1极为
(2)放电时,电子流向是
a.由石墨1极流出,经外电路流向石墨2极
b.由石墨2极流出,经电解质溶液流向石墨1极
c.由石墨1极流出,经电解质溶液流向石墨2极
d.由石墨2极流出,经外电路流向石墨1极
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】观察“简易氢氧燃料电池的实验”思考完成以下问题:
①简易氢氧燃料电池是如何将化学能转化成电能的?
②组装电池需要满足哪些基本条件?
氢氧燃料电池中发生的反应为:_______ 。氢分子中的氢原子在石墨电极上_______ 电子,氢气作为电池的_______ ;氧气分子中的氧原子在石墨电极上_______ 电子,氧气作为电池的_______ ;稀硫酸中存在的自由移动的离子起到_______ 的作用,导线起到_______ 的作用。简易氢氧燃料电池能够给用电器提供电势差,是由于在两个石墨电极上有_______ 不同的物质-氢气和氧气。
①简易氢氧燃料电池是如何将化学能转化成电能的?
②组装电池需要满足哪些基本条件?
氢氧燃料电池中发生的反应为:
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】电池是人类生产和生活中的重要能量来源。人们应用原电池原理制作了多种电池以满足不同的需要。在现代生活、生产和科学技术发展中,电池发挥着越来越重要的作用。
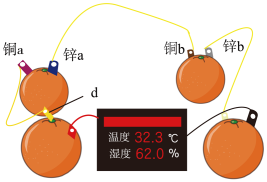
(1)知识源于实践。学习原电池知识后,某学习小组以 和
和 为电极材料,制作了如图所示的水果电池(水果果汁中含游离的
为电极材料,制作了如图所示的水果电池(水果果汁中含游离的 )。该组电池放电时,下列说法正确的是_______(填字母)。
)。该组电池放电时,下列说法正确的是_______(填字母)。
(2)生活中利用原电池原理生产了各种各样的电池,下列有关电池的叙述正确的是_______(填字母)。
(3)将 设计成燃料电池,共利用率更高,装置如图所示(
设计成燃料电池,共利用率更高,装置如图所示( 、
、 为多孔碳棒)
为多孔碳棒)
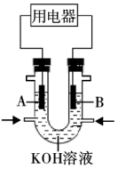
实验测得电子定向移向 电极,则
电极,则_______ (填“ ”或“
”或“ ”)电极入口通甲烷,其电极反应式为
”)电极入口通甲烷,其电极反应式为_______ 。
(4)高铁电池是一种新型可充电电池,与普通电池相比,该电池能较长时间保持稳定的放电电压。高铁电池的总反应式为: ,请回答下列问题:
,请回答下列问题:
①放电时,正极反应式为_______ 。
②放电时,负极附近溶液的碱性_______ 。(填“增强”或“减弱”)
(5) 与
与 反应还可制备
反应还可制备 ,
, 可作为燃料使用,用
可作为燃料使用,用 和
和 组合形成的质子交换膜燃料电池的结构示意图如图:
组合形成的质子交换膜燃料电池的结构示意图如图:
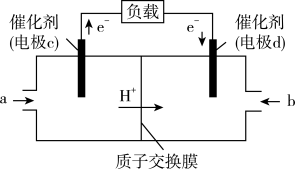
电池总反应为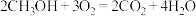 ,则
,则 电极反应式为
电极反应式为_______ ,若线路中转移 电子,则上述
电子,则上述 燃料电池,消耗的
燃料电池,消耗的 的质量为
的质量为_______  。
。
(1)知识源于实践。学习原电池知识后,某学习小组以
 和
和 为电极材料,制作了如图所示的水果电池(水果果汁中含游离的
为电极材料,制作了如图所示的水果电池(水果果汁中含游离的 )。该组电池放电时,下列说法正确的是_______(填字母)。
)。该组电池放电时,下列说法正确的是_______(填字母)。
A.每个水果果汁中的 移向正极 移向正极 |
B.锌 、 、 发生的电极反应式为 发生的电极反应式为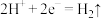 |
C.四个水果电池串联,则电极 为铜片 为铜片 |
D.铜 为电池正极,发生氧化反应 为电池正极,发生氧化反应 |
| A.锌锰电池工作一段时间后碳棒会变细 |
| B.氢氧燃料电池具有高效的特点,能量转化率可达100% |
| C.太阳能电池的主要材料是高纯度的二氧化硅 |
D.铅蓄电池负极是 ,正极是 ,正极是 |
 设计成燃料电池,共利用率更高,装置如图所示(
设计成燃料电池,共利用率更高,装置如图所示( 、
、 为多孔碳棒)
为多孔碳棒)
实验测得电子定向移向
 电极,则
电极,则 ”或“
”或“ ”)电极入口通甲烷,其电极反应式为
”)电极入口通甲烷,其电极反应式为(4)高铁电池是一种新型可充电电池,与普通电池相比,该电池能较长时间保持稳定的放电电压。高铁电池的总反应式为:
 ,请回答下列问题:
,请回答下列问题:①放电时,正极反应式为
②放电时,负极附近溶液的碱性
(5)
 与
与 反应还可制备
反应还可制备 ,
, 可作为燃料使用,用
可作为燃料使用,用 和
和 组合形成的质子交换膜燃料电池的结构示意图如图:
组合形成的质子交换膜燃料电池的结构示意图如图:
电池总反应为
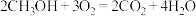 ,则
,则 电极反应式为
电极反应式为 电子,则上述
电子,则上述 燃料电池,消耗的
燃料电池,消耗的 的质量为
的质量为 。
。
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】现代社会应用最广泛的能源之一
(1)某原电池装置如图所示:
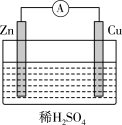
①其中,Zn电极为原电池的____ 极,电极反应式是_________________ 。
②Cu电极上发生的反应属于______ (填“氧化”或“还原”)反应,当铜表面析出4.48 L氢气(标准状况)时,导线中通过了______ mol电子。
(2)依据氧化还原反应:2Ag+(aq)+Cu(s)=Cu2+(aq)+2Ag(s)设计的原电池如图所示:

请回答下列问题:
①电极X的材料是______ ; 正极上发生的电极反应式为____________ ;
②当导线中通过了0.1mol电子时,银棒增重______ g
(1)某原电池装置如图所示:

①其中,Zn电极为原电池的
②Cu电极上发生的反应属于
(2)依据氧化还原反应:2Ag+(aq)+Cu(s)=Cu2+(aq)+2Ag(s)设计的原电池如图所示:

请回答下列问题:
①电极X的材料是
②当导线中通过了0.1mol电子时,银棒增重
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】利用反应Cu+2Ag+=2Ag+Cu2+设计一个化学电池(正极材料用碳棒)。
(1)请设计并画出原电池装置图:_______
(2)该电池的负极发生___________ 反应,电极反应式为___________ ;
(3)正极上出现的现象是___________ ;
(4)若导线上转移电子1mol,则生成银的质量为___________ 。
(5)在外电路中,电子从___________ 极流向___________ 极。
(1)请设计并画出原电池装置图:
(2)该电池的负极发生
(3)正极上出现的现象是
(4)若导线上转移电子1mol,则生成银的质量为
(5)在外电路中,电子从
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】氢气是未来理想的能源,最近科学家研究出利用太阳能产生激光,在二氧化钛( )表面作用使海水分解得到氢气的新技术:
)表面作用使海水分解得到氢气的新技术: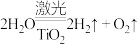 。制得的氢气可用供燃料电池使用。请回答下列问题:
。制得的氢气可用供燃料电池使用。请回答下列问题:
(1)太阳光分解海水时,实现了_______ 能转变为_______ 能。生成的氢气用于燃料电池时,实现了_______ 能转变为_______ 能。分解海水的反应属于_______ (填“放热”或“吸热”)反应。
(2)某种氢燃料电池是用固体金属氧化物陶瓷作电解质,电池工作时两极上发生的电极反应分别为:
 极:
极:
 极:
极:
则 极是电池的
极是电池的_______ 极(填“正”或“负”),发生_______ (填“氧化”或“还原”)反应;电子从该极_______ (填“流入”或“流出”)电池。
 )表面作用使海水分解得到氢气的新技术:
)表面作用使海水分解得到氢气的新技术: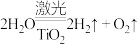 。制得的氢气可用供燃料电池使用。请回答下列问题:
。制得的氢气可用供燃料电池使用。请回答下列问题:(1)太阳光分解海水时,实现了
(2)某种氢燃料电池是用固体金属氧化物陶瓷作电解质,电池工作时两极上发生的电极反应分别为:
 极:
极:
 极:
极:
则
 极是电池的
极是电池的
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】Li-SOCl2电池可用于心脏起搏器。该电池的电极材料分别为锂和碳,电解液是LiAlCl4-SOCl2。电池的总反应可表示为4Li+2SOCl2=4LiCl+S+SO2。请回答下列问题:
(1)电池的负极材料为_____ ,发生的电极反应为______________ 。
(2)电池正极发生的电极反应为_______________ 。
(1)电池的负极材料为
(2)电池正极发生的电极反应为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】化学电源在日常生活中有着广泛的应用。
(1)将石墨和铜片用导线及电流计相连浸入500mLFeCl3溶液中,构成如图1所示的原电池装置,正极发生的电极反应式为______ ;该电池在工作时,Cu的质量将______ (填“增加”、“减少”或“不变”)。

(2)如图2是甲烷燃料电池的原理示意图:

①电池的正极反应式为______ 。
②电池工作一段时间后,电解质溶液的pH_____ (填“增大”、“减小”或“不变”)。
(3)研究人员发明了一种“水”电池,这种电池能利用淡水与海水之间含盐量的差别进行发电,电池的总反应方程式为5MnO2+2Ag+2NaCl=Na2Mn5O10+2AgCl。
①该电池负极的电极反应式为______ 。
②电池中,Na+不断移动到“水”电池的_______ 极(填“正”或“负”)。
③外电路每通过4mol电子时,生成Na2Mn5O10的物质的量是______ mol。
(1)将石墨和铜片用导线及电流计相连浸入500mLFeCl3溶液中,构成如图1所示的原电池装置,正极发生的电极反应式为

(2)如图2是甲烷燃料电池的原理示意图:

①电池的正极反应式为
②电池工作一段时间后,电解质溶液的pH
(3)研究人员发明了一种“水”电池,这种电池能利用淡水与海水之间含盐量的差别进行发电,电池的总反应方程式为5MnO2+2Ag+2NaCl=Na2Mn5O10+2AgCl。
①该电池负极的电极反应式为
②电池中,Na+不断移动到“水”电池的
③外电路每通过4mol电子时,生成Na2Mn5O10的物质的量是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】已知:2H2+O2 2H2O。
2H2O。
(1)该反应1g氢气完全燃烧放出热量121.6kJ,其中断裂1molH-H键吸收436kJ,断裂1molO=O键吸收496kJ,那么形成1molH-O键放出热量___________ 。
(2)原电池是直接把化学能转化为电能的装置。如图为原电池装置示意图:

①若A、B均为铂片,电解质为氢氧化钠溶液,分别从A、B两极通入H2和O2,该电池即为燃料电池,写出通入氢气的一极的电极反应式为:___________ 。
②如把H2改为甲烷,则负极反应式为:_______ ,该甲烷燃料电池总反应的离子方程式为:________ 。
③已知N2H4(g)-空气燃料电池,电解质溶液为KOH溶液,则负极的电极反应式为_______ ;若导线中转移电子2mol,则标况下,正极消耗的O2为_______ L
 2H2O。
2H2O。(1)该反应1g氢气完全燃烧放出热量121.6kJ,其中断裂1molH-H键吸收436kJ,断裂1molO=O键吸收496kJ,那么形成1molH-O键放出热量
(2)原电池是直接把化学能转化为电能的装置。如图为原电池装置示意图:

①若A、B均为铂片,电解质为氢氧化钠溶液,分别从A、B两极通入H2和O2,该电池即为燃料电池,写出通入氢气的一极的电极反应式为:
②如把H2改为甲烷,则负极反应式为:
③已知N2H4(g)-空气燃料电池,电解质溶液为KOH溶液,则负极的电极反应式为
您最近一年使用:0次



