新型化学电源在生活、工业、国防等方面有广泛用途。
(1)Li/CFx一次电池的工作原理如图所示:
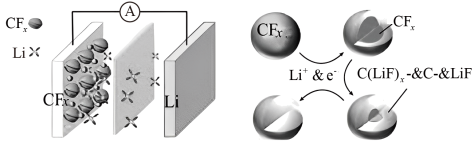
①该电池的正极反应式为_______ :
②若放电前两电极质量相等,当转移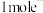 时,两电极质量差为
时,两电极质量差为_______ g。
(2)下图是铝-硫二次电池工作原理示意图,放电时的电池反应为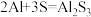 。
。
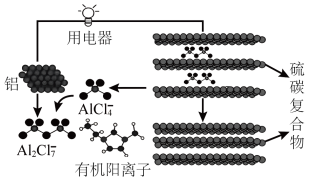
①放电时每生成 ,转移电子的物质的量为
,转移电子的物质的量为_______  ;
;
②充电时阳极电极反应式为_______ ;
③用该电池保护地下铁管道不被腐蚀,铁管道应连接电池的_______ 电极(填“铝”或“硫碳复合物”)。
(3)用固态碳燃料电池电解饱和食盐水的装置如下图所示。
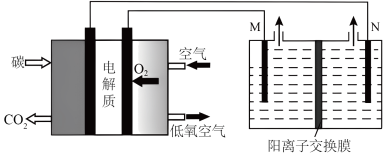
①电极M是_______ 极,N极区的产物为_______ (用化学式表示);
②已知电解前M极区溶液的浓度为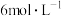 ,体积为200mL。当消耗标准状况下1.12LO2时,M极区溶液的浓度变为
,体积为200mL。当消耗标准状况下1.12LO2时,M极区溶液的浓度变为_______  。(电解前后溶液体积变化忽略不计)
。(电解前后溶液体积变化忽略不计)
(1)Li/CFx一次电池的工作原理如图所示:

①该电池的正极反应式为
②若放电前两电极质量相等,当转移
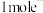 时,两电极质量差为
时,两电极质量差为(2)下图是铝-硫二次电池工作原理示意图,放电时的电池反应为
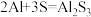 。
。
①放电时每生成
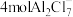 ,转移电子的物质的量为
,转移电子的物质的量为 ;
;②充电时阳极电极反应式为
③用该电池保护地下铁管道不被腐蚀,铁管道应连接电池的
(3)用固态碳燃料电池电解饱和食盐水的装置如下图所示。

①电极M是
②已知电解前M极区溶液的浓度为
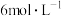 ,体积为200mL。当消耗标准状况下1.12LO2时,M极区溶液的浓度变为
,体积为200mL。当消耗标准状况下1.12LO2时,M极区溶液的浓度变为 。(电解前后溶液体积变化忽略不计)
。(电解前后溶液体积变化忽略不计)
更新时间:2023-07-11 14:40:53
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】电化学原理在生产、生活、科学研究中有重要的应用。
(1)生活中常用的碱性锌锰电池放电的总反应可用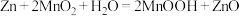 表示,该电池的正极反应式为
表示,该电池的正极反应式为_______ 。该电池每消耗13gZn时,理论上外电路转移电子的物质的量为_______ 。
(2)科学家研制的某种新型锂离子电池放电时正极材料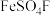 转化为
转化为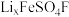 ,则充电时该电极的反应式为
,则充电时该电极的反应式为_______ 。
(3)一种冶炼铜的方法是在常温,常压下用溶剂溶浸矿石,浸出液经过萃取使铜和其他杂质金属分离,然后用电积法将溶液中的铜提取出来。铜电积的原理如图所示。该装置工作时,M电极应与直流电源的_______ 极(填“正”或“负”)相连,铜板上的电极反应式为_______ 。电解时溶液中的
_______ (填“减小”“增大”或“不变”)。

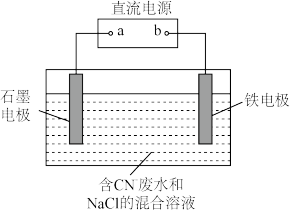
(4)工业上在强碱性条件下用电解法除去废水中的 ,将其转化成无聀物质。电解装置的工作原理如图所示,阳极附近发生的反应依次有:
,将其转化成无聀物质。电解装置的工作原理如图所示,阳极附近发生的反应依次有:
①
②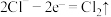
③_______ (填写离子方程式)。若将该装置的两电极材料互换,可能产生的影响是_______ 。
(1)生活中常用的碱性锌锰电池放电的总反应可用
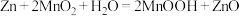 表示,该电池的正极反应式为
表示,该电池的正极反应式为(2)科学家研制的某种新型锂离子电池放电时正极材料
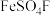 转化为
转化为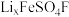 ,则充电时该电极的反应式为
,则充电时该电极的反应式为(3)一种冶炼铜的方法是在常温,常压下用溶剂溶浸矿石,浸出液经过萃取使铜和其他杂质金属分离,然后用电积法将溶液中的铜提取出来。铜电积的原理如图所示。该装置工作时,M电极应与直流电源的


(4)工业上在强碱性条件下用电解法除去废水中的
 ,将其转化成无聀物质。电解装置的工作原理如图所示,阳极附近发生的反应依次有:
,将其转化成无聀物质。电解装置的工作原理如图所示,阳极附近发生的反应依次有:①

②
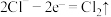
③

您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】银锌电池(纽扣电池)
(1)银锌电池的负极材料为Zn,正极是Ag2O,电解质为KOH,
(2)电极反应方程为:
负极:___________ 。
正极:___________ 。
总反应方程:___________ 。
(3)应用:适用于小电流,而持续放电型。常制成纽扣式微型电池,用于电子手表、照相机、计算器或其他用电设备。
(1)银锌电池的负极材料为Zn,正极是Ag2O,电解质为KOH,
(2)电极反应方程为:
负极:
正极:
总反应方程:
(3)应用:适用于小电流,而持续放电型。常制成纽扣式微型电池,用于电子手表、照相机、计算器或其他用电设备。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】生活中,形式多样化的电池,满足不同的市场需求。图中是几种不同类型的原电池装置。
(1)某实验小组设计了如图甲所示装置:a为铝棒,b为镁棒。
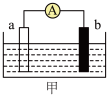
①若容器中盛有NaOH溶液,a极为_______ (填“正极”或“负极):a极的电极反应式是_______ 。
②若容器中盛有浓硫酸,b极的电极反应式是_______ ,导线中电子的流动方向是_______ (填“a→b”或“b→a”)。
(2)铅酸蓄电池常用作汽车电瓶,其构造如图乙所示,按要求回答下列问题:

①负极材料是_______ ,负极的电极反应式是_______
②工作时,电解质溶液中硫酸的浓度_______ (填“增大”“减小”或“不变”)。
③当铅酸蓄电池向外电路提供 时,理论上负极板的质量增加
时,理论上负极板的质量增加_______ g。
(3)如图丙是甲烷空气燃料电池的结构示意图。放电时甲醇应从_______ 处通入(填“a”或“b”),电池内部H+向_______ (填“左”或“右”)移动,正极的电极反应式为_______ ;若a极通入H2,请写出负极的电极反应式_______ 。

(1)某实验小组设计了如图甲所示装置:a为铝棒,b为镁棒。

①若容器中盛有NaOH溶液,a极为
②若容器中盛有浓硫酸,b极的电极反应式是
(2)铅酸蓄电池常用作汽车电瓶,其构造如图乙所示,按要求回答下列问题:

①负极材料是
②工作时,电解质溶液中硫酸的浓度
③当铅酸蓄电池向外电路提供
 时,理论上负极板的质量增加
时,理论上负极板的质量增加(3)如图丙是甲烷空气燃料电池的结构示意图。放电时甲醇应从

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】Ⅰ.根据化学能转化为电能的相关知识,回答下列问题:
(1)根据构成原电池的本质判断,下列化学(或离子)方程式正确且能设计成原电池的是___________(填字母,下同)。
Ⅱ.铅蓄电池是常用的化学电源。
(2)铅蓄电池属于___________ (填“一次”或“二次”)电池。已知硫酸铅为不溶于水的白色固体,生成时附着在电极上。写出该电池放电时,正极上的电极反应式:___________ 。
(3)甲烷(CH4)燃料电池以30%KOH溶液为电解质溶液,该燃料电池放电时负极上的电极反应式为___________ ;正极附近溶液的碱性___________ (填“增强”、“减弱”或“不变”)。
(4)银锌电池总反应为:Ag2O+Zn+H2O=Zn(OH)2+2Ag。则该电池的正极电极反应式:___________ 。
(5)如图为氢氧燃料电池的构造示意图。

①氧气从___________ (填“a”或“b”)口通入;电池工作时,OH-向___________ (填“X”或“Y”)极移动。
②某种氢氧燃料电池是用固体金属氧化物陶瓷作电解质可以传导O2-,则电池工作时负极电极反应式为___________ 。
(1)根据构成原电池的本质判断,下列化学(或离子)方程式正确且能设计成原电池的是___________(填字母,下同)。
A.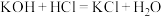 | B. |
C.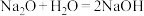 | D. |
Ⅱ.铅蓄电池是常用的化学电源。
(2)铅蓄电池属于
(3)甲烷(CH4)燃料电池以30%KOH溶液为电解质溶液,该燃料电池放电时负极上的电极反应式为
(4)银锌电池总反应为:Ag2O+Zn+H2O=Zn(OH)2+2Ag。则该电池的正极电极反应式:
(5)如图为氢氧燃料电池的构造示意图。

①氧气从
②某种氢氧燃料电池是用固体金属氧化物陶瓷作电解质可以传导O2-,则电池工作时负极电极反应式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】能源、资源问题是当前人类社会面临的一项重大课题。直接利用物质燃烧提供热能在当今社会仍然占很大比重,但存在利用率低的问题,燃料电池将能量转化效率比直接燃烧效率高,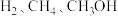 都是重要的能源物质。
都是重要的能源物质。
(1)其中氢氧燃料电池是常见的燃料电池,如图1为氢氧燃料电池的工作原理示意图,a、b均为惰性电极。___________ 口通入(填“A”或“B”);负极是___________ (填“a”或“b”)。电流由___________ 流向___________ (填“a”或“b”)。在碱性条件下,负极反应式为___________ 。
②假设使用的“燃料”是甲烷(酸性条件下),a极的电极反应为:___________ 。
(2)某同学设计如图2的原电池,正极实验现象为___________ ,则负极的电极反应式为:___________ ,当导线中有 个电子流过,溶液质量变化为
个电子流过,溶液质量变化为___________ g。_______ (填 或
或 ),负极的电极反应式为:
),负极的电极反应式为:_______ 。
 都是重要的能源物质。
都是重要的能源物质。(1)其中氢氧燃料电池是常见的燃料电池,如图1为氢氧燃料电池的工作原理示意图,a、b均为惰性电极。
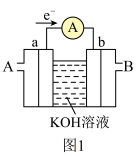
②假设使用的“燃料”是甲烷(酸性条件下),a极的电极反应为:
(2)某同学设计如图2的原电池,正极实验现象为
 个电子流过,溶液质量变化为
个电子流过,溶液质量变化为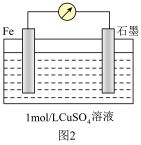
 或
或 ),负极的电极反应式为:
),负极的电极反应式为: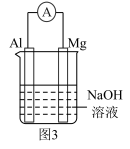
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】研究CO和 的应用对构建生态文明型社会具有重要意义。
的应用对构建生态文明型社会具有重要意义。
(1)用CO和 为原料可制取甲醇:
为原料可制取甲醇:
 。恒温时,向如图所示的密闭容器中(活栓已经固定住活塞)充入一定量的CO和
。恒温时,向如图所示的密闭容器中(活栓已经固定住活塞)充入一定量的CO和 。
。
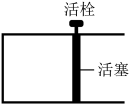
①能够说明反应已经处于平衡状态的是:_________ 。
A.容器内CO的物质的量浓度不变
B.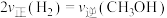
C.容器内气体压强不变
D.混合气体的密度不变
E.容器内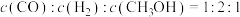
②若其他条件均保持不变,起始时拔去活栓,让活塞自由移动,则平衡时 的体积百分含量将
的体积百分含量将_________ (填“增大”、“减少”或“不变”)
(2)二氧化碳是潜在的碳资源,可以与 合成二甲醚(化学式为
合成二甲醚(化学式为 ),也可以与
),也可以与 直接转化为乙酸。
直接转化为乙酸。
①一种“二甲醚燃料电池”的结构如图所示,以熔融的碳酸钾为电解质,总反应为: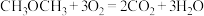 。该电池工作时,负极的电极反应为
。该电池工作时,负极的电极反应为_________ 。

②以二氧化钛表面覆盖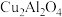 为催化剂,可以将
为催化剂,可以将 和
和 直接转化为乙酸。在不同温度下乙酸的生成速率如图所示。在250~300℃时,温度升高而乙酸的生成速率快速降低,原因可能是:
直接转化为乙酸。在不同温度下乙酸的生成速率如图所示。在250~300℃时,温度升高而乙酸的生成速率快速降低,原因可能是:_________ 。

 的应用对构建生态文明型社会具有重要意义。
的应用对构建生态文明型社会具有重要意义。(1)用CO和
 为原料可制取甲醇:
为原料可制取甲醇:
 。恒温时,向如图所示的密闭容器中(活栓已经固定住活塞)充入一定量的CO和
。恒温时,向如图所示的密闭容器中(活栓已经固定住活塞)充入一定量的CO和 。
。
①能够说明反应已经处于平衡状态的是:
A.容器内CO的物质的量浓度不变
B.
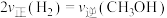
C.容器内气体压强不变
D.混合气体的密度不变
E.容器内
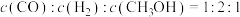
②若其他条件均保持不变,起始时拔去活栓,让活塞自由移动,则平衡时
 的体积百分含量将
的体积百分含量将(2)二氧化碳是潜在的碳资源,可以与
 合成二甲醚(化学式为
合成二甲醚(化学式为 ),也可以与
),也可以与 直接转化为乙酸。
直接转化为乙酸。①一种“二甲醚燃料电池”的结构如图所示,以熔融的碳酸钾为电解质,总反应为:
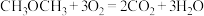 。该电池工作时,负极的电极反应为
。该电池工作时,负极的电极反应为
②以二氧化钛表面覆盖
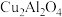 为催化剂,可以将
为催化剂,可以将 和
和 直接转化为乙酸。在不同温度下乙酸的生成速率如图所示。在250~300℃时,温度升高而乙酸的生成速率快速降低,原因可能是:
直接转化为乙酸。在不同温度下乙酸的生成速率如图所示。在250~300℃时,温度升高而乙酸的生成速率快速降低,原因可能是:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】回答下列问题:
(1)我国某科研团队设计了一种电解装置,将CO2和NaCl高效转化为CO和NaClO,原理如图1所示:

通入CO2气体的一极为___________ (填“阴极”、“阳极”、“正极”或“负极”),写出该极的电极反应式:___________ 。
(2)全钒液流电池是利用不同价态的含钒离子在酸性条件下发生反应,其电池结构如图2所示。已知酸性溶液中钒以VO (黄色)、V2+(紫色)、VO2+(蓝色)、V3+(绿色)的形式存在。放电过程中,电池的正极反应式为
(黄色)、V2+(紫色)、VO2+(蓝色)、V3+(绿色)的形式存在。放电过程中,电池的正极反应式为___________ ,右侧储液罐中溶液颜色变化为___________ 。
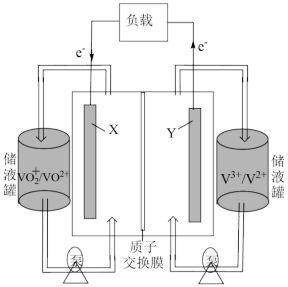
(3)如果用全钒液流电池作为图1电解装置的电源,则催化电极b应与该电池的___________ 极(填“X’或“Y’)相连;若电解时电路中转移0.4mol电子,则理论上生成NaClO的质量为___________ g;
(1)我国某科研团队设计了一种电解装置,将CO2和NaCl高效转化为CO和NaClO,原理如图1所示:

通入CO2气体的一极为
(2)全钒液流电池是利用不同价态的含钒离子在酸性条件下发生反应,其电池结构如图2所示。已知酸性溶液中钒以VO
 (黄色)、V2+(紫色)、VO2+(蓝色)、V3+(绿色)的形式存在。放电过程中,电池的正极反应式为
(黄色)、V2+(紫色)、VO2+(蓝色)、V3+(绿色)的形式存在。放电过程中,电池的正极反应式为
(3)如果用全钒液流电池作为图1电解装置的电源,则催化电极b应与该电池的
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】研究电化学原理与应用有非常重要的意义。
(1)与普通(酸性)锌锰电池相比较,碱性锌锰电池的优点是_______ (回答一条即可)。
(2)铅蓄电池是最常见的二次电池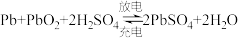 。
。
①充电时阴极反应为_______ 。
②用铅蓄电池为电源进行电解饱和食盐水实验(石墨棒为阳极,铁为阴极,食盐水500mL,温度为常温),当电路中有0.05mol电子转移时,食盐水的pH为_______ (假设溶液体积不变,产物无损耗)。
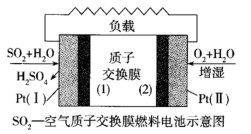
(3)二氧化硫—空气质子交换膜燃料电池实现了制硫酸发电、环保三位一体的结合,原理如图所示。Pt(II)上的电极反应式_______ 。
(4)高铁酸钠( )易溶于水,是一种新型多功能水处理剂,可以用电解法制取,离子反应为
)易溶于水,是一种新型多功能水处理剂,可以用电解法制取,离子反应为 ,工作原理如图所示。
,工作原理如图所示。
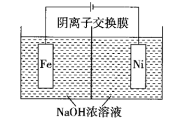
装置通电后,铁电极附近生成紫红色的 ,镍电极有气泡产生。电解一段时间后,
,镍电极有气泡产生。电解一段时间后, 降低的区域在
降低的区域在_______ (填“阴极室”或“阳极室”);铁电极发生的反应为_______ 。
(1)与普通(酸性)锌锰电池相比较,碱性锌锰电池的优点是
(2)铅蓄电池是最常见的二次电池
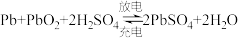 。
。①充电时阴极反应为
②用铅蓄电池为电源进行电解饱和食盐水实验(石墨棒为阳极,铁为阴极,食盐水500mL,温度为常温),当电路中有0.05mol电子转移时,食盐水的pH为
(3)二氧化硫—空气质子交换膜燃料电池实现了制硫酸发电、环保三位一体的结合,原理如图所示。Pt(II)上的电极反应式

(4)高铁酸钠(
 )易溶于水,是一种新型多功能水处理剂,可以用电解法制取,离子反应为
)易溶于水,是一种新型多功能水处理剂,可以用电解法制取,离子反应为 ,工作原理如图所示。
,工作原理如图所示。
装置通电后,铁电极附近生成紫红色的
 ,镍电极有气泡产生。电解一段时间后,
,镍电极有气泡产生。电解一段时间后, 降低的区域在
降低的区域在
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】化学电池在通讯、交通及日常生活中有着广泛的应用。
(1)如图是锌锰干电池的基本构造图。
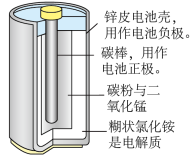
①该干电池工作时负极上的电极反应式是_______________ MnO2的作用是除去正极上的产物H2,本身生成Mn2O3,该反应的化学方程式是______________ 。
②关于该电池的使用和性能,说法正确的是( )
A.该电池可充电后反复使用
B.该电池可用于闹钟、收音机、照相机等
C.该电池使用后能投入火中,也可投入池塘中
D.外电路中每通过0.2mol电子,负极的质量理论上减小6.5g
(2)目前常用的镍(Ni)镉(Cd)电池,其电池总反应可表示为: Cd +2NiO(OH)+2H2O 2Ni(OH)2+Cd(OH)2,已知Ni(OH)2和Cd(OH)2均难于溶水但能溶于酸,以下说法正确的是
2Ni(OH)2+Cd(OH)2,已知Ni(OH)2和Cd(OH)2均难于溶水但能溶于酸,以下说法正确的是 ( )
A .以上反应是可逆反应 B.以上反应不是可逆反应
C. 电池放电时Cd 做负极 D. 电池放电时Cd 做正极
(3)废弃的镍镉电池已成为重要的环境污染物,有资料表明一节废镍镉电池可以使一平方米的耕地失去使用价值。在酸性土壤中这种污染更为严重这是因为___________ 。
(4)另一种常用的电池锂电池由于比容量(单位质量电极材料所能转换的电量)特别大而广泛用于心脏起搏器,一般使用时间可长达十年,它的负极材料用金属锂制成,电解质溶液需用非水溶液配制,请用化学方程式表示不能用水溶液的原因___________ 。
(1)如图是锌锰干电池的基本构造图。

①该干电池工作时负极上的电极反应式是
②关于该电池的使用和性能,说法正确的是
A.该电池可充电后反复使用
B.该电池可用于闹钟、收音机、照相机等
C.该电池使用后能投入火中,也可投入池塘中
D.外电路中每通过0.2mol电子,负极的质量理论上减小6.5g
(2)目前常用的镍(Ni)镉(Cd)电池,其电池总反应可表示为: Cd +2NiO(OH)+2H2O
 2Ni(OH)2+Cd(OH)2,已知Ni(OH)2和Cd(OH)2均难于溶水但能溶于酸,以下说法正确的是
2Ni(OH)2+Cd(OH)2,已知Ni(OH)2和Cd(OH)2均难于溶水但能溶于酸,以下说法正确的是 A .以上反应是可逆反应 B.以上反应不是可逆反应
C. 电池放电时Cd 做负极 D. 电池放电时Cd 做正极
(3)废弃的镍镉电池已成为重要的环境污染物,有资料表明一节废镍镉电池可以使一平方米的耕地失去使用价值。在酸性土壤中这种污染更为严重这是因为
(4)另一种常用的电池锂电池由于比容量(单位质量电极材料所能转换的电量)特别大而广泛用于心脏起搏器,一般使用时间可长达十年,它的负极材料用金属锂制成,电解质溶液需用非水溶液配制,请用化学方程式表示不能用水溶液的原因
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】铅蓄电池是常用的化学电源,其电极材料分别是Pb和PbO2,电解液为稀硫酸。该电池总反应为:Pb+PbO2+2H2SO4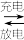 2PbSO4+2H2O。请根据上述情况判断:
2PbSO4+2H2O。请根据上述情况判断:
(1)该蓄电池的负极材料是________ ,放电时发生_______ (填“氧化”或“还原”)反应。
(2)该蓄电池放电时,电解质溶液的酸性_________ (填“增大”“减小”或“不变”)。
(3)已知硫酸铅为不溶于水的白色固体,生成时附着在电极上。试写出该电池放电时,正极的电极反应:__________________________________ (用离子方程式表示)。
(4)铅的电解精炼是工业上实现废铅回收以及粗铅提纯的重要手段。铅的电解精炼在由PbSiF6和H2SiF6两种强电解质组成的水溶液中进行。从还原炉中产出的某粗铅成分如下表所示:
①电解精炼时阳极泥的主要成分是_______ (填元素符号)。
②电解过程中,粗铅表面会生成SiF6气体,写出该电极反应式:_________________________ 。
 2PbSO4+2H2O。请根据上述情况判断:
2PbSO4+2H2O。请根据上述情况判断:(1)该蓄电池的负极材料是
(2)该蓄电池放电时,电解质溶液的酸性
(3)已知硫酸铅为不溶于水的白色固体,生成时附着在电极上。试写出该电池放电时,正极的电极反应:
(4)铅的电解精炼是工业上实现废铅回收以及粗铅提纯的重要手段。铅的电解精炼在由PbSiF6和H2SiF6两种强电解质组成的水溶液中进行。从还原炉中产出的某粗铅成分如下表所示:
| 成分 | Pb | Cu | Ag | Fe | Zn | Sn | 其它 |
| 质量分数% | 97.50 | 1.22 | 0.12 | 0.15 | 0.09 | 0.64 | 0.28 |
①电解精炼时阳极泥的主要成分是
②电解过程中,粗铅表面会生成SiF6气体,写出该电极反应式:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】对金属制品进行抗腐蚀处理,可延长其使用寿命。
(1)以下为铝材表面处理的一种方法。

①碱洗的目的是除去铝材表面的自然氧化膜,碱洗时常有气泡冒出,原因是__________ (用离子方程式表示)。为将碱洗槽液中的铝以沉淀形式回收,最好向槽液中加入(或通入)下列试剂中的______ 。
a. b.
b. c. NaOH溶液 d.硝酸
c. NaOH溶液 d.硝酸
②以铝材为阳极,在H2SO4溶液中电解,铝材表面形成氧化膜,阳极电极反应式为________ 。
(2)镀铜可防止铁制品腐蚀,电镀时用铜而不用石墨作阳极的原因是__________ 。
(3)用铝制饭盒盛放醋酸,一段时间后,饭盒被腐蚀,该种腐蚀属于__________ ,反应的化学方程式为__________ ;若用铝饭盒盛放食盐(含水)时,一段时间后,饭盒被腐蚀,这种腐蚀叫作__________ ,反应原理是__________ (写电极反应式)。
(1)以下为铝材表面处理的一种方法。

①碱洗的目的是除去铝材表面的自然氧化膜,碱洗时常有气泡冒出,原因是
a.
 b.
b. c. NaOH溶液 d.硝酸
c. NaOH溶液 d.硝酸②以铝材为阳极,在H2SO4溶液中电解,铝材表面形成氧化膜,阳极电极反应式为
(2)镀铜可防止铁制品腐蚀,电镀时用铜而不用石墨作阳极的原因是
(3)用铝制饭盒盛放醋酸,一段时间后,饭盒被腐蚀,该种腐蚀属于
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】假设图中原电池产生的电压、电流强度均能满足电解、电镀要求,即为理想化。观察下列装置,回答下列问题:
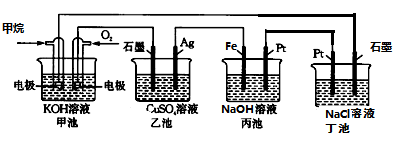
(1)甲装置中通入甲烷的电极反应式为_______________________________ ;
(2)写出丙池中Fe电极电极反应式__________________ 。
(3)丁池可以用来模拟氯碱工业原理,请写出丁池中电解总反应的离子方程式_________________________________________________________ ;假设NaCl溶液的浓度为1mol/L、体积2L,若甲池中消耗标况下5.6LO2,忽略溶液体积的变化,则电解后丁池中溶液的pH=________ (lg2=0.3)
(4)若要将乙池电解后的溶液完全恢复到电解前的浓度和pH,需要在电解后的溶液中加入0.1molCu2(OH)2CO3 ,则电路中转移的电子数为______ (用NA表示阿伏加德罗常数)。

(1)甲装置中通入甲烷的电极反应式为
(2)写出丙池中Fe电极电极反应式
(3)丁池可以用来模拟氯碱工业原理,请写出丁池中电解总反应的离子方程式
(4)若要将乙池电解后的溶液完全恢复到电解前的浓度和pH,需要在电解后的溶液中加入0.1molCu2(OH)2CO3 ,则电路中转移的电子数为
您最近一年使用:0次



