研究CO和 的应用对构建生态文明型社会具有重要意义。
的应用对构建生态文明型社会具有重要意义。
(1)用CO和 为原料可制取甲醇:
为原料可制取甲醇:
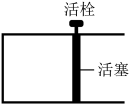
 。恒温时,向如图所示的密闭容器中(活栓已经固定住活塞)充入一定量的CO和
。恒温时,向如图所示的密闭容器中(活栓已经固定住活塞)充入一定量的CO和 。
。
①能够说明反应已经处于平衡状态的是:_________ 。
A.容器内CO的物质的量浓度不变
B.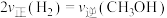
C.容器内气体压强不变
D.混合气体的密度不变
E.容器内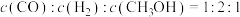
②若其他条件均保持不变,起始时拔去活栓,让活塞自由移动,则平衡时 的体积百分含量将
的体积百分含量将_________ (填“增大”、“减少”或“不变”)
(2)二氧化碳是潜在的碳资源,可以与 合成二甲醚(化学式为
合成二甲醚(化学式为 ),也可以与
),也可以与 直接转化为乙酸。
直接转化为乙酸。
①一种“二甲醚燃料电池”的结构如图所示,以熔融的碳酸钾为电解质,总反应为: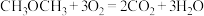 。该电池工作时,负极的电极反应为
。该电池工作时,负极的电极反应为_________ 。

②以二氧化钛表面覆盖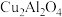 为催化剂,可以将
为催化剂,可以将 和
和 直接转化为乙酸。在不同温度下乙酸的生成速率如图所示。在250~300℃时,温度升高而乙酸的生成速率快速降低,原因可能是:
直接转化为乙酸。在不同温度下乙酸的生成速率如图所示。在250~300℃时,温度升高而乙酸的生成速率快速降低,原因可能是:_________ 。

 的应用对构建生态文明型社会具有重要意义。
的应用对构建生态文明型社会具有重要意义。(1)用CO和
 为原料可制取甲醇:
为原料可制取甲醇:
 。恒温时,向如图所示的密闭容器中(活栓已经固定住活塞)充入一定量的CO和
。恒温时,向如图所示的密闭容器中(活栓已经固定住活塞)充入一定量的CO和 。
。
①能够说明反应已经处于平衡状态的是:
A.容器内CO的物质的量浓度不变
B.
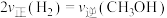
C.容器内气体压强不变
D.混合气体的密度不变
E.容器内
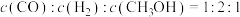
②若其他条件均保持不变,起始时拔去活栓,让活塞自由移动,则平衡时
 的体积百分含量将
的体积百分含量将(2)二氧化碳是潜在的碳资源,可以与
 合成二甲醚(化学式为
合成二甲醚(化学式为 ),也可以与
),也可以与 直接转化为乙酸。
直接转化为乙酸。①一种“二甲醚燃料电池”的结构如图所示,以熔融的碳酸钾为电解质,总反应为:
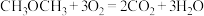 。该电池工作时,负极的电极反应为
。该电池工作时,负极的电极反应为
②以二氧化钛表面覆盖
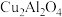 为催化剂,可以将
为催化剂,可以将 和
和 直接转化为乙酸。在不同温度下乙酸的生成速率如图所示。在250~300℃时,温度升高而乙酸的生成速率快速降低,原因可能是:
直接转化为乙酸。在不同温度下乙酸的生成速率如图所示。在250~300℃时,温度升高而乙酸的生成速率快速降低,原因可能是:
更新时间:2022-11-30 14:16:30
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】汽车尾气中含有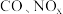 等有害气体。
等有害气体。
(1) 能形成酸雨,写出
能形成酸雨,写出 转化为
转化为 的化学方程式:
的化学方程式:______ .
(2)汽车尾气中 生成过程的能量变化示意图如下:
生成过程的能量变化示意图如下:____________ .
(3)通过NO传感器可监测汽车尾气中NO的含量,其工作原理如图所示: 电极上发生的是
电极上发生的是______ 反应(填“氧化”或“还原”)。
②外电路中,电子的流动方向是从______ 电极流出(填 或Pt);Pt电极上的电极反应式为
或Pt);Pt电极上的电极反应式为______ .
(4)一种新型催化剂能使 和
和 发生反应:
发生反应: 。已知增大催化剂的比表面积可提高该反应速率。为了验证温度、催化剂的比表面积对化学反应速率的影响规律,某同学设计了三组实验,部分实验条件已经填在下表中。
。已知增大催化剂的比表面积可提高该反应速率。为了验证温度、催化剂的比表面积对化学反应速率的影响规律,某同学设计了三组实验,部分实验条件已经填在下表中。
①请将表中数据补充完整:A______ ;B______ .
②能验证温度对化学反应速率影响规律的实验是______ (填实验编号)。
③实验Ⅰ和实验Ⅱ中,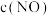 随时间
随时间 的变化曲线如图所示,其中表示实验Ⅱ的曲线是
的变化曲线如图所示,其中表示实验Ⅱ的曲线是______ (填“甲”或“乙”)。 。一定温度下,在容积不变的密闭容器中,下列可以说明该反应达到平衡状态的是
。一定温度下,在容积不变的密闭容器中,下列可以说明该反应达到平衡状态的是______ 。(从A-D项中选择)
A.容器内 的质量分数不再变化。
的质量分数不再变化。
B.相同时间内,消耗 同时生成
同时生成
C.容器内压强不再变化
D.容器内气体的平均密度不再发生变化
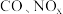 等有害气体。
等有害气体。(1)
 能形成酸雨,写出
能形成酸雨,写出 转化为
转化为 的化学方程式:
的化学方程式:(2)汽车尾气中
 生成过程的能量变化示意图如下:
生成过程的能量变化示意图如下:
(3)通过NO传感器可监测汽车尾气中NO的含量,其工作原理如图所示:

 电极上发生的是
电极上发生的是②外电路中,电子的流动方向是从
 或Pt);Pt电极上的电极反应式为
或Pt);Pt电极上的电极反应式为(4)一种新型催化剂能使
 和
和 发生反应:
发生反应: 。已知增大催化剂的比表面积可提高该反应速率。为了验证温度、催化剂的比表面积对化学反应速率的影响规律,某同学设计了三组实验,部分实验条件已经填在下表中。
。已知增大催化剂的比表面积可提高该反应速率。为了验证温度、催化剂的比表面积对化学反应速率的影响规律,某同学设计了三组实验,部分实验条件已经填在下表中。| 实验编号 | 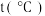 |  初始浓度 初始浓度 |  初始浓度 初始浓度 | 催化剂的比表面积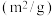 |
| Ⅰ | 280 |  |  | 82 |
| Ⅱ | 280 |  |  | 124 |
| Ⅲ | 350 |  |  | 82 |
②能验证温度对化学反应速率影响规律的实验是
③实验Ⅰ和实验Ⅱ中,
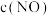 随时间
随时间 的变化曲线如图所示,其中表示实验Ⅱ的曲线是
的变化曲线如图所示,其中表示实验Ⅱ的曲线是
 。一定温度下,在容积不变的密闭容器中,下列可以说明该反应达到平衡状态的是
。一定温度下,在容积不变的密闭容器中,下列可以说明该反应达到平衡状态的是A.容器内
 的质量分数不再变化。
的质量分数不再变化。B.相同时间内,消耗
 同时生成
同时生成
C.容器内压强不再变化
D.容器内气体的平均密度不再发生变化
您最近一年使用:0次
【推荐2】“低碳经济”备受关注,CO2的有效开发利用成为科学家研究的重要课题。二氧化碳催化加氢制甲醇,有利于减少温室气体二氧化碳,反应方程式为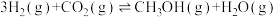 ΔH<0,一定温度下,于恒容密闭容器中充入
ΔH<0,一定温度下,于恒容密闭容器中充入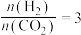 ,反应开始进行。
,反应开始进行。
(1)下列能说明该反应已经达到平衡状态的是_______(填字母代号)。
(2)上述投料在不同条件下达到平衡,设体系中甲醇的物质的量分数为x(CH3OH),在t=250℃下的x(CH3OH)~p变化曲线、在p=5×105Pa下的x(CH3OH)~t变化曲线如图所示。
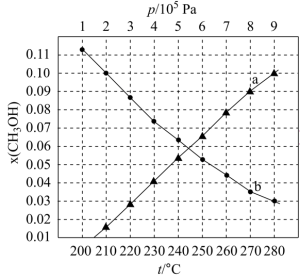
①图中对应等压过程的曲线是_______ 。
②当x(CH3OH)=0.10时,CO2的平衡转化率α=_______ ,反应条件可能为_______ 。
(3)温度为T时,向密闭恒容容器中充入3molH2和1molCO2的混合气体,此时容器内压强为4P,当CO2的转化率为50%时该反应达到平衡,则该温度下,此反应的平衡常数Kp=_______ 。(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)
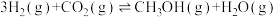 ΔH<0,一定温度下,于恒容密闭容器中充入
ΔH<0,一定温度下,于恒容密闭容器中充入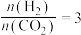 ,反应开始进行。
,反应开始进行。(1)下列能说明该反应已经达到平衡状态的是_______(填字母代号)。
| A.c(CH3OH)与c(CO2)比值不变 |
| B.容器中混合气体的密度不变 |
| C.3v正(H2)=v逆(CH3OH) |
| D.容器中混合气体的平均摩尔质量不变 |

①图中对应等压过程的曲线是
②当x(CH3OH)=0.10时,CO2的平衡转化率α=
(3)温度为T时,向密闭恒容容器中充入3molH2和1molCO2的混合气体,此时容器内压强为4P,当CO2的转化率为50%时该反应达到平衡,则该温度下,此反应的平衡常数Kp=
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】按要求回答下列问题:
(1) 一定温度下,发生反应: 2 SO2(g)+ O2 (g) 2SO3(g)(反应条件已略),现向2L密闭容器中充入4.0 mol SO2和2.0 mol O2发生反应,测得n (O2) 随时间的变化如下表:
2SO3(g)(反应条件已略),现向2L密闭容器中充入4.0 mol SO2和2.0 mol O2发生反应,测得n (O2) 随时间的变化如下表:
①0~2 min内,v(SO2)=_______________
②达到平衡时SO3的物质的量浓度为____________
③下列可证明上述反应达到平衡状态的是____________ (填序号)。
a. v(O2)=2v(SO3)
b. O2的物质的量浓度不再变化
c.每消耗1molO2,同时生成2molSO3
d.容器内压强保持不变
(2)已知可逆反应: 2NO2(g) (红棕色) N2O4(g) (无色),正反应为放热反应。将装有NO2和N2O4混合气体的烧瓶放入热水中,观察到的现象
N2O4(g) (无色),正反应为放热反应。将装有NO2和N2O4混合气体的烧瓶放入热水中,观察到的现象______________ ,产生该现象的原因是________________

(3)某温度下的密闭容器中,X、Y、Z三种气体的物质的量随时间变化曲线如图,则该反应的化学方程式为_________________
(1) 一定温度下,发生反应: 2 SO2(g)+ O2 (g)
 2SO3(g)(反应条件已略),现向2L密闭容器中充入4.0 mol SO2和2.0 mol O2发生反应,测得n (O2) 随时间的变化如下表:
2SO3(g)(反应条件已略),现向2L密闭容器中充入4.0 mol SO2和2.0 mol O2发生反应,测得n (O2) 随时间的变化如下表:| 时间/min | 1 | 2 | 3 | 4 | 5 |
| n(O2)/mol | 1.5 | 1.2 | 1.1 | 1.0 | 1.0 |
①0~2 min内,v(SO2)=
②达到平衡时SO3的物质的量浓度为
③下列可证明上述反应达到平衡状态的是
a. v(O2)=2v(SO3)
b. O2的物质的量浓度不再变化
c.每消耗1molO2,同时生成2molSO3
d.容器内压强保持不变
(2)已知可逆反应: 2NO2(g) (红棕色)
 N2O4(g) (无色),正反应为放热反应。将装有NO2和N2O4混合气体的烧瓶放入热水中,观察到的现象
N2O4(g) (无色),正反应为放热反应。将装有NO2和N2O4混合气体的烧瓶放入热水中,观察到的现象
(3)某温度下的密闭容器中,X、Y、Z三种气体的物质的量随时间变化曲线如图,则该反应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】Ⅰ.在水溶液中橙色的Cr2O72—与黄色的CrO42—有下列平衡关系:Cr2O72—+H2O 2CrO42—+2H+,重铬酸钾(K2Cr2O7)溶于水配成的稀溶液是橙黄色的。
2CrO42—+2H+,重铬酸钾(K2Cr2O7)溶于水配成的稀溶液是橙黄色的。
(1)向上述溶液中加入NaOH溶液,溶液呈________ 色,因为_________________ 。
(2)向已加入NaOH溶液的(1)溶液中再加入过量稀硫酸,则溶液呈_____ 色,因为________ 。
Ⅱ.现有浓度均为0.1 mol/L的盐酸、硫酸、醋酸三种溶液,回答下列问题:
(1)若三种溶液中c(H+)分别为x1 mol/L、x2 mol/L、x3 mol/L,则它们的大小关系为_______ 。
(2)等体积的以上三种酸分别与过量的NaOH溶液反应,消耗NaOH的物质的量依次为y1 mol、y2 mol、y3 mol,则它们的大小关系为______ 。
(3)在一定温度下,向冰醋酸中加水稀释,溶液导电能力变化情况图所示,回答下列问题。
①a、b、c三点醋酸电离程度由大到小的顺序为____ ;a、b、c三点对应的溶液中c(H+)最大的是_____ 。
②若实验测得c点处溶液中c(CH3COOH)=0.01 mol·L-1,c(CH3COO-)=0.0001 mol·L-1,则该条件下CH3COOH的电离常数Ka=____ 。
③在稀释过程中,随着醋酸浓度的降低,下列始终保持增大趋势的量是( ) 。
A.c(H+) B.溶液pH C. D. CH3COOH分子数
D. CH3COOH分子数
 2CrO42—+2H+,重铬酸钾(K2Cr2O7)溶于水配成的稀溶液是橙黄色的。
2CrO42—+2H+,重铬酸钾(K2Cr2O7)溶于水配成的稀溶液是橙黄色的。(1)向上述溶液中加入NaOH溶液,溶液呈
(2)向已加入NaOH溶液的(1)溶液中再加入过量稀硫酸,则溶液呈
Ⅱ.现有浓度均为0.1 mol/L的盐酸、硫酸、醋酸三种溶液,回答下列问题:
(1)若三种溶液中c(H+)分别为x1 mol/L、x2 mol/L、x3 mol/L,则它们的大小关系为
(2)等体积的以上三种酸分别与过量的NaOH溶液反应,消耗NaOH的物质的量依次为y1 mol、y2 mol、y3 mol,则它们的大小关系为
(3)在一定温度下,向冰醋酸中加水稀释,溶液导电能力变化情况图所示,回答下列问题。

①a、b、c三点醋酸电离程度由大到小的顺序为
②若实验测得c点处溶液中c(CH3COOH)=0.01 mol·L-1,c(CH3COO-)=0.0001 mol·L-1,则该条件下CH3COOH的电离常数Ka=
③在稀释过程中,随着醋酸浓度的降低,下列始终保持增大趋势的量是
A.c(H+) B.溶液pH C.
 D. CH3COOH分子数
D. CH3COOH分子数
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】甲醛(HCHO)在化工、医药、农药等方面有广泛的应用。利用甲醛一定条件下直接脱氢可制甲醛,反应方程式:CH3OH(g) HCHO(g)+H2(g) △H1
HCHO(g)+H2(g) △H1
实验测得随温度升高,平衡常数如下表所示。
(1)甲醛分子中所有原子都达到稳定结构,甲醛的电子式为_____________ 。
(2) 若在恒温恒压容器中进行上述反应,可判断反应到达平衡状态的是_______________ 。
A.混合气体的密度不变
B.CH3OH、HCHO的物质的量浓度之比为1:1
C.H2的体积分数不再改变
D.单位时间内甲醛的生成量与氢气的消耗量相等
(3)T1时,CH3OH、HCHO、H2 起始浓度(mol·L-1)分别为1.0、0.50 、1.0,反应达到平衡时,HCHO 的体积分数___________ 20% (填“>”、“ =”、“ <”)。
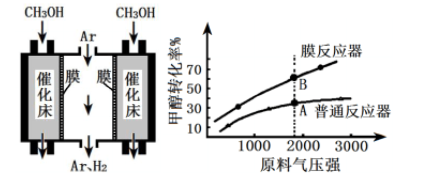
(4)工业上采用膜分离器(对氢气具有很高的选择性和透过率)催化脱氢,装置如下图。为探究转化率变化,分别在普通反应器和膜反应器中,改变原料气压强,控制相同温度,经过相同反应时间,测定甲醇转化率,实验结果如下图。
①A点:v正______ v逆(填“>”、“ =”、“ <”),理由是____________ ;
②B点比A点转化率高的原因是_______________ 。
(5)体系中加入一定量氧气有利于甲醛的生成。反应体系中存在下列反应:
CH3OH(g)+1/2O2(g) HCHO(g)+H2O(g) △H2
HCHO(g)+H2O(g) △H2
H2(g)+12O2(g) H2O(g) △H3
H2O(g) △H3
则△H2、△H3的大小关系是△H2________ △H3(填“>”、“ =”、“ <”)。
 HCHO(g)+H2(g) △H1
HCHO(g)+H2(g) △H1实验测得随温度升高,平衡常数如下表所示。
温度(K) | 500 | 700 | T1 | T2 | T3 |
平衡常数 | 7.13×10-4 | 3.30×10-1 | 2.00 | 9.00 | 10.00 |
(2) 若在恒温恒压容器中进行上述反应,可判断反应到达平衡状态的是
A.混合气体的密度不变
B.CH3OH、HCHO的物质的量浓度之比为1:1
C.H2的体积分数不再改变
D.单位时间内甲醛的生成量与氢气的消耗量相等
(3)T1时,CH3OH、HCHO、H2 起始浓度(mol·L-1)分别为1.0、0.50 、1.0,反应达到平衡时,HCHO 的体积分数
(4)工业上采用膜分离器(对氢气具有很高的选择性和透过率)催化脱氢,装置如下图。为探究转化率变化,分别在普通反应器和膜反应器中,改变原料气压强,控制相同温度,经过相同反应时间,测定甲醇转化率,实验结果如下图。
①A点:v正
②B点比A点转化率高的原因是

(5)体系中加入一定量氧气有利于甲醛的生成。反应体系中存在下列反应:
CH3OH(g)+1/2O2(g)
 HCHO(g)+H2O(g) △H2
HCHO(g)+H2O(g) △H2H2(g)+12O2(g)
 H2O(g) △H3
H2O(g) △H3则△H2、△H3的大小关系是△H2
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】合成氨工业的核心反应是:N2(g)+3H2(g)  2NH3(g) ΔH=" Q" kJ·mol-1,能量变化如图所示,回答下列问题:
2NH3(g) ΔH=" Q" kJ·mol-1,能量变化如图所示,回答下列问题:

(1)在500 ℃、2×107 Pa和催化剂条件下向一密闭容器中充入0.5 mol N2和1.5 mol H2,充分反应后,放出的热量______ 46.2kJ(填“<”、“>”或“=”)。
(2)在反应体系中加入催化剂,反应速率增大,E1和E2的变化是:E1_________ (填“增大”、“减小”、“不变”,下同); E2- E1________ 。若升高温度,平衡向______ 反应方向移动(填“正”或“逆”),E2- E1_____ (填“增大”、“减小”、“不变”) 。
(3)将一定量的N2(g)和H2(g)放入1 L密闭容器中,在500 ℃、2×107 Pa下达到平衡,测得N2为0.10 mol,H2为0.30 mol,NH3为0.10 mol。计算该条件下达到平衡时H2的转化率________ 。
(4)在上述(3)反应条件的密闭容器中欲提高合成氨中H2的转化率,下列措施可行的____ (填字母)。
 2NH3(g) ΔH=" Q" kJ·mol-1,能量变化如图所示,回答下列问题:
2NH3(g) ΔH=" Q" kJ·mol-1,能量变化如图所示,回答下列问题:
(1)在500 ℃、2×107 Pa和催化剂条件下向一密闭容器中充入0.5 mol N2和1.5 mol H2,充分反应后,放出的热量
(2)在反应体系中加入催化剂,反应速率增大,E1和E2的变化是:E1
(3)将一定量的N2(g)和H2(g)放入1 L密闭容器中,在500 ℃、2×107 Pa下达到平衡,测得N2为0.10 mol,H2为0.30 mol,NH3为0.10 mol。计算该条件下达到平衡时H2的转化率
(4)在上述(3)反应条件的密闭容器中欲提高合成氨中H2的转化率,下列措施可行的
| A.向容器中按原比例再充入原料气 | B.向容器中再充入惰性气体 |
| C.改变反应的催化剂 | D.分离出氨气 |
您最近一年使用:0次
【推荐2】一定温度下,在固定体积为2 L的容器中铁与水蒸气反应可制得氢气:3Fe(S)+4H2O(g)⇌Fe3O4(s)+4H2(g) ∆H=+64.0kJ•mol-1
(1)该反应平衡后的混合气体的质量随温度的升高而_______ (填“增大”、“减小” 、“不变”);
(2)下列叙述能作为反应达到平衡状态的标志的是_______ ;
A.该反应的∆H不变时 B.铁的质量不变时 C.当v(H2O)=v(H2)时 D.容器的压强不变时 E.混合气体的密度不变时
(3)一定温度下,在固定体积为2L的容器中进行着上述反应,若起始投料铁(s)、H2O(g)均为1mol,反应经过5min达到平衡,平衡混合气体中氢气的体积分数为50%。
①用消耗水的量来表示该反应经过5min达到平衡时的平均反应速率,v(H2O)=_______ ,
②计算该反应的平衡常数K=_______ 。
(1)该反应平衡后的混合气体的质量随温度的升高而
(2)下列叙述能作为反应达到平衡状态的标志的是
A.该反应的∆H不变时 B.铁的质量不变时 C.当v(H2O)=v(H2)时 D.容器的压强不变时 E.混合气体的密度不变时
(3)一定温度下,在固定体积为2L的容器中进行着上述反应,若起始投料铁(s)、H2O(g)均为1mol,反应经过5min达到平衡,平衡混合气体中氢气的体积分数为50%。
①用消耗水的量来表示该反应经过5min达到平衡时的平均反应速率,v(H2O)=
②计算该反应的平衡常数K=
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】Ⅰ. CH3OH是一种无色有刺激性气味的液体,在生产生活中有重要用途,同时也是一种重要的化工原料。
(1)已知CH3OH(g)+1/2O2(g) CO2(g)+2H2(g)的能量变化如图所示,下列说法正确的是
CO2(g)+2H2(g)的能量变化如图所示,下列说法正确的是______ (填字母)。
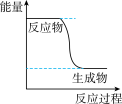
a.CH3OH转变成H2的过程是一个吸收能量的过程
b.H2的生成速率与CH3OH的消耗速率之比为1∶2
c.化学变化不仅有新物质生成,同时也一定有能量变化
d.1 mol H—O键断裂的同时2 mol C===O键断裂,则反应达最大限度
(2)某温度下,将5molCH3OH和2molO2充入2L的密闭容器中,经过4min反应达到平衡,测得c(O2)=0.2mol·L-1,4min内平均反应速率v(H2)=________________ ,则CH3OH的转化率为___________ 。
Ⅱ.在恒温条件下将一定量X和Y的混合气体通入一容积为2 L的密闭容器中,X和Y两物质的浓度随时间变化情况如下图。
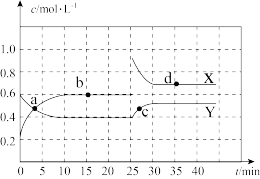
(1)该反应的化学方程式为(反应物或生成物用符号X、Y表示)______________________________ 。
(2)a、b、c、d四个点中,表示化学反应处于平衡状态的点是___________ 。
Ⅲ.当电极a为Al,电极b为Mg,电解质溶液为氢氧化钠溶液时,该电池的正极为________ ,负极的电极反应式为_______________________________ 。当反应中收集到标准状况下224 mL气体时,消耗的a电极质量为________ g。
(1)已知CH3OH(g)+1/2O2(g)
 CO2(g)+2H2(g)的能量变化如图所示,下列说法正确的是
CO2(g)+2H2(g)的能量变化如图所示,下列说法正确的是
a.CH3OH转变成H2的过程是一个吸收能量的过程
b.H2的生成速率与CH3OH的消耗速率之比为1∶2
c.化学变化不仅有新物质生成,同时也一定有能量变化
d.1 mol H—O键断裂的同时2 mol C===O键断裂,则反应达最大限度
(2)某温度下,将5molCH3OH和2molO2充入2L的密闭容器中,经过4min反应达到平衡,测得c(O2)=0.2mol·L-1,4min内平均反应速率v(H2)=
Ⅱ.在恒温条件下将一定量X和Y的混合气体通入一容积为2 L的密闭容器中,X和Y两物质的浓度随时间变化情况如下图。

(1)该反应的化学方程式为(反应物或生成物用符号X、Y表示)
(2)a、b、c、d四个点中,表示化学反应处于平衡状态的点是
Ⅲ.当电极a为Al,电极b为Mg,电解质溶液为氢氧化钠溶液时,该电池的正极为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】完成下列问题
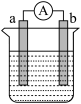
(1)如图所示,能够组成原电池(烧杯里为相应物质的溶液),并且产生明显电流的是_______ 。

(2)某化学小组探究不同条件下化学能转变为电能的装置如图所示。回答问题:若电极a为Fe、电极b为Cu、电解质溶液为稀硫酸时,正极的电极反应式是_______ 。燃料电池的工作原理是将燃料和氧化剂(如O2)反应所产生的化学能直接转化为电能,现设计一燃料电池,以电极a为正极,电极b为负极,CH4为燃料,采用酸性溶液做电解液,则CH4应通入_______ 极 (填“a”或“b”);电池的负极反应式是_______ 。
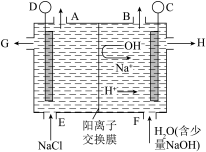
(3)工业电解饱和食盐水制烧碱时必须阻止OH- 移向阳极,目前采用阳离子交换膜将两极溶液分开(如下图所示)。F处加少量NaOH的目的是_______ ;C、D分别是直流电源的两电极,则C是电源_______ 极;若不采用阳离子交换膜,OH-向阳极移动,发生的反应可用离子方程式表示为_______ 。
(1)如图所示,能够组成原电池(烧杯里为相应物质的溶液),并且产生明显电流的是

(2)某化学小组探究不同条件下化学能转变为电能的装置如图所示。回答问题:若电极a为Fe、电极b为Cu、电解质溶液为稀硫酸时,正极的电极反应式是

(3)工业电解饱和食盐水制烧碱时必须阻止OH- 移向阳极,目前采用阳离子交换膜将两极溶液分开(如下图所示)。F处加少量NaOH的目的是

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】按下图装置进行实验,并回答下列问题:
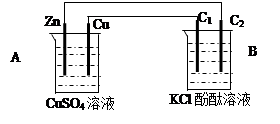
(1)判断装置的名称:A池为___________ ;B池为______________ ;
(2)锌极为________ 极,电极反应式为___________________________________ ;铜极为________ 极,电极反应式为___________________________________ ;石墨棒C1为______ 极,电极反应式为__________________________________ ;石墨棒C2附近发生的实验现象为______________________________________ ;
(3)当C2极析出224mL气体(标准状态)时,锌的质量变化_________ (变大、不变或变小)了________ g,CuSO4溶液的质量_________ (增加、不变或减少)_________ g。
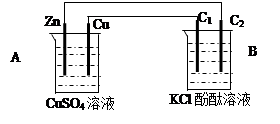
(1)判断装置的名称:A池为
(2)锌极为
(3)当C2极析出224mL气体(标准状态)时,锌的质量变化
您最近一年使用:0次

 催化,测得
催化,测得 的转化率随温度变化情况如下图所示。
的转化率随温度变化情况如下图所示。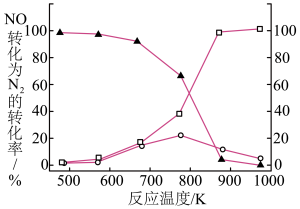
 条件下,
条件下, ,发现
,发现

