乙烯、乙醇是重要有机化工原料。回答下列问题:
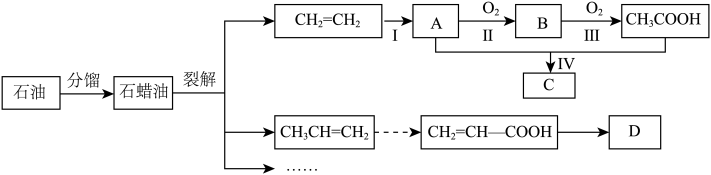
已知: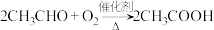
(1)石蜡油裂解产生的不饱和烃是重要的有机合成中间体。
①反应I的化学方程式是___________ 。
②D为高分子化合物,结构简式是___________ 。
③下列装置正确且能达到实验目的的是___________ (填序号)。
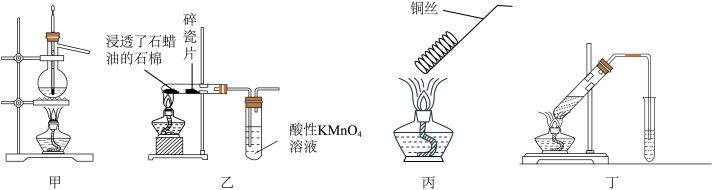
A.甲装置:从石油中分离石蜡油 B.乙装置:证明石蜡油分解生成乙烯
C.丙装置:完成乙醇的催化氧化 D.丁装置:制备乙酸乙酯
(2)已知:CaCl2与C2H5OH形成CaCl2·6C2H5OH.实验室制备乙酸乙酯粗产品并精制提纯,流程如下。
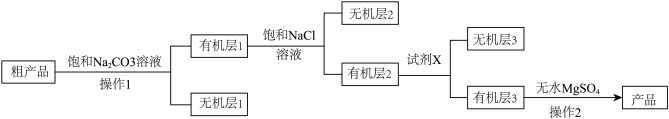
①制备乙酸乙酯的化学方程式为___________ 。
②饱和Na2CO3溶液的作用是___________ ;操作1的名称是___________ 。
③为除去有机层2中的乙醇,加入的试剂X为___________ 。
④选择合适的仪器组装完成操作2(夹持、加热及单孔、双孔橡胶塞、导管等连接仪器略),仪器的连接顺序为d→___________ 。
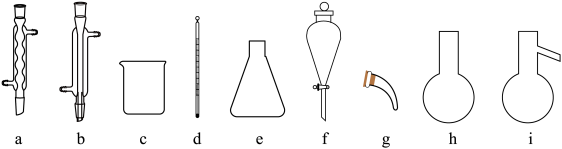

已知:
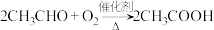
(1)石蜡油裂解产生的不饱和烃是重要的有机合成中间体。
①反应I的化学方程式是
②D为高分子化合物,结构简式是
③下列装置正确且能达到实验目的的是

A.甲装置:从石油中分离石蜡油 B.乙装置:证明石蜡油分解生成乙烯
C.丙装置:完成乙醇的催化氧化 D.丁装置:制备乙酸乙酯
(2)已知:CaCl2与C2H5OH形成CaCl2·6C2H5OH.实验室制备乙酸乙酯粗产品并精制提纯,流程如下。

①制备乙酸乙酯的化学方程式为
②饱和Na2CO3溶液的作用是
③为除去有机层2中的乙醇,加入的试剂X为
④选择合适的仪器组装完成操作2(夹持、加热及单孔、双孔橡胶塞、导管等连接仪器略),仪器的连接顺序为d→

更新时间:2023-07-12 13:33:38
|
相似题推荐
解答题-有机推断题
|
适中
(0.65)
【推荐1】I、实验室用下图所示装置制备乙酸乙酯。
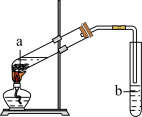
(1)试管a中生成乙酸乙酯的化学方程式是_______ 。
(2)试管a中试剂的添加顺序是先加入_______ ,再加入_______ ,最后加入乙酸。
(3)试管b中盛放的试剂是______ ,导气管不伸入液面下的理由是_______ 。
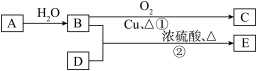
II、乳酸在生命化学中起重要作用,也是重要的化工原料。下图是获得乳酸的两种方法,其中A是一种常见的烃,它的产量可以用来衡量一个国家的石油化工发展水平。

(1)A→B的反应类型是_____ ;淀粉完全水解得到D,D的名称是________ 。
(2)B→C反应的化学方程式是________ 。
(3)乳酸在一定条件下可生成六元环酯(C6H8O4),其结构简式是________ 。

(1)试管a中生成乙酸乙酯的化学方程式是
(2)试管a中试剂的添加顺序是先加入
(3)试管b中盛放的试剂是
II、乳酸在生命化学中起重要作用,也是重要的化工原料。下图是获得乳酸的两种方法,其中A是一种常见的烃,它的产量可以用来衡量一个国家的石油化工发展水平。

(1)A→B的反应类型是
(2)B→C反应的化学方程式是
(3)乳酸在一定条件下可生成六元环酯(C6H8O4),其结构简式是
您最近半年使用:0次
解答题-有机推断题
|
适中
(0.65)
解题方法
【推荐2】某有机物X的分子式为C4H8O2,X在酸性条件下与水反应,生成分子内均含有2个碳原子的有机物Y和Z,Y在铜催化下被氧化为W,W能发生银镜反应。
(1)写出X和Z的结构简式X____________________ ,Z________________________ 。
(2)写出下列反应的化学方程式
X在酸性条件下与水反应________________________ ,反应类型为__________________ 。
Y与浓硫酸的混合物共热发生消去反应_____________________________________________ 。
W与新制Cu(OH)2反应的现象是____________________________________________ 。
(1)写出X和Z的结构简式X
(2)写出下列反应的化学方程式
X在酸性条件下与水反应
Y与浓硫酸的混合物共热发生消去反应
W与新制Cu(OH)2反应的现象是
您最近半年使用:0次
解答题-有机推断题
|
适中
(0.65)
解题方法
【推荐3】已知 的产量通常用来衡量一个国家的石油化工发展水平,
的产量通常用来衡量一个国家的石油化工发展水平, 、
、 是饮食中两种常见的有机物,
是饮食中两种常见的有机物, 是一种有香味的物质,
是一种有香味的物质, 中碳原子数是
中碳原子数是 的两倍。现以
的两倍。现以 为主要原料合成
为主要原料合成 ,其合成路线如图所示:
,其合成路线如图所示:
(1) 的结构式为
的结构式为________ 。 中官能团的名称为
中官能团的名称为________ 。
(2)写出下列反应的化学方程式。
①________________ ,反应类型:________ 。
②________________ ,反应类型:________ 。
(3)写出 与金属钠反应的化学方程式
与金属钠反应的化学方程式________________ 。
(4)实验室怎样区分 和
和 ?
?________________ 。
(5)含 的体积分数为75%的水溶液可以作
的体积分数为75%的水溶液可以作________ 。
 的产量通常用来衡量一个国家的石油化工发展水平,
的产量通常用来衡量一个国家的石油化工发展水平, 、
、 是饮食中两种常见的有机物,
是饮食中两种常见的有机物, 是一种有香味的物质,
是一种有香味的物质, 中碳原子数是
中碳原子数是 的两倍。现以
的两倍。现以 为主要原料合成
为主要原料合成 ,其合成路线如图所示:
,其合成路线如图所示:
(1)
 的结构式为
的结构式为 中官能团的名称为
中官能团的名称为(2)写出下列反应的化学方程式。
①
②
(3)写出
 与金属钠反应的化学方程式
与金属钠反应的化学方程式(4)实验室怎样区分
 和
和 ?
?(5)含
 的体积分数为75%的水溶液可以作
的体积分数为75%的水溶液可以作
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】实验室制取乙酸乙酯的主要步骤如下:
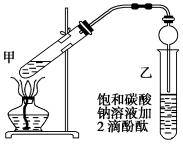
①在甲试管(如图)中加入2 mL浓硫酸、3 mL乙醇和2 mL乙酸的混合溶液。
②按图连接好装置(装置气密性良好)并加入混合液,用小火均匀地加热3~5 min。
③待试管乙收集到一定量产物后停止加热,撤出试管乙,并用力振荡,然后静置待分层。
④分离出乙酸乙酯层,洗涤、干燥。
(1)配制该混合溶液的主要操作步骤为_______ ;反应中浓硫酸的作用是_______ 。
(2)试管甲中发生反应的化学方程式为_______ 。
(3)上述实验中饱和碳酸钠溶液的作用是(填字母)_______。
(4)欲将乙试管中的物质分离开以得到乙酸乙酯,必须使用的仪器有_______ ;分离时,乙酸乙酯应该从仪器_______ (填“下口放出”或“上口倒出”)。

①在甲试管(如图)中加入2 mL浓硫酸、3 mL乙醇和2 mL乙酸的混合溶液。
②按图连接好装置(装置气密性良好)并加入混合液,用小火均匀地加热3~5 min。
③待试管乙收集到一定量产物后停止加热,撤出试管乙,并用力振荡,然后静置待分层。
④分离出乙酸乙酯层,洗涤、干燥。
(1)配制该混合溶液的主要操作步骤为
(2)试管甲中发生反应的化学方程式为
(3)上述实验中饱和碳酸钠溶液的作用是(填字母)_______。
| A.中和乙酸和乙醇 |
| B.中和乙酸并吸收部分乙醇 |
| C.乙酸乙酯在饱和碳酸钠溶液中的溶解度比在水中更小,有利于分层析出 |
| D.加速酯的生成,提高其产率 |
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】乙醇与乙酸发生酯化反应的装置如图所示,请回答下列问题:
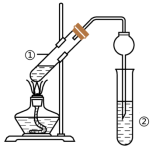
(1)实验操作:在试管里先加入3mL____ ,边振荡,边慢慢地加入2mL____ 和2mL____ 。用酒精灯小心加热试管3~5min。产生的蒸气经导管通到____ 的液面上。
(2)从试管②中分离出乙酸乙酯的方法是____ 。(填操作名称)球形干燥管,除起冷凝作用外,另一重要作用是____ 。
(3)②中的溶液的作用是_____ 。
(4)乙醇与乙酸反应的化学方程式是_____ 。
(5)乙醇与乙酸发生酯化反应,一段时间后达到了该反应的限度。下列描述能说明该反应已达到化学平衡状态的是____ (填序号)。
①混合物中各物质的浓度不再变化
②单位时间里,生成1mol乙醇,同时生成1mol乙酸
③单位时间里,生成1mol乙酸乙酯,同时生成1mol乙酸

(1)实验操作:在试管里先加入3mL
(2)从试管②中分离出乙酸乙酯的方法是
(3)②中的溶液的作用是
(4)乙醇与乙酸反应的化学方程式是
(5)乙醇与乙酸发生酯化反应,一段时间后达到了该反应的限度。下列描述能说明该反应已达到化学平衡状态的是
①混合物中各物质的浓度不再变化
②单位时间里,生成1mol乙醇,同时生成1mol乙酸
③单位时间里,生成1mol乙酸乙酯,同时生成1mol乙酸
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】某化学兴趣小组利用如图装置进行乙酸乙酯合成和分离的实验探究,请回答以下问题:
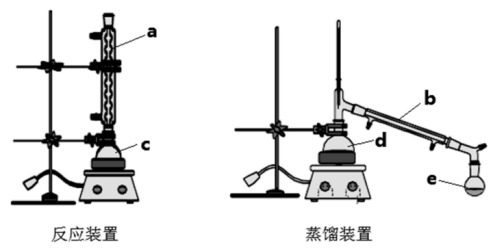
(1)仪器b的名称_______ ,图中起冷凝回流作用的是_______ (填a、b、c、d、e)。
(2)反应装置c中加入的试剂是浓硫酸、无水乙醇和_______ ,该反应是可逆反应,为了提高乙酸乙酯的产率可采取的措施_______
(3)经过0.5h加热反应后,将反应装置c中粗产品转移至d中进行蒸馏
根据表分析,蒸馏后得到的乙酸乙酯中,最有可能含有_______ 等杂质。为除去上述杂质可选择_______ 试剂,然后采用_______ (填分离方法)。

(1)仪器b的名称
(2)反应装置c中加入的试剂是浓硫酸、无水乙醇和
(3)经过0.5h加热反应后,将反应装置c中粗产品转移至d中进行蒸馏
| 物质 | 98.3%浓硫酸 | 乙酸乙酯 | 乙酸 | 乙醇 | 乙醚 | 水 |
| 沸点 | 338℃, | 77.1℃ | 118℃ | 78.5℃ | 34.6℃ | 100℃ |
您最近半年使用:0次
解答题-有机推断题
|
适中
(0.65)
解题方法
【推荐1】高聚物G是一种合成纤维,以A(邻二甲苯)与E为原料制备J和G的一种合成路线如图所示(部分生成物已略去):
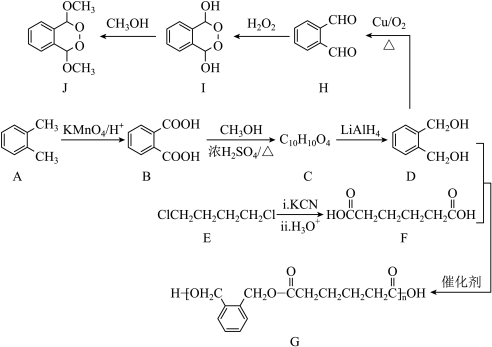
已知:化合物E的键线式为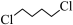 。
。
回答下列问题:
(1)A的分子式为_____ 。
(2)C的结构简式为_____ 。
(3)1molD与足量的金属钠反应最多可生成_____ 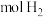 。
。
(4)D→H的化学方程式为_____ ,该反应的反应类型为_____ 。
(5)F中所含官能团的名称为_____ 。
(6)下列有关化合物I和J的说法正确的是_____ (填标号)。
a.均可发生氧化反应 b.两者互为同分异构体
c.I→J的反应类型为取代反应 d.含量最高的元素均为氧元素

已知:化合物E的键线式为
 。
。回答下列问题:
(1)A的分子式为
(2)C的结构简式为
(3)1molD与足量的金属钠反应最多可生成
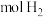 。
。(4)D→H的化学方程式为
(5)F中所含官能团的名称为
(6)下列有关化合物I和J的说法正确的是
a.均可发生氧化反应 b.两者互为同分异构体
c.I→J的反应类型为取代反应 d.含量最高的元素均为氧元素
您最近半年使用:0次
解答题-有机推断题
|
适中
(0.65)
解题方法
【推荐2】已知A的结构简式为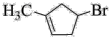 。化合物A~H的转化关系如图所示,B1和B2互为同分异构体,B1的摩尔质量80g/mol;G1和G2互为同分异构体,核磁共振氢谱显示二者均只有两种氢,G1无甲基。请完成下列问题。
。化合物A~H的转化关系如图所示,B1和B2互为同分异构体,B1的摩尔质量80g/mol;G1和G2互为同分异构体,核磁共振氢谱显示二者均只有两种氢,G1无甲基。请完成下列问题。
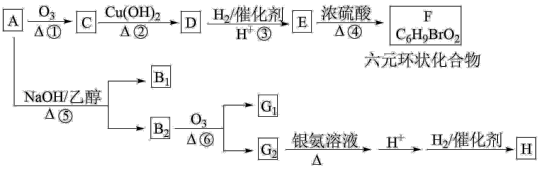
已知: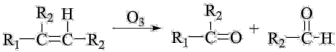
(1)B1的结构简式为___ ,G2所含官能团为___ 。
(2)⑤的反应类型是___ 。
(3)反应④的化学方程式:___ 。
(4)写出C与新制Cu(OH)2反应的方程式:___ 。
(5)一定条件下H能够生成高分子化合物,写出反应的方程式___ 。
(6)符合下列条件的E的同分异构体共有___ 种;写出其中一个的结构简式为___ 。
①含有三个甲基;②与E所含官能团相同;③-OH和-Br不连在同一个碳原子上。
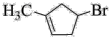 。化合物A~H的转化关系如图所示,B1和B2互为同分异构体,B1的摩尔质量80g/mol;G1和G2互为同分异构体,核磁共振氢谱显示二者均只有两种氢,G1无甲基。请完成下列问题。
。化合物A~H的转化关系如图所示,B1和B2互为同分异构体,B1的摩尔质量80g/mol;G1和G2互为同分异构体,核磁共振氢谱显示二者均只有两种氢,G1无甲基。请完成下列问题。
已知:
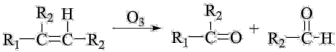
(1)B1的结构简式为
(2)⑤的反应类型是
(3)反应④的化学方程式:
(4)写出C与新制Cu(OH)2反应的方程式:
(5)一定条件下H能够生成高分子化合物,写出反应的方程式
(6)符合下列条件的E的同分异构体共有
①含有三个甲基;②与E所含官能团相同;③-OH和-Br不连在同一个碳原子上。
您最近半年使用:0次
解答题-有机推断题
|
适中
(0.65)
【推荐3】马来酸酐(顺-丁烯二酸酐) 是一种重要的化工原料,可用于合成可降解的高聚物PES树脂以及具有抗肿瘤活性的化合物K。
是一种重要的化工原料,可用于合成可降解的高聚物PES树脂以及具有抗肿瘤活性的化合物K。

已知:①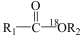 +HO-R3
+HO-R3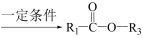 +H18O-R2
+H18O-R2
②R1OH+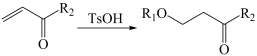
③R1NH2+ +H2O(R1、R2、R3代表烃基)
+H2O(R1、R2、R3代表烃基)
回答下列问题:
(1)C的名称是________ ,反应②的反应类型是___________ 。
(2)B的顺式结构简式为_________ ,F的结构简式为__________ 。
(3)反应①的化学方程式为_________ 。
(4)C有多种同分异构体,其中与C具有完全相同的官能团,且核磁共振氢谱只有两个峰的同分异构体的结构简式为______ (不考虑立体异构)。
(5)已知:氨基(-NH2)与羟基类似,也能发生反应①。在由F制备K的过程中,常会产生副产物L。L分子式为C16H13NO3,含三个六元环,则L的结构简式为______ 。
(6)已知:酸酐在水溶液中极易水解。写出由马来酸酐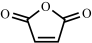 合成酒石酸
合成酒石酸 的合成路线:
的合成路线:____________________ 。
 是一种重要的化工原料,可用于合成可降解的高聚物PES树脂以及具有抗肿瘤活性的化合物K。
是一种重要的化工原料,可用于合成可降解的高聚物PES树脂以及具有抗肿瘤活性的化合物K。
已知:①
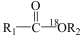 +HO-R3
+HO-R3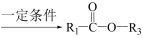 +H18O-R2
+H18O-R2②R1OH+
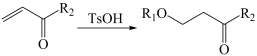
③R1NH2+
 +H2O(R1、R2、R3代表烃基)
+H2O(R1、R2、R3代表烃基)回答下列问题:
(1)C的名称是
(2)B的顺式结构简式为
(3)反应①的化学方程式为
(4)C有多种同分异构体,其中与C具有完全相同的官能团,且核磁共振氢谱只有两个峰的同分异构体的结构简式为
(5)已知:氨基(-NH2)与羟基类似,也能发生反应①。在由F制备K的过程中,常会产生副产物L。L分子式为C16H13NO3,含三个六元环,则L的结构简式为
(6)已知:酸酐在水溶液中极易水解。写出由马来酸酐
 合成酒石酸
合成酒石酸 的合成路线:
的合成路线:
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】海洋植物如海带、海藻中含有丰富的碘元素,碘元素以碘离子的形式存在。实验室里从海藻中提取碘的流程如图:
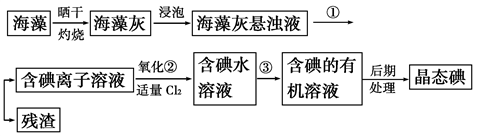
(1)指出提取碘的过程中有关的实验操作名称:
①____ ,③____ 。
(2)提取碘的过程中,可供选择的有机试剂是____ 。
A.酒精 B.四氯化碳
C.醋酸 D.苯
(3)为使海藻灰中碘离子转化为碘的有机溶液,实验室里有烧杯、玻璃棒、集气瓶、酒精灯、导管、圆底烧瓶、石棉网以及必要的夹持仪器、物品,尚缺少的玻璃仪器是____________________________ 。
(4)从含碘的有机溶液中提取碘和回收有机溶剂,还需经过蒸馏,指出下图中实验装置中的错误之处:①________________ ;②______________ ;③________________ 。
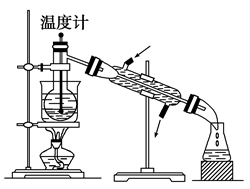

(1)指出提取碘的过程中有关的实验操作名称:
①
(2)提取碘的过程中,可供选择的有机试剂是
A.酒精 B.四氯化碳
C.醋酸 D.苯
(3)为使海藻灰中碘离子转化为碘的有机溶液,实验室里有烧杯、玻璃棒、集气瓶、酒精灯、导管、圆底烧瓶、石棉网以及必要的夹持仪器、物品,尚缺少的玻璃仪器是
(4)从含碘的有机溶液中提取碘和回收有机溶剂,还需经过蒸馏,指出下图中实验装置中的错误之处:①

您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐2】浩瀚的海洋里蕴藏着丰富的化学资源,从海带中提取碘单质和从海水中提取溴单质的工艺流程如图。回答下列问题:
I.海带提碘
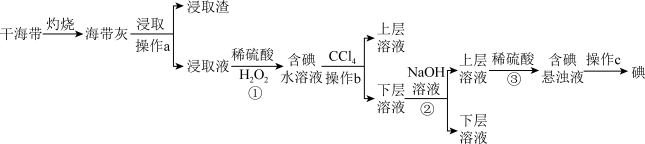
(1)在实验室进行干海带的灼烧操作时,是将海带放入___________ (填仪器名称)中,用酒精灯充分加热灰化。
(2)浸取液中碘主要以 存在,写出①发生反应的离子方程式
存在,写出①发生反应的离子方程式___________ ,实验步骤①后若检验溶液中碘单质的存在,具体方法是___________ 。
(3)向含有 的水溶液中加入
的水溶液中加入 振荡静置后的实验现象
振荡静置后的实验现象___________ 。
(4)步骤②中加入浓 溶液发生反应的化学方程式为
溶液发生反应的化学方程式为___________ ,步骤③反应中氧化剂与还原剂物质的量之比为___________ 。
(5)步骤②③是利用化学转化法将富集在四氯化碳中的碘单质重新富集在水中,该方法称为___________ 法。
(6)操作c的名称为___________ 。
Ⅱ.海水提溴
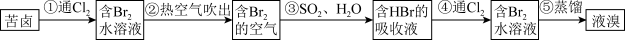
(7)流程中能说明同主族元素性质递变规律的反应为___________ (写出离子方程式)。
(8)步骤③化学方程式为___________ 。
I.海带提碘

(1)在实验室进行干海带的灼烧操作时,是将海带放入
(2)浸取液中碘主要以
 存在,写出①发生反应的离子方程式
存在,写出①发生反应的离子方程式(3)向含有
 的水溶液中加入
的水溶液中加入 振荡静置后的实验现象
振荡静置后的实验现象(4)步骤②中加入浓
 溶液发生反应的化学方程式为
溶液发生反应的化学方程式为(5)步骤②③是利用化学转化法将富集在四氯化碳中的碘单质重新富集在水中,该方法称为
(6)操作c的名称为
Ⅱ.海水提溴
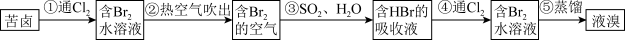
(7)流程中能说明同主族元素性质递变规律的反应为
(8)步骤③化学方程式为
您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】某油脂厂废弃的油脂加氢镍催化剂主要含金属Ni、Al、Fe及其氧化物,还有少量其他不溶性物质。采用如下工艺流程回收其中的镍制备硫酸镍晶体(NiSO4·6H2O):
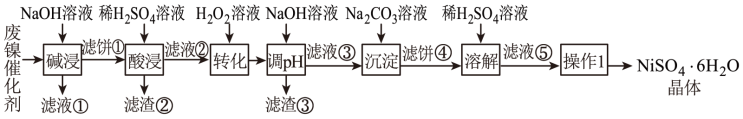
溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
回答下列问题:
(1)“碱浸”中NaOH的两个作用分别是①溶解铝及其氧化物,②_______ 。
(2)“转化”过程中反应的离子方程式为_______ ,c(H2O2)随时间t的变化关系如图所示,反应开始10~20min内c(H2O2)迅速减小,原因可能是_______ (不考虑溶液温度变化)。

(3)利用上述表格数据,计算Ni(OH)2的Ksp=_______ 。如果“转化”后的溶液中Ni2+浓度为1.0mol·L−1,则“调pH”应控制的pH范围是_______ 。
(4)硫酸镍结晶水合物的形态与温度的关系如下表。
从滤液⑤中获得稳定NiSO4·6H2O晶体的操作1依次是蒸发浓缩、_______ 、过滤、洗涤、干燥。
(5)分离出NiSO4·6H2O晶体后的剩余液体要循环使用,则应该回流到流程中滤液_______ 的位置(填②、③、⑤),其目的是_______ 。

溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
| 金属离子 | Ni2+ | Al3+ | Fe3+ | Fe2+ |
| 开始沉淀时(c=0.01mol·L−1)的pH | 7.2 | 3.7 | 2.2 | 7.5 |
| 沉淀完全时(c=1.0×10−5mol·L−1)的pH | 8.7 | 4.7 | 3.2 | 9.0 |
回答下列问题:
(1)“碱浸”中NaOH的两个作用分别是①溶解铝及其氧化物,②
(2)“转化”过程中反应的离子方程式为

(3)利用上述表格数据,计算Ni(OH)2的Ksp=
(4)硫酸镍结晶水合物的形态与温度的关系如下表。
| 温度 | 低于30.8℃ | 30.8℃~53.8℃ | 53.8℃~280℃ | 高于280℃ |
| 晶体形态 | NiSO4·7H2O | NiSO4·6H2O | 多种结晶水合物 | NiSO4 |
从滤液⑤中获得稳定NiSO4·6H2O晶体的操作1依次是蒸发浓缩、
(5)分离出NiSO4·6H2O晶体后的剩余液体要循环使用,则应该回流到流程中滤液
您最近半年使用:0次



