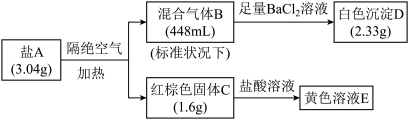
盐A由三种元素组成,其中一种为常见金属元素,某化学研究小组按如下流程图探究其组成:
(1)组成盐A的三种元素是O和___________ (写元素符号)。
(2)混合气体B的组成成分为___________ 。
(3)检验溶液E中阳离子的方法是___________ 。
(4)盐A隔绝空气加热反应的化学方程式是___________ 。
(1)组成盐A的三种元素是O和
(2)混合气体B的组成成分为
(3)检验溶液E中阳离子的方法是
(4)盐A隔绝空气加热反应的化学方程式是
22-23高一下·浙江嘉兴·期末 查看更多[2]
更新时间:2023-07-19 22:15:33
|
相似题推荐
解答题-无机推断题
|
较难
(0.4)
名校
解题方法
【推荐1】A、B、C、D均为中学常见物质且均含有同一种元素,它们之间的部分转化关系如图所示(反应条件及其他物质已经略去):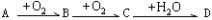 。
。
(1)若A为淡黄色固体单质,且D为强酸。则
①B物质通常用________________ (填试剂名称)来检验。
②从组成物质的元素化合价变化角度预测,B具有的与图示不相同的性质是_______________ ,并用相应的化学方程式表示你预测的性质_________________________________________________ 。
③一定条件下D转化为B有多种途径,写出其中一种D→B转化的化学方程式________________________________________ 。
(2)若A为能使湿润的红色石蕊试纸变蓝的气体,D的稀溶液能使湿润的蓝色石蕊试纸变红。
①写出实验室制取A的化学方程式_____________________________________________ 。
②标准状况下,等物质的量的B、C形成的混合气体22.4 L,与相同条件下________ L氧气混合后溶于水,气体能被水完全吸收。
③写出C→D转化的化学方程式________________________________________________ 。
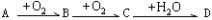 。
。(1)若A为淡黄色固体单质,且D为强酸。则
①B物质通常用
②从组成物质的元素化合价变化角度预测,B具有的与图示不相同的性质是
③一定条件下D转化为B有多种途径,写出其中一种D→B转化的化学方程式
(2)若A为能使湿润的红色石蕊试纸变蓝的气体,D的稀溶液能使湿润的蓝色石蕊试纸变红。
①写出实验室制取A的化学方程式
②标准状况下,等物质的量的B、C形成的混合气体22.4 L,与相同条件下
③写出C→D转化的化学方程式
您最近一年使用:0次
【推荐2】化合物X由三种元素组成,某实验小组按如下流程进行相关实验。

请回答:
(1)组成X的三种元素为___________ ;X的化学式为___________ 。
(2)溶液B的溶质组成为___________ (用化学式表示)。
(3)①写出由X转化为A的化学方程式:___________ 。
②写出由B转化为C的离子方程式:___________ 。
(4)设计简单实验,写出检验尾气中气体成分的方法:___________ 。

请回答:
(1)组成X的三种元素为
(2)溶液B的溶质组成为
(3)①写出由X转化为A的化学方程式:
②写出由B转化为C的离子方程式:
(4)设计简单实验,写出检验尾气中气体成分的方法:
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐3】A、B、C三种物质中均含有同一种元素,它们之间有如右图所示的转化关系(部分反应物质已略去)。

Ⅰ.(1)若A是一种两性氧化物,B的水溶液呈酸性,请写出反应④的离子方程式:______________ ,B溶液显酸性的原因(用离子方程式表示)_____________ 。
(2)若反应①为置换反应,反应④为化合反应,C物质大量存在于海水中,是人体生理活动不可缺少的物质。工业上可以用C来制取A或B,保存少量单质A的方法 是__________ ,A在氧气中燃烧产物所含的化学键有_______________ ;用C来制取B反应的化学方程式为______________________ 。
(3)若反应①②③均为化合反应,反应④为置换反应。当A为一种金属单质时,请写出反应③可能的离子方程式________________________ 。若只用一种试剂鉴别B、C,可以选的试剂是_____________ 。

Ⅰ.(1)若A是一种两性氧化物,B的水溶液呈酸性,请写出反应④的离子方程式:
(2)若反应①为置换反应,反应④为化合反应,C物质大量存在于海水中,是人体生理活动不可缺少的物质。工业上可以用C来制取A或B,保存少量单质A的方法 是
(3)若反应①②③均为化合反应,反应④为置换反应。当A为一种金属单质时,请写出反应③可能的离子方程式
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐1】为测定X的成分,设计并完成如图实验:

请回答:
(1)X的化学式是____ ;气体②的电子式_____ 。
(2)反应②的离子方程式:____ 。
(3)反应①的化学方程式:____ 。

请回答:
(1)X的化学式是
(2)反应②的离子方程式:
(3)反应①的化学方程式:
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐2】 主要用作颜料、釉料及磁性材料,利用一种钴矿石(主要成分为
主要用作颜料、釉料及磁性材料,利用一种钴矿石(主要成分为 ,含少量
,含少量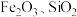 及铝、镁、钙等金属元素的氧化物)制取
及铝、镁、钙等金属元素的氧化物)制取 的工艺流程如图所示。
的工艺流程如图所示。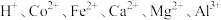 等。
等。
②部分阳离子以氢氧化物形式完全沉淀时溶液的 如下表:
如下表:
回答下列问题:
(1)“溶浸”过程中,可以加快反应速率和提高原料利用率的方法是___________ (写出一种即可)。
(2)加入 的作用是还原
的作用是还原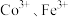 ,写出
,写出 的与
的与 反应的离子方程式
反应的离子方程式___________ 。“氧化”过程中被氧化的离子是___________ 。
(3)滤渣2的主要成分为___________ (写化学式),检验铁元素的离子已被完全沉淀的实验操作及现象:取少量待测液于试管中,___________ 。
(4)已知某温度下 。该温度下,沉淀除杂时加入足量的
。该温度下,沉淀除杂时加入足量的 溶液可将
溶液可将 沉淀除去,若所得滤液中
沉淀除去,若所得滤液中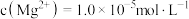 ,则滤液中
,则滤液中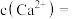
___________ 。
(5) 在空气中充分煅烧,除得到产品外还生成了
在空气中充分煅烧,除得到产品外还生成了 ,写出该反应的化学方程式
,写出该反应的化学方程式___________ 。
 主要用作颜料、釉料及磁性材料,利用一种钴矿石(主要成分为
主要用作颜料、釉料及磁性材料,利用一种钴矿石(主要成分为 ,含少量
,含少量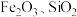 及铝、镁、钙等金属元素的氧化物)制取
及铝、镁、钙等金属元素的氧化物)制取 的工艺流程如图所示。
的工艺流程如图所示。
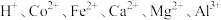 等。
等。②部分阳离子以氢氧化物形式完全沉淀时溶液的
 如下表:
如下表:| 沉淀物 |  |  |  |  |
完全沉淀的 | 3.7 | 9.6 | 9.2 | 5.2 |
(1)“溶浸”过程中,可以加快反应速率和提高原料利用率的方法是
(2)加入
 的作用是还原
的作用是还原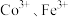 ,写出
,写出 的与
的与 反应的离子方程式
反应的离子方程式(3)滤渣2的主要成分为
(4)已知某温度下
 。该温度下,沉淀除杂时加入足量的
。该温度下,沉淀除杂时加入足量的 溶液可将
溶液可将 沉淀除去,若所得滤液中
沉淀除去,若所得滤液中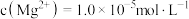 ,则滤液中
,则滤液中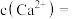
(5)
 在空气中充分煅烧,除得到产品外还生成了
在空气中充分煅烧,除得到产品外还生成了 ,写出该反应的化学方程式
,写出该反应的化学方程式
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
解题方法
【推荐3】高铁酸钠( )为紫色固体,易溶于水,微溶于NaOH溶液,具有强氧化性,可以杀菌消毒,是一种新型、高效、多功能的水处理剂。某化学实验小组利用NaClO在碱性介质中与
)为紫色固体,易溶于水,微溶于NaOH溶液,具有强氧化性,可以杀菌消毒,是一种新型、高效、多功能的水处理剂。某化学实验小组利用NaClO在碱性介质中与 溶液的反应制备
溶液的反应制备 并探究其性质,实验装置如下图所示。
并探究其性质,实验装置如下图所示。
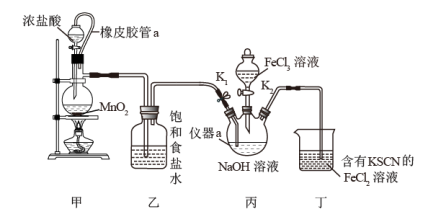
请回答下列问题:
(1)橡皮管a的作用是___________ ,装置甲中反应的化学方程式为___________ 。
(2)若去掉装置乙,其不足之处为___________ 。
(3)当装置丁中出现___________ 现象时,关闭 ;此时向装置丙中加入
;此时向装置丙中加入 溶液。
溶液。
(4)装置丙中生成 的离子方程式为
的离子方程式为___________ 。
(5)反应后,向装置丙中加入饱和的___________ (填化学式)溶液,析出紫色晶体,过滤、洗涤、干燥。
(6)取少量 晶体加入浑浊的泥浆水很快澄清,同时产生气体。请结合化学方程分析
晶体加入浑浊的泥浆水很快澄清,同时产生气体。请结合化学方程分析 的净水原理为
的净水原理为___________ 。
 )为紫色固体,易溶于水,微溶于NaOH溶液,具有强氧化性,可以杀菌消毒,是一种新型、高效、多功能的水处理剂。某化学实验小组利用NaClO在碱性介质中与
)为紫色固体,易溶于水,微溶于NaOH溶液,具有强氧化性,可以杀菌消毒,是一种新型、高效、多功能的水处理剂。某化学实验小组利用NaClO在碱性介质中与 溶液的反应制备
溶液的反应制备 并探究其性质,实验装置如下图所示。
并探究其性质,实验装置如下图所示。
请回答下列问题:
(1)橡皮管a的作用是
(2)若去掉装置乙,其不足之处为
(3)当装置丁中出现
 ;此时向装置丙中加入
;此时向装置丙中加入 溶液。
溶液。(4)装置丙中生成
 的离子方程式为
的离子方程式为(5)反应后,向装置丙中加入饱和的
(6)取少量
 晶体加入浑浊的泥浆水很快澄清,同时产生气体。请结合化学方程分析
晶体加入浑浊的泥浆水很快澄清,同时产生气体。请结合化学方程分析 的净水原理为
的净水原理为
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
解题方法
【推荐1】I.浓硝酸具有强氧化性。
①把铜粉和铁粉混合物加入热的浓硝酸中,充分反应后,溶液中有铜剩余,则溶液中存在的金属阳离子为_______ 。
②某稀硫酸与稀硝酸的混合溶液中,c(SO )+c(NO
)+c(NO )=3.0mol·L-1。取200mL该混合酸,能溶解铜的最大质量为
)=3.0mol·L-1。取200mL该混合酸,能溶解铜的最大质量为_______ 。
II.亚硫酰氯(SOC12)又名氯化亚砜,其熔点-105℃,沸点79℃,140℃以上时易分解。是一种无色或淡黄色发烟液体,遇水剧烈与水反应生成SO2和另一酸性气体,常用作脱水剂,广泛应用于医药、农药、来料工业及有机合成工业。
(1)氯化亚砜储存于阴凉、干燥、通风良好的库房,但久置后微显黄色,其原因是_______ ;用硫黄、液氯和三氧化硫为原料在一定条件可合成氯化亚砜,如果想达到原子利用率最大化,则三者的物质的量之比为_______ 。
(2)实验室合成SOCl2的原理之一为SO2+Cl2+SCl2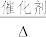 2SOCl2,部分装置如图所示。
2SOCl2,部分装置如图所示。
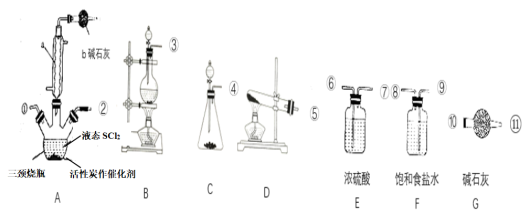
①装置b的作用是_______ 。
②实验室制取SOCl2所选仪器的链接顺序:③→_______ 。
(3)甲同学设计如图装置用ZnCl2·xH2O晶体制取无水ZnCl2,回收剩余的SOCl2并验证生成物中含有SO2(夹持及加热装置略)。选用装置如图:
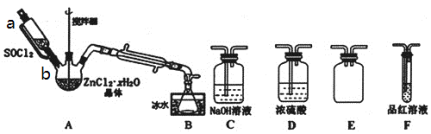
①向仪器A中缓慢滴加SOCl2,需打开活塞_______ (填“a”、“b”或“a和b”)。
②为了更加充分的回收SOCl2,写出可对装置B采取的有效措施_______ 。
(4)乙同学认为利用(3)中装置,由FeCl3·6H2O制取无水FeCl3也可用SOCl2作脱水剂,但丙同学认为会发生氧化还原反应而难以制无水FeCl3。丙同学设计了如下实验方案验证自己的观点:
取少量FeCl3·6H2O于试管中,加入过量SOCl2,振荡使两种物质充分反应;再往试管中加水溶解,加入_______ ,证明该过程发生了氧化还原反应。
①把铜粉和铁粉混合物加入热的浓硝酸中,充分反应后,溶液中有铜剩余,则溶液中存在的金属阳离子为
②某稀硫酸与稀硝酸的混合溶液中,c(SO
 )+c(NO
)+c(NO )=3.0mol·L-1。取200mL该混合酸,能溶解铜的最大质量为
)=3.0mol·L-1。取200mL该混合酸,能溶解铜的最大质量为II.亚硫酰氯(SOC12)又名氯化亚砜,其熔点-105℃,沸点79℃,140℃以上时易分解。是一种无色或淡黄色发烟液体,遇水剧烈与水反应生成SO2和另一酸性气体,常用作脱水剂,广泛应用于医药、农药、来料工业及有机合成工业。
(1)氯化亚砜储存于阴凉、干燥、通风良好的库房,但久置后微显黄色,其原因是
(2)实验室合成SOCl2的原理之一为SO2+Cl2+SCl2
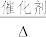 2SOCl2,部分装置如图所示。
2SOCl2,部分装置如图所示。
①装置b的作用是
②实验室制取SOCl2所选仪器的链接顺序:③→
(3)甲同学设计如图装置用ZnCl2·xH2O晶体制取无水ZnCl2,回收剩余的SOCl2并验证生成物中含有SO2(夹持及加热装置略)。选用装置如图:

①向仪器A中缓慢滴加SOCl2,需打开活塞
②为了更加充分的回收SOCl2,写出可对装置B采取的有效措施
(4)乙同学认为利用(3)中装置,由FeCl3·6H2O制取无水FeCl3也可用SOCl2作脱水剂,但丙同学认为会发生氧化还原反应而难以制无水FeCl3。丙同学设计了如下实验方案验证自己的观点:
取少量FeCl3·6H2O于试管中,加入过量SOCl2,振荡使两种物质充分反应;再往试管中加水溶解,加入
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
【推荐2】叠氮化钠(NaN3)是一种防腐剂、分析试剂和汽车安全气囊中的药剂,在生活中有重要作用。两个学习小组对叠氮化钠的制备进行设计和探究,最后一起对第二组产品纯度进行测定。
Ⅰ.叠氮化钠的制备:
第一组的制备实验

查阅资料:①氨基钠(NaNH2)的熔点为208℃,易潮解易被氧化;N2O有强氧化性,不与酸、碱反应;叠氮酸(HN3)不稳定,易分解爆炸。
② ,
, 。
。
(1)按气流方向,图1中装置的连接顺序为:a→_____→_____→d→e→_____→______→h;填仪器接口字母:___________ 。
(2)实验时装置E中生成SnO2•xH2O沉淀,反应的化学方程式为___________ 。
(3)装置C中物质充分反应后,停止加热,需继续通入 至三颈烧瓶冷却后,再关闭装置A中分液漏斗活塞,其目的为
至三颈烧瓶冷却后,再关闭装置A中分液漏斗活塞,其目的为___________ 。
第二组的制备实验:
实验装置(略去夹持仪器)如图2所示:

实验步骤如下:①制取氨气:打开装置D导管上的旋塞,加热。
②制备NaNH2:加热装置A中的金属钠,使其熔化并充分反应后,再停止加热装置D并关闭旋塞。
③制取NaN3:向装置A中b容器内充入加热介质并加热到210~220℃,然后通入N2O。
④冷却后,向产物中加入乙醇,减压浓缩结晶后,再过滤,并用乙醚洗涤,晾干。
查阅资料:NaN3是易溶于水的白色晶体,微溶于乙醇,不溶于乙醚;
(4)仪器a是___________ (填“银坩埚”“瓷坩埚”或“石英坩埚”);仪器e中盛放的药品___________ 。
(5)先加热制取NH3再加热装置A中金属钠的原因是___________ 。
Ⅱ.叠氮化钠的纯度测定:
(6)图3中装置F中发生反应的离子方程式为___________ 。

(7)若仪器G的初始读数为V1mL,实验结束时,读数为V2mL,本实验条件下气体摩尔体积为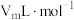 ,则产品中
,则产品中 的质量分数为
的质量分数为___________ %(用含V1、V2、Vm、w的式子表示)。
Ⅰ.叠氮化钠的制备:
第一组的制备实验

查阅资料:①氨基钠(NaNH2)的熔点为208℃,易潮解易被氧化;N2O有强氧化性,不与酸、碱反应;叠氮酸(HN3)不稳定,易分解爆炸。
②
 ,
, 。
。(1)按气流方向,图1中装置的连接顺序为:a→_____→_____→d→e→_____→______→h;填仪器接口字母:
(2)实验时装置E中生成SnO2•xH2O沉淀,反应的化学方程式为
(3)装置C中物质充分反应后,停止加热,需继续通入
 至三颈烧瓶冷却后,再关闭装置A中分液漏斗活塞,其目的为
至三颈烧瓶冷却后,再关闭装置A中分液漏斗活塞,其目的为第二组的制备实验:
实验装置(略去夹持仪器)如图2所示:

实验步骤如下:①制取氨气:打开装置D导管上的旋塞,加热。
②制备NaNH2:加热装置A中的金属钠,使其熔化并充分反应后,再停止加热装置D并关闭旋塞。
③制取NaN3:向装置A中b容器内充入加热介质并加热到210~220℃,然后通入N2O。
④冷却后,向产物中加入乙醇,减压浓缩结晶后,再过滤,并用乙醚洗涤,晾干。
查阅资料:NaN3是易溶于水的白色晶体,微溶于乙醇,不溶于乙醚;
(4)仪器a是
(5)先加热制取NH3再加热装置A中金属钠的原因是
Ⅱ.叠氮化钠的纯度测定:
(6)图3中装置F中发生反应的离子方程式为

(7)若仪器G的初始读数为V1mL,实验结束时,读数为V2mL,本实验条件下气体摩尔体积为
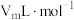 ,则产品中
,则产品中 的质量分数为
的质量分数为
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
解题方法
【推荐3】某实验小组探究钠的性质。
Ⅰ.探究钠与水反应
(1)钠与水反应的化学方程式是___________
(2)钠与水反应放出热量的现象是___________
Ⅱ.探究钠与 的反应,设计如下装置。请回答下列问题:
的反应,设计如下装置。请回答下列问题:
一、实验室用大理石与稀盐酸反应制备
(3)应选用下列装置中的___________ (填序号),乙装置中仪器A的名称是___________ 。
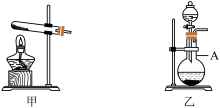
二、钠与 反应
反应
查阅资料:ⅰ.氯化钯溶液与CO反应产生黑色沉淀。
三、钠与 发生反应可能有三种情况:
发生反应可能有三种情况:
①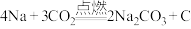 ;
;
② ;
;
②
(4)图中按气流由左至右的顺序,导管口连接顺序为 混合气体→
混合气体→___________ (填接口字母)。

(5)若无装置丁会有什么影响?___________ 。
(6)点燃装置甲中酒精灯之前,需要通一段时间 气体,其目的是
气体,其目的是___________ 。
(7)若装置乙中 溶液中没有黑色沉淀产生,说明上述反应
溶液中没有黑色沉淀产生,说明上述反应___________ (填“①”、“②”或“③”)不可能发生。
(8)为了验证装置甲中钠与 反应的产物,设计如下实验步骤(假设金属钠反应完全),请填写下列表格。
反应的产物,设计如下实验步骤(假设金属钠反应完全),请填写下列表格。
Ⅰ.探究钠与水反应
(1)钠与水反应的化学方程式是
(2)钠与水反应放出热量的现象是
Ⅱ.探究钠与
 的反应,设计如下装置。请回答下列问题:
的反应,设计如下装置。请回答下列问题:一、实验室用大理石与稀盐酸反应制备

(3)应选用下列装置中的
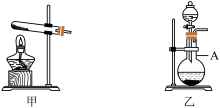
二、钠与
 反应
反应查阅资料:ⅰ.氯化钯溶液与CO反应产生黑色沉淀。
三、钠与
 发生反应可能有三种情况:
发生反应可能有三种情况:①
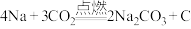 ;
;②
 ;
;②

(4)图中按气流由左至右的顺序,导管口连接顺序为
 混合气体→
混合气体→
(5)若无装置丁会有什么影响?
(6)点燃装置甲中酒精灯之前,需要通一段时间
 气体,其目的是
气体,其目的是(7)若装置乙中
 溶液中没有黑色沉淀产生,说明上述反应
溶液中没有黑色沉淀产生,说明上述反应(8)为了验证装置甲中钠与
 反应的产物,设计如下实验步骤(假设金属钠反应完全),请填写下列表格。
反应的产物,设计如下实验步骤(假设金属钠反应完全),请填写下列表格。| 步骤 | 实验操作及现象 | 实验结论 |
| ① | 取一定量装置甲中反应后的固体溶于足量水中,有黑色不溶固体,过滤 | 说明固体中含有碳 |
| ② | 说明固体中含有 | |
| ③ | 说明固体中含有 |
您最近一年使用:0次



