下列说法或表示方法中正确的是

A.由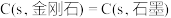 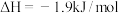 可知,金刚石比石墨稳定 可知,金刚石比石墨稳定 |
B.干冰可用于人工增雨作业。干冰在云层中的变化过程中 , , |
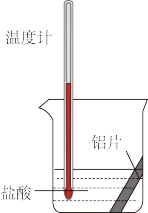
| C.将如图实验中的铝片更换为等质量的铝粉后能释放出更多的热量 |
D.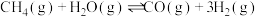  ,低温有利于该反应的自发进行 ,低温有利于该反应的自发进行 |
更新时间:2023-07-24 13:57:20
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】下列依据热化学方程式得出的结论正确的是
| A.已知2SO2(g)+O2(g)=2SO3(g)为放热反应,则SO2的能量一定高于SO3的能量 |
| B.已知C(石墨,s)=C(金刚石,s)ΔH>0,则金刚石比石墨稳定 |
| C.已知H+(aq)+OH-(aq)=H2O(l)ΔH=-57.3 kJ·mol-1,则任何酸碱中和反应的热效应均为57.3 kJ |
| D.在25℃、101kPa时,已知C(s)+O2(g)=CO2(g) ΔH,则C的燃烧热为-ΔH |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列依据热化学方程式得出的结论正确的是
| A.若2H2(g)+O2(g)=2H2O(g) ΔH=-483.6kJ·mol-1,则H2的标准燃烧热为-241.8kJ·mol-1 |
| B.若C(石墨;s)=C(金刚石,s) ΔH>0,则石墨比金刚石稳定 |
| C.已知NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l) ΔH=-57.4kJ·mol-1,则20.0gNaOH固体与稀盐酸完全中和,放出28.7kJ的热量 |
| D.已知2C(s)+2O2(g)=2CO2(g) ΔHl;2C(s)+O2(g)=2CO(g) ΔH2,则ΔHl>ΔH2 |
您最近一年使用:0次
【推荐3】下列说法正确的是
A.H2(g)+ O2(g)=H2O(g) △H1,H2(g)+ O2(g)=H2O(g) △H1,H2(g)+ O2(g)=H2O(l) △H2,则△H1>△H2 O2(g)=H2O(l) △H2,则△H1>△H2 |
B.C(s)+ O2(g)=CO(g) △H1,C(s)+O2(g)=CO2(g) △H2,则△H1<△H2 O2(g)=CO(g) △H1,C(s)+O2(g)=CO2(g) △H2,则△H1<△H2 |
| C.已知H+(aq)+OH- (aq)=H2O(l) △H=-57.3kJ·mol-1,H2SO4和Ba(OH)2反应的反应热△H=2×(-57.3)kJ·mol-1 |
| D.在某一反应中,若反应物总键能大于生成物总键能,则是放热反应 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列关于焓判据和熵判据的说法中,不正确的是
| A.放热的自发过程可能是熵减小的过程,吸热的自发过程一定为熵增加的过程 |
| B.4Fe(OH)2(s)+2H2O(l)+O2(g)=4Fe(OH)3(s) ΔH=-444.3kJ·mol-1,ΔS=-280.1J·mol-1·K-1。此反应在常温常压下能自发进行 |
| C.碳酸钙分解为吸热反应,该反应室温下不能自发进行,但在高温下则能自发进行 |
| D.吉布斯自由能大于0的反应一定不能发生 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】关于反应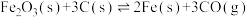
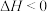 ,下列说法正确的是
,下列说法正确的是
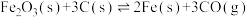
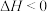 ,下列说法正确的是
,下列说法正确的是| A.该反应在低温条件下不能自发进行 |
B.增大 的量,可提高铁的产率 的量,可提高铁的产率 |
| C.只改变压强,达新平衡后CO浓度保持不变 |
| D.升高温度,逆反应速率加快,正反应速率减慢 |
您最近一年使用:0次

 CaO(s)+CO2(g) △H>0,该反应能否自发进行与温度无关
CaO(s)+CO2(g) △H>0,该反应能否自发进行与温度无关

