下表所示为某5种元素的相关信息,已知W、X都位于第三周期。
请根据要求回答问题:
(1)Q原子的结构示意图为___________ ,W在元素周期表中的位置为___________ ,Y的最高价氧化物对应水化物的化学式为___________ 。
(2)用电子式表示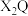 的形成过程
的形成过程___________ 。
(3)原子序数为Q的2倍的元素是___________ (填元素符号),该元素单质在过量Q元素的单质中燃烧,产物是___________ (写选项编号)
A. B.
B.
(4)X的单质与水反应的化学方程式是___________ 。
(5)下列对于Z及其化合物的推断中正确的是___________ (双选,填选项编号)。
A.Z的化合价中有-1和+7
B.Z元素单质的氧化性强于W元素单质的氧化性
C.Z的最高价氧化物对应水化物的酸性弱于W的最高价氧化物对应水化物的酸性
(6)金属性:Y___________ X(填“>”或“<”),从原子结构角度解释其原因___________ 。
(7)将X元素的单质在Q元素的单质中点燃生成M___________ (填产物名称),将M投入水中,反应现象是___________ 。
| 元素 | 信息 |
| Q | 最外层电子数是次外层电子数的3倍 |
| W | 最高化合价为+7 |
| X | 最高价氧化物对应的水化物在本周期中碱性最强 |
| Y | 焰色试验(透过蓝色钴玻璃)的火焰呈紫色 |
| Z | 与W同主族且其单质在 溶液中呈橙红色 溶液中呈橙红色 |
(1)Q原子的结构示意图为
(2)用电子式表示
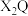 的形成过程
的形成过程(3)原子序数为Q的2倍的元素是
A.
 B.
B.
(4)X的单质与水反应的化学方程式是
(5)下列对于Z及其化合物的推断中正确的是
A.Z的化合价中有-1和+7
B.Z元素单质的氧化性强于W元素单质的氧化性
C.Z的最高价氧化物对应水化物的酸性弱于W的最高价氧化物对应水化物的酸性
(6)金属性:Y
(7)将X元素的单质在Q元素的单质中点燃生成M
更新时间:2023-06-26 16:27:53
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】下表为部分短周期元素化合价及相应原子半径的数据:
已知:①A与D可形成化合物AD2、AD3,②E与D可形成多种化合物,其中ED、ED2是常见的化合物,C可用于制光电池。
(1)用电子式表示A的氢化物与足量H 的最高价氧化物对应水化物反应生成的盐的形成过程:____________________________________________________________ ;
(2)E的简单气态氢化物极易溶于水的原因有:①_____________________________ ;
②____________________________________________ 。
(3)分子组成为ADG2的物质在水中会强烈水解,产生使品红溶液褪色的无色气体和一种强酸。该反应的化学方程式是_______________ 。
(4)将标准状况下40L无色气体ED与15L氧气通入一定浓度的NaOH溶液中,恰好被完全吸收,同时生成两种盐。请写出该反应的离子方程式_______________________ 。
| 元素性质 | 元素编号 | |||||||
| A | B | C | D | E | F | G | H | |
| 原子半径(nm) | 0.102 | 0.110 | 0.117 | 0.074 | 0.075 | 0.071 | 0.099 | 0.186 |
| 最高化合价 | +6 | +5 | +4 | +5 | +7 | +1 | ||
| 最低化合价 | ﹣2 | ﹣3 | ﹣4 | ﹣2 | ﹣3 | ﹣1 | ﹣1 | 0 |
(1)用电子式表示A的氢化物与足量H 的最高价氧化物对应水化物反应生成的盐的形成过程:
(2)E的简单气态氢化物极易溶于水的原因有:①
②
(3)分子组成为ADG2的物质在水中会强烈水解,产生使品红溶液褪色的无色气体和一种强酸。该反应的化学方程式是
(4)将标准状况下40L无色气体ED与15L氧气通入一定浓度的NaOH溶液中,恰好被完全吸收,同时生成两种盐。请写出该反应的离子方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】下表为元素周期表的一部分,表中列出了11种元素在周期表中的位置,按要求完成下列各小题。
(1)化学性质最不活泼的元素是__________ (填元素符号,下同),非金属性最强的元素__________ 。金属性最强的单质与水反应的离子方程式是___________ 。
(2)①、③、⑤三种元素的最高价氧化物水化物中,碱性最强的化合物的化学式是__________ 。
(3)①、③、⑤三种元素的原子半径由大到小的顺序是(元素符号表示)______ 。
(4)⑥,⑦两种元素形成的最简单氢化物的稳定性由大到小的顺序(写化学式)__________ ;写出⑦元素形成的简单氢化物的电子式___________ 。
(5)⑧,⑪两种元素形成的最简单氢化物的沸点由大到小的顺序(写化学式)___________ 。
| ⅠA | ⅡA | ⅢA | ⅣA | VA | ⅥA | ⅦA | 0 | |
| 2 | ⑥ | ⑦ | ⑨ | |||||
| 3 | ① | ③ | ⑤ | ⑧ | ⑩ | |||
| 4 | ② | ④ | ⑪ |
(2)①、③、⑤三种元素的最高价氧化物水化物中,碱性最强的化合物的化学式是
(3)①、③、⑤三种元素的原子半径由大到小的顺序是(元素符号表示)
(4)⑥,⑦两种元素形成的最简单氢化物的稳定性由大到小的顺序(写化学式)
(5)⑧,⑪两种元素形成的最简单氢化物的沸点由大到小的顺序(写化学式)
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】现有短周期元素性质的部分数据如下表,其中x的值表示不同元素的原子吸引电子的能力大小,若x值越大,元素的非金属性越强,金属性越弱。x值相对较大的元素在所形成的分子中化合价为负。⑩原子的核外电子层数与核外电子总数相同。
(1)根据以上条件,推断③④⑤的元素符号分别为:___ ,__ ,__ 。
(2)②的最高价氧化物的固体属于__ 晶体,空间构型__ 。
(3)用电子式表示下列原子相互结合成的化合物电子式:
①+⑦+⑩:___ ,
①+⑩形成原子个数比为1:1的化合物:__ 。
(4)写出①与⑦所形成仅含离子键的化合物和④与⑩所形成的化合物反应的离子方程式:___ 。
| 元素编号 元素性质 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |
| x | 3.44 | 2.55 | 0.98 | 3.16 | 2.19 | 3.98 | 0.93 | 3.04 | 1.91 | |
| 常见化合价 | 最高价 | +4 | +1 | +1 | +4 | |||||
| 最低价 | -2 | -1 | -3 | -1 | -3 | |||||
(1)根据以上条件,推断③④⑤的元素符号分别为:
(2)②的最高价氧化物的固体属于
(3)用电子式表示下列原子相互结合成的化合物电子式:
①+⑦+⑩:
①+⑩形成原子个数比为1:1的化合物:
(4)写出①与⑦所形成仅含离子键的化合物和④与⑩所形成的化合物反应的离子方程式:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】A、B、D、E、F、G为短周期元素,且原子序数依次递增。A、F同主族,E、G同主族。A与其他非金属元素化合时易形成共价键,F与其他非金属元素化合时易形成离子键,且F+与E2-核外电子排布相同。由以上元素组成的物质BE和D2具有相同的电子数。请回答以下问题:
(1)F位于第________ 周期第________ 族。
(2)G的离子结构示意图为________________ 。
(3)用电子式表示D2的形成过程:_____________________ 。
(4)由A、E、F三种元素形成的化合物的化学式为______ ,含有的化学键有____________ (填写完整化学键类型),属于________ 化合物。
(5)B的最高价是__________ ,由A、B组成的化合物中,含A量最高的物质的化学式是__________ ;与D2相对分子质量相等的物质的化学式是__________ ,含有的化学键有___________ (填写完整化学键类型),有________ 对共用电子对。
(1)F位于第
(2)G的离子结构示意图为
(3)用电子式表示D2的形成过程:
(4)由A、E、F三种元素形成的化合物的化学式为
(5)B的最高价是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】W、X、Y、Z、M、E、Q均为稀有气体外的短周期元素,,其原子序数依次增大,X的最外层电子数是W的4倍,Z与E的最低负化合价相同,X、M在周期表的位置如图。
(1)Y在周期表中的位置为________ ,Q的元素名称为_______ 。
(2)X的最高价氧化物的电子式为____________________ ;Y和W形成的五核离子的电子式为_________________ 。
(3)表中元素原子半径最大的是(写元素符号)________ 。
(4)X与E的最高价氧化物的水化物反应的化学反应式为___________________________ 。
(5)下列事实能说明Z元素的非金属性比E元素的非金属性强的是________
①Z单质与E的简单氢化物的溶液反应,溶液变浑浊
②在氧化还原反应中,1mol Z单质比1mol E单质得电子多
③Z和E两元素的简单氢化物受热分解,前者分解温度高
(6)M和Q两元素的单质生成1mol M的最高价化合物,恢复至室温,放热687kJ。已知该化合物的溶沸点分别为—69℃和58℃,写出该反应的热化学方程式:_________
(7)铜与一定浓度的硝酸和硫酸的混酸反应,生成的盐只有硫酸铜,同时生成的两种气体由以上元素中的两种元素组成。气体的相对分子质量都小于50,为防止污染,将产生的气体完全转化为最高价含氧酸,消耗1L 2.2mol/L NaOH溶液和1mol O2,则两种气体的分子式以及物质的量分别为____________________ ,生成的硫酸铜的物质的量为____________
| X | ||
| M | E |
(2)X的最高价氧化物的电子式为
(3)表中元素原子半径最大的是(写元素符号)
(4)X与E的最高价氧化物的水化物反应的化学反应式为
(5)下列事实能说明Z元素的非金属性比E元素的非金属性强的是
①Z单质与E的简单氢化物的溶液反应,溶液变浑浊
②在氧化还原反应中,1mol Z单质比1mol E单质得电子多
③Z和E两元素的简单氢化物受热分解,前者分解温度高
(6)M和Q两元素的单质生成1mol M的最高价化合物,恢复至室温,放热687kJ。已知该化合物的溶沸点分别为—69℃和58℃,写出该反应的热化学方程式:
(7)铜与一定浓度的硝酸和硫酸的混酸反应,生成的盐只有硫酸铜,同时生成的两种气体由以上元素中的两种元素组成。气体的相对分子质量都小于50,为防止污染,将产生的气体完全转化为最高价含氧酸,消耗1L 2.2mol/L NaOH溶液和1mol O2,则两种气体的分子式以及物质的量分别为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】X、Y、Z、Q、W、R属于元素周期表中前20号主族元素,且原子序数依次增大。基态X原子的2p能级上有2个电子,Z是地壳中含量最高的元素,W与Z同族,Q为电负性最强的主族元素。R的最外层电子数与最内层电子数相等。回答下列问题:
(1)R在元素周期表中的位置是___________ ;W的元素符号为___________ ,其基态简单离子的电子排布式为___________ 。
(2)Z元素位于元素周期表的___________ 区,其基态原子核外电子的空间运动状态有___________ 种。
(3)X、Y、Z三种元素中第一电离能最大的是________ (填元素符号),理由是________ 。
(4)Z、Q、W三种元素形成的简单气态氢化物的热稳定性由大到小的顺序___________ (用化学式表示)。
(1)R在元素周期表中的位置是
(2)Z元素位于元素周期表的
(3)X、Y、Z三种元素中第一电离能最大的是
(4)Z、Q、W三种元素形成的简单气态氢化物的热稳定性由大到小的顺序
您最近一年使用:0次



