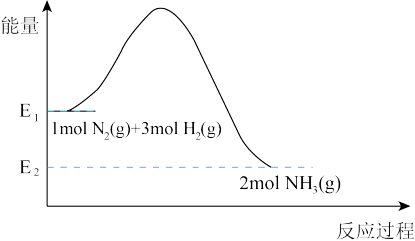
氨气是重要的化工原料,工业合成氨反应原理为: ,其反应过程中能量变化如图所示。
,其反应过程中能量变化如图所示。
(1)工业合成氨的条件是___________ 。
(2)合成氨的反应是___________ 反应(填“吸热”或“放热”)。
(3)若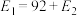 ,则每消耗
,则每消耗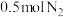 ,反应放出(或吸收)的热量
,反应放出(或吸收)的热量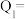
___________ kJ。
(4)将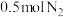 和
和 充入密闭容器中,在相同条件下发生该反应,达到平衡时,放出或吸收的热量为
充入密闭容器中,在相同条件下发生该反应,达到平衡时,放出或吸收的热量为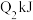 ,则
,则
___________  (填“>”“<”或“=”),理由是
(填“>”“<”或“=”),理由是___________ 。
 ,其反应过程中能量变化如图所示。
,其反应过程中能量变化如图所示。
(1)工业合成氨的条件是
(2)合成氨的反应是
(3)若
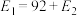 ,则每消耗
,则每消耗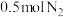 ,反应放出(或吸收)的热量
,反应放出(或吸收)的热量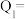
(4)将
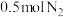 和
和 充入密闭容器中,在相同条件下发生该反应,达到平衡时,放出或吸收的热量为
充入密闭容器中,在相同条件下发生该反应,达到平衡时,放出或吸收的热量为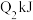 ,则
,则
 (填“>”“<”或“=”),理由是
(填“>”“<”或“=”),理由是
22-23高一下·上海徐汇·期末 查看更多[2]
更新时间:2023-06-26 16:27:53
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】回答下列问题:
(1)结合钠与水的反应现象,从能量变化的角度看,钠与水的反应属于___________ 反应。
(2)以硫酸铜为电解质溶液的银锌原电池中,银片上观察到的现象是___________ ;锌电极的反应式为___________ 。
(3)将一定量的A气体和B气体在 的密闭容器中混合并在一定条件下发生反应:
的密闭容器中混合并在一定条件下发生反应: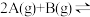
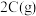 ,反应
,反应 后测得
后测得 的浓度为
的浓度为 。
。
①用物质 表示的平均反应速率为
表示的平均反应速率为___________  。
。
②其他条件不变时,再通入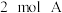 气体该反应的正反应速率将
气体该反应的正反应速率将___________ (填“增大”“不变”或“减小”)。
(1)结合钠与水的反应现象,从能量变化的角度看,钠与水的反应属于
(2)以硫酸铜为电解质溶液的银锌原电池中,银片上观察到的现象是
(3)将一定量的A气体和B气体在
 的密闭容器中混合并在一定条件下发生反应:
的密闭容器中混合并在一定条件下发生反应: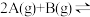
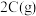 ,反应
,反应 后测得
后测得 的浓度为
的浓度为 。
。①用物质
 表示的平均反应速率为
表示的平均反应速率为 。
。②其他条件不变时,再通入
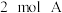 气体该反应的正反应速率将
气体该反应的正反应速率将
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】Ⅰ.已知下列热化学方程式:
①2H2(g)+O2(g)=2H2O(l) △H=-570kJ/mol
②2H2O(g)=2H2(g)+O2(g) △H=+483.6kJ/mol
回答下列问题:
(1)上述反应中属于放热反应的是_______ (填写序号)。
(2)燃烧10gH2生成液态水,放出的热量为_______ 。
(3)已知:1L1mol/LH2SO4溶液与2L1mol/LNaOH溶液完全反应,放出114.6kJ的热量,由此推知H2SO4与NaOH发生中和反应,写出该中和热的热化学方程式为_______ 。
Ⅱ.已知:工业上制二甲醚是在一定温度(230~280℃)、压强(2.0~10.0MPa)和催化剂作用下进行的,反应器中发生了下列反应:
CO(g)+2H2(g)=CH3OH(g) ΔH1=-90.7kJ·mol-1 ①
2CH3OH(g)=CH3OCH3(g)+H2O(g) ΔH2=-23.5kJ·mol-1 ②
CO(g)+H2O(g)=CO2(g)+H2(g) ΔH3=-41.2kJ·mol-1 ③
(4)反应器中的总反应可表示为3CO(g)+3H2(g)⇌CH3OCH3(g)+CO2(g),计算该反应的ΔH=_______ 。
①2H2(g)+O2(g)=2H2O(l) △H=-570kJ/mol
②2H2O(g)=2H2(g)+O2(g) △H=+483.6kJ/mol
回答下列问题:
(1)上述反应中属于放热反应的是
(2)燃烧10gH2生成液态水,放出的热量为
(3)已知:1L1mol/LH2SO4溶液与2L1mol/LNaOH溶液完全反应,放出114.6kJ的热量,由此推知H2SO4与NaOH发生中和反应,写出该中和热的热化学方程式为
Ⅱ.已知:工业上制二甲醚是在一定温度(230~280℃)、压强(2.0~10.0MPa)和催化剂作用下进行的,反应器中发生了下列反应:
CO(g)+2H2(g)=CH3OH(g) ΔH1=-90.7kJ·mol-1 ①
2CH3OH(g)=CH3OCH3(g)+H2O(g) ΔH2=-23.5kJ·mol-1 ②
CO(g)+H2O(g)=CO2(g)+H2(g) ΔH3=-41.2kJ·mol-1 ③
(4)反应器中的总反应可表示为3CO(g)+3H2(g)⇌CH3OCH3(g)+CO2(g),计算该反应的ΔH=
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】回答下列问题
(1)下列变化中属于吸热反应的是___________
①铝片与稀盐酸的反应
②将胆矾加热变为白色粉末
③干冰汽化
④过氧化钠与水的反应
⑤甲烷在氧气中的燃烧反应
⑥NaHCO3与盐酸的反应
(2)硫碘循环分解水是一种高效、环保的制氢方法,其流程图如下:
反应Ⅱ: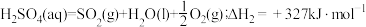
反应Ⅲ: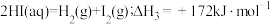
反应: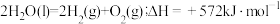
则反应Ⅰ的热化学方程式为___________ 。
(3)断裂 化学键所需要的能量如表所示,肼(H2N-NH2)的有关化学反应的能量变化如图所示。
化学键所需要的能量如表所示,肼(H2N-NH2)的有关化学反应的能量变化如图所示。
①1molN2H4(g)与1molO2(g)断键吸收的能量为___________ kJ。
②a=___________ 。
(1)下列变化中属于吸热反应的是
①铝片与稀盐酸的反应
②将胆矾加热变为白色粉末
③干冰汽化
④过氧化钠与水的反应
⑤甲烷在氧气中的燃烧反应
⑥NaHCO3与盐酸的反应
(2)硫碘循环分解水是一种高效、环保的制氢方法,其流程图如下:
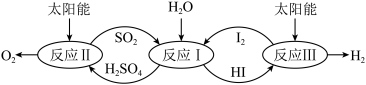
反应Ⅱ:
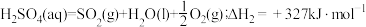
反应Ⅲ:
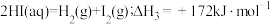
反应:
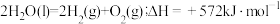
则反应Ⅰ的热化学方程式为
(3)断裂
 化学键所需要的能量如表所示,肼(H2N-NH2)的有关化学反应的能量变化如图所示。
化学键所需要的能量如表所示,肼(H2N-NH2)的有关化学反应的能量变化如图所示。| 化学键 |  |  |  |  |
| 能量/( kJ∙mol-1) | a | 498 | 946 | 391 |
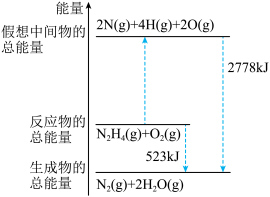
①1molN2H4(g)与1molO2(g)断键吸收的能量为
②a=
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】人类的生活离不开化学反应,在关注反应物质变化的同时也要关注能量变化。
I.金刚石和石墨均为碳的同素异形体,它们在氧气不足时燃烧生成一氧化碳,氧气充足时燃烧生成二氧化碳,反应中放出的热量如图所示。

(1)在通常状况下,___________ (填“金刚石”或“石墨”)更稳定;石墨的燃烧热ΔH为___________
(2)若12g金刚石在24g氧气中燃烧,生成气体36g,则该过程放出的热量为___________ 。
(3)已知:N2、O2分子中化学键的键能分别是946mol·L-1、497mol·L-1,N2(g)+O2(g)=2NO(g) ΔH=+180.0kJ·mol-1,综合上述有关信息请写出CO和NO反应生成两种无毒气体的热化学方程式:___________ 。
II.Cl、C、Si在工业生产、生活中有重要应用
(4)用液氯消毒自来水会产生微量有机氯代物,危害人体健康,可使用二氧化氯(ClO2)代替液氯工业上以黄铁矿(FeS2)、氯酸钠(NaClO3)和硫酸溶液混合制备二氧化氯。已知黄铁矿中的硫元素(-1价)被氧化成 ,制备二氧化氯的离子方程式为
,制备二氧化氯的离子方程式为___________ 。
(5)下列关于C、Si元素及化合物的说法中正确的是___________
A.碳纳米材料包括:富勒烯、碳纳米管、石墨烯、炭黑
B.云母、沙土、宝石的主要成分为二氧化硅
C.工业制水泥、玻璃的主要原料中都有碳酸钙
D.实验室中氢氟酸能用玻璃瓶盛装但不能用玻璃塞
E.氮化硅熔点高,硬度大,电绝缘性好可用于制作坩埚、耐高温轴承、制作切削刀具
I.金刚石和石墨均为碳的同素异形体,它们在氧气不足时燃烧生成一氧化碳,氧气充足时燃烧生成二氧化碳,反应中放出的热量如图所示。

(1)在通常状况下,
(2)若12g金刚石在24g氧气中燃烧,生成气体36g,则该过程放出的热量为
(3)已知:N2、O2分子中化学键的键能分别是946mol·L-1、497mol·L-1,N2(g)+O2(g)=2NO(g) ΔH=+180.0kJ·mol-1,综合上述有关信息请写出CO和NO反应生成两种无毒气体的热化学方程式:
II.Cl、C、Si在工业生产、生活中有重要应用
(4)用液氯消毒自来水会产生微量有机氯代物,危害人体健康,可使用二氧化氯(ClO2)代替液氯工业上以黄铁矿(FeS2)、氯酸钠(NaClO3)和硫酸溶液混合制备二氧化氯。已知黄铁矿中的硫元素(-1价)被氧化成
 ,制备二氧化氯的离子方程式为
,制备二氧化氯的离子方程式为(5)下列关于C、Si元素及化合物的说法中正确的是
A.碳纳米材料包括:富勒烯、碳纳米管、石墨烯、炭黑
B.云母、沙土、宝石的主要成分为二氧化硅
C.工业制水泥、玻璃的主要原料中都有碳酸钙
D.实验室中氢氟酸能用玻璃瓶盛装但不能用玻璃塞
E.氮化硅熔点高,硬度大,电绝缘性好可用于制作坩埚、耐高温轴承、制作切削刀具
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】氨是重要的化工产品之一,研究合成氨反应具有重要意义。
(1)已知断裂下列化学键需要吸收的能量分别为: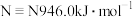 ,
,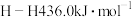 ,
,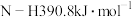 ,写出以N2和H2为原料合成NH3的热化学方程式
,写出以N2和H2为原料合成NH3的热化学方程式______ 。
(2)某小组研究了其他条件不变时,改变某一条件对上述反应的影响,实验结果如下图 所示:
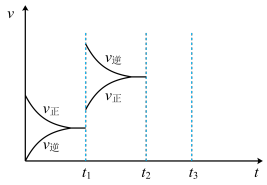
①t1时刻改变的条件为__________________ 。
②t2时刻,恒压充入氦气,t3时刻达到平衡。在图中画出t2时刻后的速率变化图象_____________ 。
(1)已知断裂下列化学键需要吸收的能量分别为:
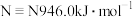 ,
,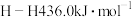 ,
,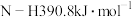 ,写出以N2和H2为原料合成NH3的热化学方程式
,写出以N2和H2为原料合成NH3的热化学方程式(2)某小组研究了其他条件不变时,改变某一条件对上述反应的影响,实验结果如下图 所示:

①t1时刻改变的条件为
②t2时刻,恒压充入氦气,t3时刻达到平衡。在图中画出t2时刻后的速率变化图象
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】能源是人类生活和社会发展的基础,研究化学反应中的能量变化,有助于更好地利用化学反应为生产和生活服务.阅读下列有关能源的材料,回答有关问题:
(1)从能量的角度看,旧键断裂,新键形成必然有能量变化.已知拆开1molH﹣H键、1mol I﹣I、1mol H﹣I键分别需要吸收的能量为436kJ、151kJ、299kJ.则由氢气和碘反应生成2mol HI需要_______ (填“放出”或“吸收”)_______ kJ的热量.
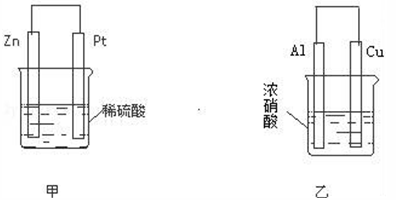
(2)在生产和生活中经常遇到化学能与电能的相互转化.
在如图甲、乙两装置中,甲中负极电极反应式为__________________ ,溶液中的阴离子向______ 极移动(填“Zn”或“Pt”);乙中铜电极作_______ 极,发生_______ 反应(填“氧化”或“还原”).

(1)从能量的角度看,旧键断裂,新键形成必然有能量变化.已知拆开1molH﹣H键、1mol I﹣I、1mol H﹣I键分别需要吸收的能量为436kJ、151kJ、299kJ.则由氢气和碘反应生成2mol HI需要
(2)在生产和生活中经常遇到化学能与电能的相互转化.
在如图甲、乙两装置中,甲中负极电极反应式为
您最近一年使用:0次
填空题
|
适中
(0.65)
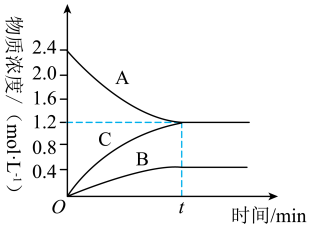
【推荐1】在一定温度和一定体积条件下,A、B、C都是气体。反应过程中,反应物与生成物的浓度随时间变化的曲线如图。回答下列问题:
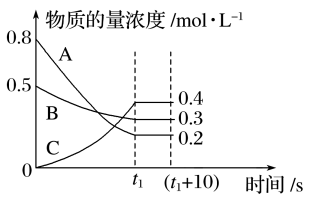
(1)该反应的化学方程式为____ 。
(2)0~t1s内A的反应速率为____ 。
(3)反应达平衡后与反应前的压强之比为____ 。
(4)(t1+10)s时,A气体的体积分数为____ ,此时v正(A)____ (填“>”“<”或“=”)v逆(B)。
(5)下列关于该反应的说法正确的是___ (填字母)。
a.到达t1s时反应已停止
b.在t1s之前B气体的消耗速率大于它的生成速率
c.在t1s时C气体的正反应速率等于逆反应速率
(6)能加快该反应速率的措施是____ 。
①升高温度
②容器体积不变,充入惰性气体Ar
③若容器压强不变,充入惰性气体Ar
④容器体积不变,充入A、B、C气体

(1)该反应的化学方程式为
(2)0~t1s内A的反应速率为
(3)反应达平衡后与反应前的压强之比为
(4)(t1+10)s时,A气体的体积分数为
(5)下列关于该反应的说法正确的是
a.到达t1s时反应已停止
b.在t1s之前B气体的消耗速率大于它的生成速率
c.在t1s时C气体的正反应速率等于逆反应速率
(6)能加快该反应速率的措施是
①升高温度
②容器体积不变,充入惰性气体Ar
③若容器压强不变,充入惰性气体Ar
④容器体积不变,充入A、B、C气体
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】完成下列问题
(1)实验一:已知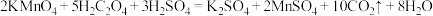 。在酸性高锰酸钾溶液与草酸(
。在酸性高锰酸钾溶液与草酸( )溶液反应时,发现开始一段时间,反应速度较快,溶液褪色不明显,但不久突然褪色,反应速度明显加快。
)溶液反应时,发现开始一段时间,反应速度较快,溶液褪色不明显,但不久突然褪色,反应速度明显加快。
①针对上述实验现象,小组同学认为 与
与 反应放热,导致溶液温度升高,反应速率加快。从影响化学反应速率的因素看,你认为还可能是
反应放热,导致溶液温度升高,反应速率加快。从影响化学反应速率的因素看,你认为还可能是___________ 的影响。
②若用实验证明你的猜想,除酸性高锰酸钾溶液、草酸溶液外,还需要的试剂最合理的是___________ (填字母)。
A.硫酸钾 B.硫酸锰 C.二氧化锰 D.水
(2)实验二:探究 和
和 混合时生成
混合时生成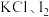 和
和 的反应存在一定的限度。
的反应存在一定的限度。
Ⅰ.向 溶液中滴加
溶液中滴加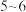 滴
滴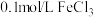 溶液,充分反应后,将所得溶液分成甲、乙两等份;
溶液,充分反应后,将所得溶液分成甲、乙两等份;
Ⅱ.向甲中滴加 ,充分振荡;
,充分振荡;
Ⅲ.向乙中滴加试剂X。
请回答下列问题:
①步骤Ⅲ中,试剂X是___________ ;
②步骤Ⅱ和Ⅲ中的实验现象说明 和
和 混合时生成
混合时生成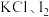 和
和 的反应存在一定的限度,该实验现象是
的反应存在一定的限度,该实验现象是___________ 。
(1)实验一:已知
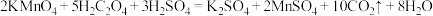 。在酸性高锰酸钾溶液与草酸(
。在酸性高锰酸钾溶液与草酸( )溶液反应时,发现开始一段时间,反应速度较快,溶液褪色不明显,但不久突然褪色,反应速度明显加快。
)溶液反应时,发现开始一段时间,反应速度较快,溶液褪色不明显,但不久突然褪色,反应速度明显加快。①针对上述实验现象,小组同学认为
 与
与 反应放热,导致溶液温度升高,反应速率加快。从影响化学反应速率的因素看,你认为还可能是
反应放热,导致溶液温度升高,反应速率加快。从影响化学反应速率的因素看,你认为还可能是②若用实验证明你的猜想,除酸性高锰酸钾溶液、草酸溶液外,还需要的试剂最合理的是
A.硫酸钾 B.硫酸锰 C.二氧化锰 D.水
(2)实验二:探究
 和
和 混合时生成
混合时生成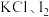 和
和 的反应存在一定的限度。
的反应存在一定的限度。Ⅰ.向
 溶液中滴加
溶液中滴加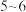 滴
滴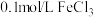 溶液,充分反应后,将所得溶液分成甲、乙两等份;
溶液,充分反应后,将所得溶液分成甲、乙两等份;Ⅱ.向甲中滴加
 ,充分振荡;
,充分振荡;Ⅲ.向乙中滴加试剂X。
请回答下列问题:
①步骤Ⅲ中,试剂X是
②步骤Ⅱ和Ⅲ中的实验现象说明
 和
和 混合时生成
混合时生成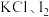 和
和 的反应存在一定的限度,该实验现象是
的反应存在一定的限度,该实验现象是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】根据表中所给数据分析催化剂对氨的合成反应速率的影响_____ 。
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】阅读短文,回答问题。
合成氨工业结束了人类依靠天然氮肥的历史,解决了人类的粮食问题。近一百年来,工业上一直采用在高温、高压、催化剂的条件下将氮气和氢气转化为氨气,这样的条件每年需要消耗全世界1%~2%的能源供应,科学家一直致力于探索在温和条件下合成氨。中科大研究团队研制了“钌单原子催化剂”合成氨,应用该催化剂通过电化学反应在室温下即可合成氨。原理如图1所示。
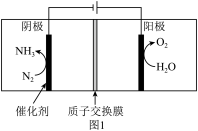
阴极表面电极反应的微观过程如图2所示。

该项研究工作开辟了单原子催化剂在电化学合成氨反应中的新途径,使得温和条件下合成氨成为可能。
请依据以上短文,判断下列说法是否正确(填“对”或“错”)。
1.合成氨工业对解决人类的粮食问题发挥了重要作用。___
2.传统方法合成氨的化学方程式为N2+3H2 2NH3。
2NH3。___
3.传统合成氨的方法需消耗大量能源。___
4.“钌单原子催化剂”合成氨体现了我国科学家在科研领域的创新。___
5.图1中,水在阳极失去电子生成氧气。___
6.图2中,步骤②所示反应的方程式为有N+H+=NH。___
合成氨工业结束了人类依靠天然氮肥的历史,解决了人类的粮食问题。近一百年来,工业上一直采用在高温、高压、催化剂的条件下将氮气和氢气转化为氨气,这样的条件每年需要消耗全世界1%~2%的能源供应,科学家一直致力于探索在温和条件下合成氨。中科大研究团队研制了“钌单原子催化剂”合成氨,应用该催化剂通过电化学反应在室温下即可合成氨。原理如图1所示。

阴极表面电极反应的微观过程如图2所示。

该项研究工作开辟了单原子催化剂在电化学合成氨反应中的新途径,使得温和条件下合成氨成为可能。
请依据以上短文,判断下列说法是否正确(填“对”或“错”)。
1.合成氨工业对解决人类的粮食问题发挥了重要作用。
2.传统方法合成氨的化学方程式为N2+3H2
 2NH3。
2NH3。3.传统合成氨的方法需消耗大量能源。
4.“钌单原子催化剂”合成氨体现了我国科学家在科研领域的创新。
5.图1中,水在阳极失去电子生成氧气。
6.图2中,步骤②所示反应的方程式为有N+H+=NH。
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】工业制造硫酸的主要反应为:
SO2(g)+ O2(g)=SO3(g) △H=-99kJ•mol-1 ①
O2(g)=SO3(g) △H=-99kJ•mol-1 ①
SO3(g)+H2O(l)=H2SO4(aq) ②
反应①的平衡常数K随温度升高而减小,所用催化剂的主要成分为V2O5(6%~12%)、K2SO4(17%~20%)、SiO2(50%~70%),能使催化剂中毒的物质有砷、硒、氟等。请根据以上信息讨论二氧化硫氧化反应的工艺条件(温度、压强、原料气配比等)对工业生产硫酸的影响____ 。
SO2(g)+
 O2(g)=SO3(g) △H=-99kJ•mol-1 ①
O2(g)=SO3(g) △H=-99kJ•mol-1 ①SO3(g)+H2O(l)=H2SO4(aq) ②
反应①的平衡常数K随温度升高而减小,所用催化剂的主要成分为V2O5(6%~12%)、K2SO4(17%~20%)、SiO2(50%~70%),能使催化剂中毒的物质有砷、硒、氟等。请根据以上信息讨论二氧化硫氧化反应的工艺条件(温度、压强、原料气配比等)对工业生产硫酸的影响
您最近一年使用:0次