下列关于氮及其化合物的说法错误的是
| A.NO2与水反应生成HNO3,但NO2不属于酸性氧化物 |
| B.某盐与强碱的浓溶液混合加热,产生的气体遇HCl气体冒白烟,可证明是铵盐 |
| C.浓硝酸与铜或碳反应时均体现其酸性和强氧化性 |
D.加热NH4Cl和 的固体混合物,可用CaCl2干燥生成的气体 的固体混合物,可用CaCl2干燥生成的气体 |
更新时间:2023-08-14 15:00:56
|
相似题推荐
多选题
|
适中
(0.65)
解题方法
【推荐1】下列实验中,所采取的方法及其原理均正确的是
| 选项 | 实验目的 | 实验方法 | 实验原理 |
| A | 除去NO中的NO2 | 通过盛有水的洗气瓶 | NO2能与水反应生成NO,NO不溶于水 |
| B | 除去乙醇中的水 | 加入无水硫酸铜,然后蒸馏 | 无水硫酸铜能结合水形成晶体 |
| C | 除去KNO3中的NaCl | 冷却热饱和溶液,重结晶 | NaCl的溶解度随温度变化改变较大 |
| D | 除去铁粉中混有的铝粉 | 加入过量NaOH溶液,充分反应后过滤 | 铝能与NaOH溶液反应而铁不能 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
多选题
|
适中
(0.65)
【推荐2】下列关于常见金属、非金属元素及其化合物的说法错误的是
A. 与水反应生成硝酸,说明 与水反应生成硝酸,说明 是酸性氧化物 是酸性氧化物 |
B. 能使品红溶液褪色,说明 能使品红溶液褪色,说明 具有漂白性 具有漂白性 |
C.向酸性 溶液中加入 溶液中加入 粉末,紫色褪去,说明 粉末,紫色褪去,说明 中含有 中含有 价 价 |
D.硫与浓 在加热条件下生成 在加热条件下生成 和水,说明浓 和水,说明浓 具有酸性和强氧化性 具有酸性和强氧化性 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列离子方程式正确的是
A.向氨水中加盐酸:NH3·H2O+H+=NH +H2O +H2O |
B.实验室用氯化铵和熟石灰制氨:NH +OH- +OH- NH3↑+H2O NH3↑+H2O |
| C.将SO2通入到BaCl2溶液中:SO2+H2O+Ba2+=BaSO3↓+2H+ |
D.铜与稀硝酸反应:3Cu+8H++2NO =3Cu2++2NO↑+4H2O =3Cu2++2NO↑+4H2O |
您最近一年使用:0次
多选题
|
适中
(0.65)
【推荐2】某学习小组利用 制备
制备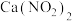 的流程如下图,下列说法正确的是
的流程如下图,下列说法正确的是
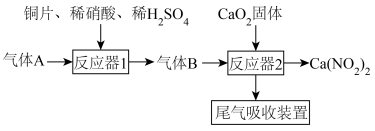
 制备
制备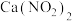 的流程如下图,下列说法正确的是
的流程如下图,下列说法正确的是
A.实验前和实验后均需通一段时间的 或 或 |
| B.反应器1中加入少量稀硫酸可提高稀硝酸的利用率 |
| C.气体B在反应器1中是还原产物,在2中是氧化剂 |
| D.理论上反应器1、2中生成盐的物质的量之比为3:1 |
您最近一年使用:0次
多选题
|
适中
(0.65)
解题方法
【推荐1】关于物质的检验,下列判断正确的是
| A.在溶液中加入盐酸酸化,无现象;再加入BaCl2溶液,如果生成白色沉淀,则原溶液中一定有大量的SO42-存在 |
| B.在溶液中加入AgNO3溶液,生成不溶于硝酸的沉淀,则原溶液中一定有Cl-存在 |
| C.在溶液中加入浓NaOH溶液,加热后如果生成气体使湿润的红色石蕊试纸变蓝,则原溶液一定是铵盐溶液 |
| D.在溶液中加入KSCN溶液,无现象;再加入稀硝酸,溶液变血红色,则原溶液中一定有Fe2+存在 |
您最近一年使用:0次
多选题
|
适中
(0.65)
解题方法
【推荐2】根据下列实验操作和现象所得出的结论正确的是
| 选项 | 实验操作和现象 | 结论 |
| A | 向盛有某盐溶液的试管中滴入氢氧化钠溶液后,加热,试管口处湿润的红色石蕊试纸变蓝 | 该盐中含 |
| B | 向溴水中通入某无色气体,溴水褪色 | 该气体可能是CH2=CH2 |
| C | 一定量的铜与硝酸充分反应后,有铜剩余,再加入少量稀硫酸,铜继续溶解,并有气泡放出 | Cu与稀硫酸发生了反应 |
| D | 向淀粉溶液中加少量稀硫酸,加热4~5min。冷却后向其中加入新制Cu(OH)2悬浊液,加热至沸腾,无砖红色沉淀 | 淀粉没有发生水解 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
多选题
|
适中
(0.65)
解题方法
【推荐1】下列对一些实验事实、理论推测或解释都正确的是
| 选项 | 实验事实 | 理论推测或解释 |
| A | Si、Ge均是半导体材料 | IVA族元素的单质都是半导体材料 |
| B | Be第一电离能小于B | 同周期元素原子的电离能随原子序数增大呈增大趋势 |
| C | KSCN遇Fe3+血红色 | SCN—能通过配位键与Fe3+生成[Fe(SCN)n]3-n(n=1~6)而呈现血红色 |
| D | 冰的密度比液态水小 | 冰中水分子间最大限度形成氢键,水分子间形成的空穴造成冰晶体的微观空间存在空隙,体积膨胀 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
解题方法
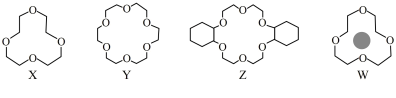
【推荐2】X、Y、Z是常见的三种冠醚,其结构如图所示。它们能与碱金属离子作用,并随着环的大小不同而与不同金属离子作用。Li+的体积与X的空腔大小相近,恰好能进入X的环内,且Li+与氧原子的一对孤电子对作用形成稳定结构W(如图所示)。
例如:冠醚Z可与KMnO4发生如图所示的变化:
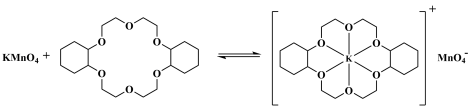
下列说法正确的是

例如:冠醚Z可与KMnO4发生如图所示的变化:

下列说法正确的是
| A.W中Li+与冠醚X之间的作用属于离子键 |
| B.冠醚Y既能与K+形成稳定结构,也能与Li+形成稳定结构 |
| C.烯烃难溶于水,被KMnO4水溶液氧化的效果较差,若烯烃中溶入冠醚Z,氧化效果明显提升 |
| D.与X相比,W中的C-O-C键角更大 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
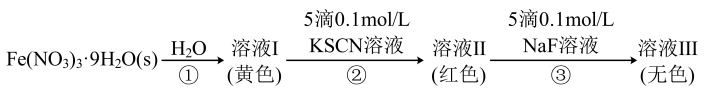
【推荐3】Fe3+可与H2O、SCN-、Cl-、F-等形成配离子使溶液显色。如:显浅紫色的[Fe(H2O)6]3+、红色的[Fe(SCN)6]3-、黄色的[FeCl4]-、无色[FeF6]3-。某同学按如图步骤完成实验: [Fe(SCN)6]3-(红色);Fe3++6F-
[Fe(SCN)6]3-(红色);Fe3++6F- [FeF6]3-(无色)。下列说法正确的是
[FeF6]3-(无色)。下列说法正确的是
 [Fe(SCN)6]3-(红色);Fe3++6F-
[Fe(SCN)6]3-(红色);Fe3++6F- [FeF6]3-(无色)。下列说法正确的是
[FeF6]3-(无色)。下列说法正确的是| A.Ⅰ中溶液呈黄色可能是由Fe3+水解产物的颜色引起的 |
| B.SCN-与Fe3+的配位能力强于F- |
| C.为了能观察到溶液Ⅰ中[Fe(H2O)6]3+的颜色,可向该溶液中加入稀盐酸 |
| D.向溶液Ⅲ中加入足量的KSCN固体,溶液可能再次变为红色 |
您最近一年使用:0次

 =2Br-+2H++SO
=2Br-+2H++SO
 、Na+、NH
、Na+、NH

