实验室需要950mL0.5mol·L-1的稀硫酸和480mL1mol·L-1NaOH溶液进行实验,请你用98%的浓硫酸(ρ=1.84g·mL-1)和NaOH固体进行配制。回答下列问题:
(1)配制稀硫酸时,需要使用的玻璃仪器有量筒、烧杯、胶头滴管、_________ (写仪器名称)。
(2)配制稀硫酸时,需要量取98%的浓硫酸________ mL,应选用下列量器中的_________ (填字母)。
A.5mL量筒 B.10mL量筒 C.25mL量筒 D.50mL量筒
(3)稀释浓硫酸的操作是___________ 。
(4)对所配制的稀硫酸进行测定,发现其浓度为0.48mol·L-1,下列各项操作可能引起该误差的是___________ (填字母)
A.用量筒量取浓硫酸读数时仰视刻度线
B.转移稀释的硫酸溶液后未洗涤烧杯和玻璃棒
C.浓硫酸稀释后未经冷却即转移到容量瓶中
D.容量瓶未干燥就用来配制溶液
E.定容后摇匀溶液,发现液面低于刻度线,再加入少量水使液面与刻度线相平
(1)配制稀硫酸时,需要使用的玻璃仪器有量筒、烧杯、胶头滴管、
(2)配制稀硫酸时,需要量取98%的浓硫酸
A.5mL量筒 B.10mL量筒 C.25mL量筒 D.50mL量筒
(3)稀释浓硫酸的操作是
(4)对所配制的稀硫酸进行测定,发现其浓度为0.48mol·L-1,下列各项操作可能引起该误差的是
A.用量筒量取浓硫酸读数时仰视刻度线
B.转移稀释的硫酸溶液后未洗涤烧杯和玻璃棒
C.浓硫酸稀释后未经冷却即转移到容量瓶中
D.容量瓶未干燥就用来配制溶液
E.定容后摇匀溶液,发现液面低于刻度线,再加入少量水使液面与刻度线相平
更新时间:2023-08-16 16:10:03
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】某硫化锌精矿的主要成分为 (还含一定量
(还含一定量 ),以其为原料制备七水合硫酸锌(
),以其为原料制备七水合硫酸锌( )与铁红的工艺流程如图所示:
)与铁红的工艺流程如图所示:

已知:①焙砂的成分是ZnO和FeO
②相关金属离子形成氢氧化物沉淀的pH范围如下:
回答下列问题:
(1)“焙烧”中ZnS发生反应的化学方程式为___________ 。“净化制酸”所得的产品可用于后续的___________ 操作。
(2)“浸出”后加入 发生反应的离子方程式为
发生反应的离子方程式为___________ ,调pH的范围是___________ 。
(3)“滤渣”的化学式是___________ ,由“滤液”得到 的操作是蒸发浓缩、
的操作是蒸发浓缩、___________ 、过滤洗涤。
(4)用以上流程制备的七水合硫酸锌样品配制 溶液,需用托盘天平称取样品
溶液,需用托盘天平称取样品___________ g,溶解操作后须用到的玻璃仪器有玻璃棒、胶头滴管、___________ 。
 (还含一定量
(还含一定量 ),以其为原料制备七水合硫酸锌(
),以其为原料制备七水合硫酸锌( )与铁红的工艺流程如图所示:
)与铁红的工艺流程如图所示:
已知:①焙砂的成分是ZnO和FeO
②相关金属离子形成氢氧化物沉淀的pH范围如下:
| 金属离子 |  |  |  |
| 开始沉淀的pH | 1.5 | 6.3 | 6.2 |
| 沉淀完全的pH | 2.8 | 8.3 | 8.2 |
(1)“焙烧”中ZnS发生反应的化学方程式为
(2)“浸出”后加入
 发生反应的离子方程式为
发生反应的离子方程式为(3)“滤渣”的化学式是
 的操作是蒸发浓缩、
的操作是蒸发浓缩、(4)用以上流程制备的七水合硫酸锌样品配制
 溶液,需用托盘天平称取样品
溶液,需用托盘天平称取样品
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】 (草酸亚铁)常用作分析试剂,受热分解后生成三种氧化物。某兴趣小组将
(草酸亚铁)常用作分析试剂,受热分解后生成三种氧化物。某兴趣小组将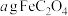 充分加热,得到
充分加热,得到 ,同时将生成的气体先缓慢通过足量的澄清石灰水,得到沉淀
,同时将生成的气体先缓慢通过足量的澄清石灰水,得到沉淀 ,逸出的气体其体积换算成标准状况为
,逸出的气体其体积换算成标准状况为 ,能使热的
,能使热的 变成红色。
变成红色。
(1) 受热分解产物除
受热分解产物除 外还有
外还有____________ 。
(2)
____________ 。
(3)为将生成的 完全溶解,需要
完全溶解,需要 的
的 溶液
溶液____________  。
。
(4)实验室由 的
的 溶液配制
溶液配制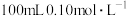 的
的 溶液,所需
溶液,所需 的
的 溶液的体积为
溶液的体积为____________  。配制所需的玻璃仪器除酸式滴定管(用于准确量取
。配制所需的玻璃仪器除酸式滴定管(用于准确量取 的
的 溶液)、烧杯、玻璃棒外还有
溶液)、烧杯、玻璃棒外还有____________ 。
(5)下列操作会使得(4)中所配 溶液物质的量浓度偏小的是
溶液物质的量浓度偏小的是____________ 。
A.量取 的
的 溶液时部分
溶液时部分 挥发
挥发
B.实验前容量瓶洗涤后,未干燥
C.转移溶液后,未洗涤烧杯和玻璃棒并将洗涤液转移到容量瓶中
D.定容时俯视刻度线
 (草酸亚铁)常用作分析试剂,受热分解后生成三种氧化物。某兴趣小组将
(草酸亚铁)常用作分析试剂,受热分解后生成三种氧化物。某兴趣小组将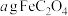 充分加热,得到
充分加热,得到 ,同时将生成的气体先缓慢通过足量的澄清石灰水,得到沉淀
,同时将生成的气体先缓慢通过足量的澄清石灰水,得到沉淀 ,逸出的气体其体积换算成标准状况为
,逸出的气体其体积换算成标准状况为 ,能使热的
,能使热的 变成红色。
变成红色。(1)
 受热分解产物除
受热分解产物除 外还有
外还有(2)

(3)为将生成的
 完全溶解,需要
完全溶解,需要 的
的 溶液
溶液 。
。(4)实验室由
 的
的 溶液配制
溶液配制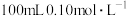 的
的 溶液,所需
溶液,所需 的
的 溶液的体积为
溶液的体积为 。配制所需的玻璃仪器除酸式滴定管(用于准确量取
。配制所需的玻璃仪器除酸式滴定管(用于准确量取 的
的 溶液)、烧杯、玻璃棒外还有
溶液)、烧杯、玻璃棒外还有(5)下列操作会使得(4)中所配
 溶液物质的量浓度偏小的是
溶液物质的量浓度偏小的是A.量取
 的
的 溶液时部分
溶液时部分 挥发
挥发B.实验前容量瓶洗涤后,未干燥
C.转移溶液后,未洗涤烧杯和玻璃棒并将洗涤液转移到容量瓶中
D.定容时俯视刻度线
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】已知无水FeCl3在空气中遇水易潮解变质,加热易升华。实验室利用如图所示实验装置制取无水FeCl3(夹持装置略去),FeCl3在收集器中得到。

回答下列问题:
(1)仪器a的名称是_______ ;溶液X、Y依次是_______ 、_______ ;
(2)实验结束时,应先熄灭_______ (填“A”或“D”)处酒精灯;装置F的作用是_______ 。
(3)装置G发生反应的离子方程式为_______ 。
(4)装置G中用到2.00molLNaOH溶液220mL,实验室配制该溶液要用到的所有玻璃仪器有量筒、烧杯、玻璃棒、_______ 、_______ 。在配制过程中,其他操作都是正确的,下列操作会引起所配溶液浓度偏高的是_______ (填序号)。
①没有洗涤烧杯和玻璃棒
②转移溶液时不慎有少量洒到容量瓶外面
③容量瓶不干燥,含有少量蒸馏水
④定容时俯视刻度线
⑤未冷却至室温就将溶液转移到容量瓶并定容
⑥摇匀,静置后,液面低于刻度线,再加水至刻度线

回答下列问题:
(1)仪器a的名称是
(2)实验结束时,应先熄灭
(3)装置G发生反应的离子方程式为
(4)装置G中用到2.00molLNaOH溶液220mL,实验室配制该溶液要用到的所有玻璃仪器有量筒、烧杯、玻璃棒、
①没有洗涤烧杯和玻璃棒
②转移溶液时不慎有少量洒到容量瓶外面
③容量瓶不干燥,含有少量蒸馏水
④定容时俯视刻度线
⑤未冷却至室温就将溶液转移到容量瓶并定容
⑥摇匀,静置后,液面低于刻度线,再加水至刻度线
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】实验室需要0.1 mol/L NaOH溶液450 mL和0.5mol/L硫酸溶液480 mL。根据这两种溶液的配制情况回答下列问题:
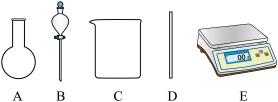
(1)如图所示的仪器中配制溶液需要的是_______ (填字号),配制上述溶液还需用到的玻璃仪器是_______ (填仪器名称)。

(2)下列操作中,是容量瓶所具备的功能有_______ 。
A.配制一定体积准确浓度的标准溶液 B.贮存溶液
C.配制任意浓度和体积的标准溶液 D.稀释某一浓度的溶液 E.量取一定体积的液体
(3)根据计算用托盘天平称取NaOH的质量为_______ g。在实验中其他操作均正确,若定容时俯视刻度线,则所得溶液浓度_______ (填“大于”“等于”或“小于”)0.1 mol/L。若NaOH溶液在转移至容量瓶时,洒落了少许,则需要如何操作:_______ 。
(4)根据计算得知,所需质量分数为98%、密度为l.84 g/cm3的浓硫酸的体积为_______ ml。如果实验室有10 mL,15 mL,20 mL量筒,应选用_______ mL的量筒最好。配制过程中需先在烧杯中将浓硫酸进行稀释,稀释时操作方法是_______ 。
(5)下列操作会使配制的NaOH溶液浓度偏低_______ 的是。
A.用滤纸称量NaOH B.选用的容量瓶内有少量蒸馏水
C.定容摇匀后,液面下降,又加水至刻度线 D.整个配制过程中,容量瓶不振荡
(1)如图所示的仪器中配制溶液需要的是

(2)下列操作中,是容量瓶所具备的功能有
A.配制一定体积准确浓度的标准溶液 B.贮存溶液
C.配制任意浓度和体积的标准溶液 D.稀释某一浓度的溶液 E.量取一定体积的液体
(3)根据计算用托盘天平称取NaOH的质量为
(4)根据计算得知,所需质量分数为98%、密度为l.84 g/cm3的浓硫酸的体积为
(5)下列操作会使配制的NaOH溶液浓度偏低
A.用滤纸称量NaOH B.选用的容量瓶内有少量蒸馏水
C.定容摇匀后,液面下降,又加水至刻度线 D.整个配制过程中,容量瓶不振荡
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】实验室用固体烧碱配制480mL0.1mol⋅L−1NaOH溶液。
(1)配制上述溶液时需称量NaOH固体的质量为__________ g(保留两位小数)
(2)配制过程中不需要使用下列仪器中的_______ (填仪器序号),其中还缺少的玻璃仪器是_________ 、___________ (填仪器名称)。_______ 。
A.用适量蒸馏水洗涤烧杯和玻璃棒2~3次,洗涤液均注入容量瓶,振荡
B.在盛有NaOH固体的烧杯中加入适量蒸馏水溶解
C.将烧杯中已冷却的溶液沿玻璃棒注入容量瓶中
D.将容量瓶盖紧,反复上下颠倒,摇匀
E.改用胶头滴管加蒸馏水,使溶液凹液面恰好与刻度线相切
F.继续往容量瓶内小心加蒸馏水,直到液面接近刻度线1~2cm处
(4)在容量瓶内确定溶液体积的过程中,当液面离容量瓶颈部的刻度线1~2cm时的做法是_______
(5)下列的实验操作可能导致配制的溶液浓度偏高的是(填序号)_______ 。
①称量NaOH固体时,砝码生锈
②移液时,未洗涤烧杯和玻璃棒
③定容时俯视容量瓶刻度线
④摇匀后液面低于刻度线,继续加水至刻度线
⑤容量瓶内有少量水
(1)配制上述溶液时需称量NaOH固体的质量为
(2)配制过程中不需要使用下列仪器中的
A.用适量蒸馏水洗涤烧杯和玻璃棒2~3次,洗涤液均注入容量瓶,振荡
B.在盛有NaOH固体的烧杯中加入适量蒸馏水溶解
C.将烧杯中已冷却的溶液沿玻璃棒注入容量瓶中
D.将容量瓶盖紧,反复上下颠倒,摇匀
E.改用胶头滴管加蒸馏水,使溶液凹液面恰好与刻度线相切
F.继续往容量瓶内小心加蒸馏水,直到液面接近刻度线1~2cm处
(4)在容量瓶内确定溶液体积的过程中,当液面离容量瓶颈部的刻度线1~2cm时的做法是
(5)下列的实验操作可能导致配制的溶液浓度偏高的是(填序号)
①称量NaOH固体时,砝码生锈
②移液时,未洗涤烧杯和玻璃棒
③定容时俯视容量瓶刻度线
④摇匀后液面低于刻度线,继续加水至刻度线
⑤容量瓶内有少量水
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】某化学兴趣小组利用某工业废铁屑制备食品添加剂FeSO4·7H2O,流程图如下:
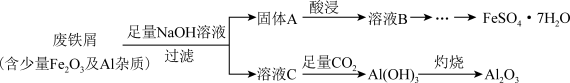
请回答:
(1)请写出废铁屑中加入足量NaOH溶液的化学方程式___________ 。
(2)“酸浸”过程中属于非氧化还原反应的离子方程式___________ 。
(3)“灼烧”操作应选择下列哪一种仪器___________(填序号)。
(4)若要从稀溶液B得到FeSO4·7H2O绿矾晶体,必须进行的实验操作步骤:___________ 、___________ 、过滤、洗涤、自然干燥。
(5)该实验需要用到0.5mol·L-1NaOH溶液240mL,现用固体NaOH进行配制。
①配制时需用托盘天平称量___________ g_NaOH固体。
②下列说法正确的是___________ 。
A.容量瓶经蒸馏水洗涤后,有少量蒸馏水残留,不影响使用
B.容量瓶在实验室可用于存放试剂
C.配制时,NaOH固体溶解后,立即用玻璃棒引流至容量瓶中,然后缓慢加水至刻度线1~2cm处,再滴加蒸馏水至刻度线
D.定容时若俯视刻度线,则会使所配溶液的浓度偏低
E.称取的NaOH固体中若含有Na2O杂质,会导致所配溶液的浓度偏高

请回答:
(1)请写出废铁屑中加入足量NaOH溶液的化学方程式
(2)“酸浸”过程中属于非氧化还原反应的离子方程式
(3)“灼烧”操作应选择下列哪一种仪器___________(填序号)。
A. | B.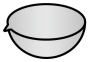 | C.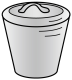 | D. |
(4)若要从稀溶液B得到FeSO4·7H2O绿矾晶体,必须进行的实验操作步骤:
(5)该实验需要用到0.5mol·L-1NaOH溶液240mL,现用固体NaOH进行配制。
①配制时需用托盘天平称量
②下列说法正确的是
A.容量瓶经蒸馏水洗涤后,有少量蒸馏水残留,不影响使用
B.容量瓶在实验室可用于存放试剂
C.配制时,NaOH固体溶解后,立即用玻璃棒引流至容量瓶中,然后缓慢加水至刻度线1~2cm处,再滴加蒸馏水至刻度线
D.定容时若俯视刻度线,则会使所配溶液的浓度偏低
E.称取的NaOH固体中若含有Na2O杂质,会导致所配溶液的浓度偏高
您最近一年使用:0次



