某化合物X由四种短周期元素组成,为探究X的组成设计如下实验。
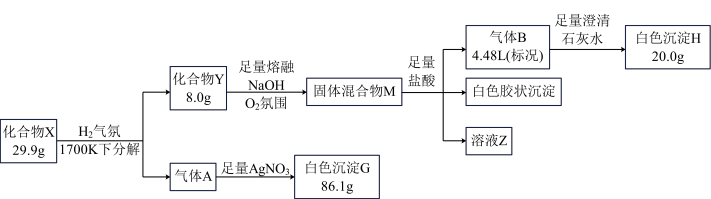
已知:化合物Y由两种元素按原子比1∶1组成,回答下列问题。
(1)X的组成元素为____________________ (填元素符号); 的化学式是
的化学式是____________________ 。
(2)写出化合物 在
在 氛围下分解的化学方程式
氛围下分解的化学方程式________________________________________ 。
(3)写出固体混合物M的组成:__________________________________________________ 。
(4)设计实验检验 溶液中的阳离子:
溶液中的阳离子:______________________________

已知:化合物Y由两种元素按原子比1∶1组成,回答下列问题。
(1)X的组成元素为
 的化学式是
的化学式是(2)写出化合物
 在
在 氛围下分解的化学方程式
氛围下分解的化学方程式(3)写出固体混合物M的组成:
(4)设计实验检验
 溶液中的阳离子:
溶液中的阳离子:
更新时间:2023-08-20 20:18:51
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
【推荐1】某无色混合物水溶液,可能含有以下离子中的若干种:K+、NH 、Mg2+、Cu2+、Cl-、CO
、Mg2+、Cu2+、Cl-、CO 、SO
、SO ,现各取100mL溶液三份进行如下实验:①向第一份加入AgNO3溶液,有白色沉淀产生;②向第二份加入足量NaOH溶液后加热,收集到气体0.896L(标准状况);③向第三份加入足量BaCl2溶液,得到沉淀6.27克,经足量盐酸洗涤后,剩余2.33克。
,现各取100mL溶液三份进行如下实验:①向第一份加入AgNO3溶液,有白色沉淀产生;②向第二份加入足量NaOH溶液后加热,收集到气体0.896L(标准状况);③向第三份加入足量BaCl2溶液,得到沉淀6.27克,经足量盐酸洗涤后,剩余2.33克。
试回答下列问题:
(1)肯定存在的离子有___________ ,肯定不存在的离子有___________ ;
(2)可能存在的离子是___________ ,判断该离子存在与否的方法是___________
(3)试计算肯定存在中阳离子在原溶液中的物质的量浓度___________ 。
 、Mg2+、Cu2+、Cl-、CO
、Mg2+、Cu2+、Cl-、CO 、SO
、SO ,现各取100mL溶液三份进行如下实验:①向第一份加入AgNO3溶液,有白色沉淀产生;②向第二份加入足量NaOH溶液后加热,收集到气体0.896L(标准状况);③向第三份加入足量BaCl2溶液,得到沉淀6.27克,经足量盐酸洗涤后,剩余2.33克。
,现各取100mL溶液三份进行如下实验:①向第一份加入AgNO3溶液,有白色沉淀产生;②向第二份加入足量NaOH溶液后加热,收集到气体0.896L(标准状况);③向第三份加入足量BaCl2溶液,得到沉淀6.27克,经足量盐酸洗涤后,剩余2.33克。试回答下列问题:
(1)肯定存在的离子有
(2)可能存在的离子是
(3)试计算肯定存在中阳离子在原溶液中的物质的量浓度
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】某强酸性溶液X:可能含有Al3+、Ba2+、NH4+、Fe2+、Fe3+、CO32-、SO42-、SiO32-、NO3-中的一种或几种离子,取该溶液进行实验,转化关系如图所示。反应过程中有一种气体在空气中会变为红棕色。回答下列问题:
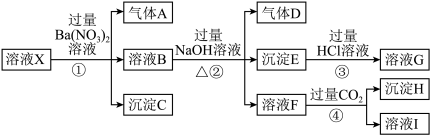
(1)沉淀C是___ (填化学式),由此可确定溶液X中肯定不存在的阳离子有___ 。
(2)气体A是___ (填化学式),产生气体A的离子方程式为___ 。
(3)步骤④中发生反应的离子方程式为___ 。
(4)根据题给信息和图中转化关系,可以确定溶液X中肯定存在的离子有___ ,可能存在的离子有___ 。

(1)沉淀C是
(2)气体A是
(3)步骤④中发生反应的离子方程式为
(4)根据题给信息和图中转化关系,可以确定溶液X中肯定存在的离子有
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】大气中硫、氮的氧化物是形成酸雨的主要物质。某地酸雨中可能含有下列离子: 、
、 、
、 、
、 、
、 、
、 、
、 、
、 等。某研究小组取该地一定量的酸雨,浓缩后将所得澄清试液分成3份,进行如下实验:
等。某研究小组取该地一定量的酸雨,浓缩后将所得澄清试液分成3份,进行如下实验:
请回答下列问题:
(1)根据实验结果判断该酸雨中肯定不存在的离子是_______ ,不能确定的离子有_______ 。
(2)写出第一份试液中发生的反应的离子方程式:_______ 。
(3)写出bc段的离子方程式:_______ 。
(4)设计实验方案,检验该溶液中是否存在 :
:_______ 。
 、
、 、
、 、
、 、
、 、
、 、
、 、
、 等。某研究小组取该地一定量的酸雨,浓缩后将所得澄清试液分成3份,进行如下实验:
等。某研究小组取该地一定量的酸雨,浓缩后将所得澄清试液分成3份,进行如下实验:| 试样 | 所加试剂 | 实验现象 |
| 第一份试液 | 加入少量 片 片 |  片逐渐溶解,溶液颜色变蓝,试管上方有红棕色气体产生 片逐渐溶解,溶液颜色变蓝,试管上方有红棕色气体产生 |
| 第二份试液 | 滴加用盐酸酸化的 溶液 溶液 | 有白色沉淀 |
| 第三份试液 | 滴加 溶液,加热,加入的 溶液,加热,加入的 溶液体积(V)与生成的沉淀、产生的气体(n)的关系如图 溶液体积(V)与生成的沉淀、产生的气体(n)的关系如图 |
|
(1)根据实验结果判断该酸雨中肯定不存在的离子是
(2)写出第一份试液中发生的反应的离子方程式:
(3)写出bc段的离子方程式:
(4)设计实验方案,检验该溶液中是否存在
 :
:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
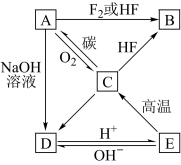
【推荐1】图中X、Y、Z为单质,其它为化合物,它们之间存在如图转化关系(部分产物已略去)。其中,A俗称磁性氧化铁;E是不溶于水的酸性氧化物,能与氢氟酸反应。

回答下列问题:
(1)1mol E中含有_______ mol化学键;M中存在的化学键类型为_________ ;
R的化学式是______________ 。
(2)一定条件下,Z与H2反应生成ZH4,ZH4的电子式为___________________ 。
(3)写出A与Al反应转化为X的化学方程式___________________________ 。
(4)写出A和D的稀溶液反应生成G的离子方程式并标出电子转移的方向和数目_________________ 。

回答下列问题:
(1)1mol E中含有
R的化学式是
(2)一定条件下,Z与H2反应生成ZH4,ZH4的电子式为
(3)写出A与Al反应转化为X的化学方程式
(4)写出A和D的稀溶液反应生成G的离子方程式并标出电子转移的方向和数目
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】某无色澄清溶液中Cl-浓度为0.5 mol·L-1,还可能含有下表中的若干种离子。
现取该溶液100 mL进行如下实验(气体体积均在标准状况下测定)。
请回答下列问题:
(1)通过以上实验不能确定是否存在的离子有______________ 。能确定一定不存在的离子是_____________________________________________________ 。
(2)实验Ⅰ中生成沉淀的离子方程式为_____________________________ 。
(3)通过实验Ⅰ、Ⅱ、Ⅲ和必要计算,请写出一定存在的阴离子______________ (不一定要填满)。
(4)判断K+是否存在,若存在,求出其最小浓度,若不存在说明理由:_____________________ 。
| 阳离子 | K+、Al3+、Mg2+、Ba2+、Fe3+ |
| 阴离子 | NO3-、CO32-、SiO32-、SO42-、OH- |
| 序号 | 实验内容 | 实验结果 |
| Ⅰ | 向该溶液中加入足量稀盐酸 | 产生白色沉淀并放出标准状况下1.12 L气体 |
| Ⅱ | 将Ⅰ的反应混合液过滤,对沉淀洗涤、灼烧至恒重,称量所得固体质量 | 固体质量为4.8 g |
| Ⅲ | 向Ⅱ的滤液中滴加BaCl2溶液 | 无明显现象 |
(1)通过以上实验不能确定是否存在的离子有
(2)实验Ⅰ中生成沉淀的离子方程式为
(3)通过实验Ⅰ、Ⅱ、Ⅲ和必要计算,请写出一定存在的阴离子
(4)判断K+是否存在,若存在,求出其最小浓度,若不存在说明理由:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐1】有A、B、C三种不溶于水的固体。A是某元素的一种单质,它在氧气中完全燃烧得到一种无色气体,此气体能使澄清石灰水变浑浊,另外测得这种气体密度为同温、同压下氧气密度的1.375倍。B固体能溶于热氢氧化钠溶液,再往所得溶液中加入过量盐酸时,析出白色胶状沉淀D。此沉淀干燥后,成为不溶于水的白色粉末,这是一种比碳酸酸性还弱的酸。将B与石灰石、纯碱按比例混合加热得到C,C在高温时软化,无固定熔点。
(1)根据以上事实,形成单质A的元素名称为__ , C的名称为__ 。
(2)B固体溶于热氢氧化钠溶液的化学方程式是__ 。
(3)生成白色胶状沉淀D的化学方程式是__ 。
(4)由B制取C的化学方程式是__ 。
(1)根据以上事实,形成单质A的元素名称为
(2)B固体溶于热氢氧化钠溶液的化学方程式是
(3)生成白色胶状沉淀D的化学方程式是
(4)由B制取C的化学方程式是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐2】硅在地壳中的含量较高。硅及其化合物的开发由来已久,在现代生活中有广泛应用。
(1)1810年瑞典化学家贝采利乌斯在加热石英砂、木炭和铁时,得到一种“金属”。这种“金属”可能是___________ 。
(2)陶瓷、水泥和玻璃是常用的硅酸盐材料。其中,生产普通玻璃的主要原料有___________ 。
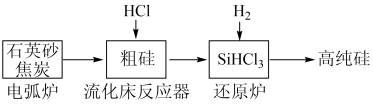
(3)高纯硅是现代信息、半导体和光伏发电等产业都需要的基础材料。工业上提纯硅有多种技术路线,其中一种工艺流程示意图及主要反应如图:
①用石英砂和焦炭在电弧炉中高温加热也可以生产碳化硅,该反应的化学方程式为___________ ;碳化硅又称___________ ,其晶体结构与___________ 相似。
②在流化床反应的产物中,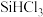 大约占
大约占 ,还有
,还有 等,有关物质的沸点数据如表,提纯
等,有关物质的沸点数据如表,提纯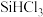 的主要工艺操作依次是沉降、冷凝和
的主要工艺操作依次是沉降、冷凝和___________ 。
③反应ii和反应iii___________ (填“是”或“不是”)可逆反应,原因是___________ 。
(1)1810年瑞典化学家贝采利乌斯在加热石英砂、木炭和铁时,得到一种“金属”。这种“金属”可能是
(2)陶瓷、水泥和玻璃是常用的硅酸盐材料。其中,生产普通玻璃的主要原料有
(3)高纯硅是现代信息、半导体和光伏发电等产业都需要的基础材料。工业上提纯硅有多种技术路线,其中一种工艺流程示意图及主要反应如图:
| 项目 | 发生的主要反应 |
| 电弧炉 | i.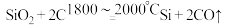 |
| 流化床反应器 | ii. |
| 还原炉 | iii.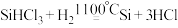 |
②在流化床反应的产物中,
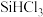 大约占
大约占 ,还有
,还有 等,有关物质的沸点数据如表,提纯
等,有关物质的沸点数据如表,提纯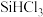 的主要工艺操作依次是沉降、冷凝和
的主要工艺操作依次是沉降、冷凝和| 物质 | 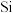 | 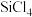 | 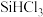 | 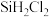 |  |  | 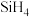 |
沸点/ | 2355 | 57.6 | 31.8 | 8.2 | 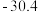 | 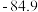 |  |
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】硅单质及其化合物应用广泛。请回答下列问题:
(1)传统的无机非金属材料多为硅酸盐材料,主要包括陶瓷、水泥和玻璃,其中制玻璃的主要原料为_______ 。
(2)下列溶液的存放不能使用磨口玻璃塞的是_______ (填序号)。
①浓硝酸 ② 溶液 ③
溶液 ③ 溶液 ④澄清石灰水 ⑤
溶液 ④澄清石灰水 ⑤ 溶液 ⑥
溶液 ⑥ 溶液 ⑦
溶液 ⑦ 溶液
溶液
(3)关于硅及其相关化合物的叙述正确的是_______ (填字母)。
A.自然界中存在天然游离的硅单质
B.已知C与Si的最高正价都是正四价,由于CO2+H2O=H2CO3,用类比法可知,SiO2+H2O=H2SiO3
C.无机非金属材料AlN熔沸点很高,可作为耐高温材料制作特定仪器
D.保存氢氟酸可用玻璃瓶,但不能用玻璃塞
E. 既能和
既能和 溶液反应,又能和氢氟酸反应,所以是两性氧化物
溶液反应,又能和氢氟酸反应,所以是两性氧化物
F.高纯硅可用于制作光导纤维
(4)硅单质可作为硅半导体材料。三氯甲硅烷(SiHCl3)还原法是当前制备高纯硅的主要方法,生产过程如图:_______ 。
②上述工艺生产中循环使用的物质除Si、SiHCl3外,还有_______ 。
③整个制备过程必须严格控制无水无氧。 遇水剧烈反应生成H2SiO3、HCl和一种气体单质,写出发生反应的化学方程式
遇水剧烈反应生成H2SiO3、HCl和一种气体单质,写出发生反应的化学方程式_______ ;在制备高纯硅的过程中若混入 ,可能引起的后果是
,可能引起的后果是_______ 。
(5)新型陶瓷材料氮化硅(Si3N4)可应用于原子反应堆,一种制备氮化硅的反应如下: 3SiO2+6C+2N2 Si3N4+6CO,若生成标准状况下33.6LCO时,反应过程中转移的电子数为
Si3N4+6CO,若生成标准状况下33.6LCO时,反应过程中转移的电子数为_______  。
。
(1)传统的无机非金属材料多为硅酸盐材料,主要包括陶瓷、水泥和玻璃,其中制玻璃的主要原料为
(2)下列溶液的存放不能使用磨口玻璃塞的是
①浓硝酸 ②
 溶液 ③
溶液 ③ 溶液 ④澄清石灰水 ⑤
溶液 ④澄清石灰水 ⑤ 溶液 ⑥
溶液 ⑥ 溶液 ⑦
溶液 ⑦ 溶液
溶液(3)关于硅及其相关化合物的叙述正确的是
A.自然界中存在天然游离的硅单质
B.已知C与Si的最高正价都是正四价,由于CO2+H2O=H2CO3,用类比法可知,SiO2+H2O=H2SiO3
C.无机非金属材料AlN熔沸点很高,可作为耐高温材料制作特定仪器
D.保存氢氟酸可用玻璃瓶,但不能用玻璃塞
E.
 既能和
既能和 溶液反应,又能和氢氟酸反应,所以是两性氧化物
溶液反应,又能和氢氟酸反应,所以是两性氧化物F.高纯硅可用于制作光导纤维
(4)硅单质可作为硅半导体材料。三氯甲硅烷(SiHCl3)还原法是当前制备高纯硅的主要方法,生产过程如图:

②上述工艺生产中循环使用的物质除Si、SiHCl3外,还有
③整个制备过程必须严格控制无水无氧。
 遇水剧烈反应生成H2SiO3、HCl和一种气体单质,写出发生反应的化学方程式
遇水剧烈反应生成H2SiO3、HCl和一种气体单质,写出发生反应的化学方程式 ,可能引起的后果是
,可能引起的后果是(5)新型陶瓷材料氮化硅(Si3N4)可应用于原子反应堆,一种制备氮化硅的反应如下: 3SiO2+6C+2N2
 Si3N4+6CO,若生成标准状况下33.6LCO时,反应过程中转移的电子数为
Si3N4+6CO,若生成标准状况下33.6LCO时,反应过程中转移的电子数为 。
。
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】有X、Y、A、B、C、D、E七种物质,其中X、Y是与呼吸有关的两种气体,A是单质,B、C、D、E是化合物,其焰色反应均为黄色,它们之间具有下列转化关系(部分反应物、产物已略去)。
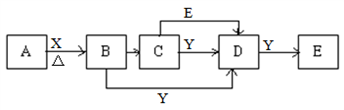
请回答下列问题:
(1)A是_____ ,少量的A保存在______________ ;B的主要用途是_____ (答出一点即可),E的俗名是_____ ;
(2)C与E反应的离子方程式是______________________________ ;
(3)D与Y反应的化学方程式是___________________________ ;
(4)将D固体置于圆底烧瓶中,利用下图装置(夹持固定装置已略去)进行实验可在V中收集到纯净的气体X,装置III中产生白色沉淀。
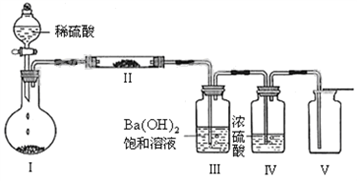
则装置Ⅱ中物质的化学式是_______ ,Ⅱ中主要反应的化学方程式是__________________ ,Ⅲ的作用是___________ 。生成1molX气体,转移电子为________ mol。

请回答下列问题:
(1)A是
(2)C与E反应的离子方程式是
(3)D与Y反应的化学方程式是
(4)将D固体置于圆底烧瓶中,利用下图装置(夹持固定装置已略去)进行实验可在V中收集到纯净的气体X,装置III中产生白色沉淀。

则装置Ⅱ中物质的化学式是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】无水氯化铝是有机化工常用的催化剂,氯化铝178 ℃时升华,极易潮解,遇水发热并产生白色烟雾。氯化铝还易溶于乙醇、氯仿和四氯化碳。实验室可用反应2Al+6HCl(g)  2AlCl3+3H2制备少量无水氯化铝,某同学利用该原理设计如下实验装置:
2AlCl3+3H2制备少量无水氯化铝,某同学利用该原理设计如下实验装置:
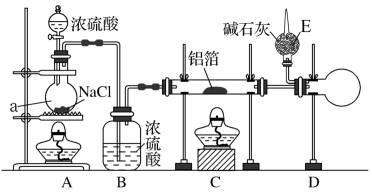
注意,盐酸极易挥发,装置A内利用此特点制备HCl气体: H2SO4(浓)+2NaCl Na2SO4+2HCl↑
Na2SO4+2HCl↑
(1)仪器a的名称____________ ,反应后a中溶液的焰色反应颜色是________
(2)以下三步操作的先后顺序为________ (填序号)。
①点燃A处酒精灯 ②点燃C处酒精灯 ③滴加A处浓硫酸
(3)E干燥管内碱石灰的作用是____________ 。
(4)若将2.67 gAlCl3溶解并配置成800 mL溶液,则溶液中c(Cl-)=___ mol·L-1
 2AlCl3+3H2制备少量无水氯化铝,某同学利用该原理设计如下实验装置:
2AlCl3+3H2制备少量无水氯化铝,某同学利用该原理设计如下实验装置:
注意,盐酸极易挥发,装置A内利用此特点制备HCl气体: H2SO4(浓)+2NaCl
 Na2SO4+2HCl↑
Na2SO4+2HCl↑(1)仪器a的名称
(2)以下三步操作的先后顺序为
①点燃A处酒精灯 ②点燃C处酒精灯 ③滴加A处浓硫酸
(3)E干燥管内碱石灰的作用是
(4)若将2.67 gAlCl3溶解并配置成800 mL溶液,则溶液中c(Cl-)=
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】某废水含有下列离子中的5种(忽略水的电离及离子的水解):K+、Cu2+、Al3+、Fe2+、Cl-、CO 、NO
、NO 、SO
、SO ,若各种离子的物质的量浓度相等,为探究废水的组成,某同学进行了如下实验:
,若各种离子的物质的量浓度相等,为探究废水的组成,某同学进行了如下实验:
①用铂丝蘸取少量溶液,在火焰上灼烧,透过蓝色钴玻璃观察无紫色火焰;
②另取少量溶液加入足量稀盐酸,有无色气体生成,该无色气体遇空气变成红棕色,此时溶液依然澄清,且溶液中阴离子种类不变;
③另取少量溶液加入BaCl2溶液,有白色沉淀生成。
根据上述实验,回答下列问题:
(1)由②判断,溶液中一定含有的阳离子为___ ,将生成的红棕色气体通入水中,气体变为无色,所发生反应的化学方程式为___ 。
(2)步骤③中生成白色的沉淀的离子方程式为:____ 。
(3)可以确定存在的离子:____ 。
(4)可以确定不存在的离子:____ 。
 、NO
、NO 、SO
、SO ,若各种离子的物质的量浓度相等,为探究废水的组成,某同学进行了如下实验:
,若各种离子的物质的量浓度相等,为探究废水的组成,某同学进行了如下实验:①用铂丝蘸取少量溶液,在火焰上灼烧,透过蓝色钴玻璃观察无紫色火焰;
②另取少量溶液加入足量稀盐酸,有无色气体生成,该无色气体遇空气变成红棕色,此时溶液依然澄清,且溶液中阴离子种类不变;
③另取少量溶液加入BaCl2溶液,有白色沉淀生成。
根据上述实验,回答下列问题:
(1)由②判断,溶液中一定含有的阳离子为
(2)步骤③中生成白色的沉淀的离子方程式为:
(3)可以确定存在的离子:
(4)可以确定不存在的离子:
您最近一年使用:0次