某化学小组欲测定一份长期放置的补铁药品(有效成分是琥珀酸亚铁,化学式为FeC4H4O4)是否已变质,实验如下:
Ⅰ.取补铁药样品10.00g,碾碎,溶于100.0mL稀盐酸中,过滤,滤液呈浅黄绿色;
Ⅱ.取少量滤液,滴加KSCN溶液,溶液变为浅红色,再滴入3滴H2O2溶液,溶液红色加深;
Ⅲ.准确量取I中滤液20.00mL,加入足量H2O2溶液,再加入足量NaOH溶液,过滤、洗涤、常温晾干,获得Fe(OH)3固体0.642g;
Ⅳ.再准确量取I中滤液20.00mL于大试管中,加入1.00g铜粉,用胶塞塞紧试管口,充分振荡后过滤,最后得到干燥的铜粉0.936g。
(1)I中琥珀酸亚铁与稀盐酸反应生成FeCl2和琥珀酸(分子式为C4H6O4),说明酸性:C4H6O4_______ HCl(填“>”或“<”)。
(2)用离子方程式解释II中实验现象产生的原因:_______ 、Fe3++3SCN-=Fe(SCN)3。
(3)IV中发生反应的离子方程式为_______ 。
(4)该补铁药中琥珀酸亚铁变质程度为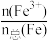 ×100%=
×100%=_______ (保留3位有效数字)。
(5)IV中溶液与铜粉反应时必须使用胶塞塞紧试管口,原因是_______ 。
Ⅰ.取补铁药样品10.00g,碾碎,溶于100.0mL稀盐酸中,过滤,滤液呈浅黄绿色;
Ⅱ.取少量滤液,滴加KSCN溶液,溶液变为浅红色,再滴入3滴H2O2溶液,溶液红色加深;
Ⅲ.准确量取I中滤液20.00mL,加入足量H2O2溶液,再加入足量NaOH溶液,过滤、洗涤、常温晾干,获得Fe(OH)3固体0.642g;
Ⅳ.再准确量取I中滤液20.00mL于大试管中,加入1.00g铜粉,用胶塞塞紧试管口,充分振荡后过滤,最后得到干燥的铜粉0.936g。
(1)I中琥珀酸亚铁与稀盐酸反应生成FeCl2和琥珀酸(分子式为C4H6O4),说明酸性:C4H6O4
(2)用离子方程式解释II中实验现象产生的原因:
(3)IV中发生反应的离子方程式为
(4)该补铁药中琥珀酸亚铁变质程度为
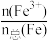 ×100%=
×100%=(5)IV中溶液与铜粉反应时必须使用胶塞塞紧试管口,原因是
更新时间:2023-08-26 13:31:14
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
名校
【推荐1】粗盐中常含有MgCl2、CaCl2等杂质,提纯粗盐的工艺流程如图所示。回答下列问题:

(1)粗盐水中含有NaCl、CaCl2和MgCl2:
①CaCl2从组成的阳离子来看,属于________ 盐。
②常温下,仅由MgCl2形成的水溶液,________ (填“能”或“不能”)发生丁达尔效应。
(2)步骤Ⅰ中MgCl2与氢氧化钠溶液发生反应的离子方程式为________ 。
(3)步骤Ⅱ中的生成物为CaCO3,该物质中氧元素的质量分数为________ 。
(4)进行操作a时,所用到的装置如图所示(滤纸已略去):
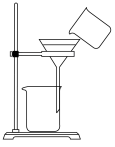
①该装置的错误有________ 处,请指出其错误:________ (写一处即可)。
②过滤后,若往漏斗下端的烧杯中滴入几滴红色石蕊试液,可观察到的现象为________ 。
(5)操作b为蒸发浓缩、冷却结晶,该过程中除了能将水蒸发,还能将过量的稀盐酸除去,主要利用了稀盐酸的________ (填“易挥发性”或“酸性”)。

(1)粗盐水中含有NaCl、CaCl2和MgCl2:
①CaCl2从组成的阳离子来看,属于
②常温下,仅由MgCl2形成的水溶液,
(2)步骤Ⅰ中MgCl2与氢氧化钠溶液发生反应的离子方程式为
(3)步骤Ⅱ中的生成物为CaCO3,该物质中氧元素的质量分数为
(4)进行操作a时,所用到的装置如图所示(滤纸已略去):

①该装置的错误有
②过滤后,若往漏斗下端的烧杯中滴入几滴红色石蕊试液,可观察到的现象为
(5)操作b为蒸发浓缩、冷却结晶,该过程中除了能将水蒸发,还能将过量的稀盐酸除去,主要利用了稀盐酸的
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】化学研究源于实验与理论的结合,得于科学的推断与探究
(1)二氧化氯是一种高效消毒剂。工业制备 的反应为:
的反应为: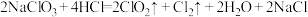
①氧化性:
___________ (填“>”或“<”) 。
。
② 在杀菌消毒过程中会产生副产物亚氯酸盐
在杀菌消毒过程中会产生副产物亚氯酸盐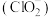 ,需将其转化为
,需将其转化为 除去,下列试剂中可将
除去,下列试剂中可将 转化为
转化为 的是
的是___________ (填字母)。
a. b.
b. c.
c. d.
d.
(2) 为爆炸物,在某温度下按下式进行分解:
为爆炸物,在某温度下按下式进行分解: ,则被氧化和被还原的氮元素质量之比为
,则被氧化和被还原的氮元素质量之比为___________ 。
(3)设 为阿伏伽德罗常数的值。
为阿伏伽德罗常数的值。 是一种氧化剂,与
是一种氧化剂,与 完全反应转移的电子数目为
完全反应转移的电子数目为___________ 。(已知该反应为置换反应)
(4)在 浓度为
浓度为 的某澄清溶液中,还可能含有下表中的若干种离子:
的某澄清溶液中,还可能含有下表中的若干种离子:
取该溶液 进行如下实验(气体体积在标准状况下测定):
进行如下实验(气体体积在标准状况下测定):
将一定含有的离子及物质的量浓度填入下表(可不必填满)
(5)A、B、C、D、E五瓶透明溶液分别是 溶液、
溶液、 溶液、
溶液、 溶液、
溶液、 溶液、
溶液、 溶液中的一种。已知:①A与D应有气体生成,②A与E反应有沉淀生成,③B与E反应有沉淀生成,④B与C反应有沉淀生成,⑤C与D反应有气体生成,⑥在②和③的反应中生成的沉淀是同一种物质。请回答下列问题:
溶液中的一种。已知:①A与D应有气体生成,②A与E反应有沉淀生成,③B与E反应有沉淀生成,④B与C反应有沉淀生成,⑤C与D反应有气体生成,⑥在②和③的反应中生成的沉淀是同一种物质。请回答下列问题:
i.A与D反应产生气体的离子方程式为_______ 。
ii.向一定量的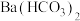 溶液中逐滴加入C溶液,直至不再生成沉淀,该过程中发生反应的离子方程式为
溶液中逐滴加入C溶液,直至不再生成沉淀,该过程中发生反应的离子方程式为_______ ,沉淀完全后,继续滴加C溶液,此时发生反应的离子方程式为_______ 。
(1)二氧化氯是一种高效消毒剂。工业制备
 的反应为:
的反应为: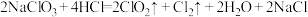
①氧化性:

 。
。②
 在杀菌消毒过程中会产生副产物亚氯酸盐
在杀菌消毒过程中会产生副产物亚氯酸盐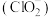 ,需将其转化为
,需将其转化为 除去,下列试剂中可将
除去,下列试剂中可将 转化为
转化为 的是
的是a.
 b.
b. c.
c. d.
d.
(2)
 为爆炸物,在某温度下按下式进行分解:
为爆炸物,在某温度下按下式进行分解: ,则被氧化和被还原的氮元素质量之比为
,则被氧化和被还原的氮元素质量之比为(3)设
 为阿伏伽德罗常数的值。
为阿伏伽德罗常数的值。 是一种氧化剂,与
是一种氧化剂,与 完全反应转移的电子数目为
完全反应转移的电子数目为(4)在
 浓度为
浓度为 的某澄清溶液中,还可能含有下表中的若干种离子:
的某澄清溶液中,还可能含有下表中的若干种离子:| 阳离子 | 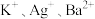 |
| 阴离子 |  |
 进行如下实验(气体体积在标准状况下测定):
进行如下实验(气体体积在标准状况下测定):| 序号 | 实验内容 | 实验结果 |
| I | 向该溶液中加入足量稀 | 产生白色沉淀并放出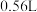 气体 气体 |
| II | 将的反应混合液过滤,对沉淀洗涤、灼 烧至恒重,称量所得固体质量 | 固体质量为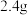 |
| III | 在II的滤液中滴加 溶液 溶液 | 无明显现象 |
| 一定含有的离子 |  | ||||
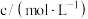 | 0.5 |
 溶液、
溶液、 溶液、
溶液、 溶液、
溶液、 溶液、
溶液、 溶液中的一种。已知:①A与D应有气体生成,②A与E反应有沉淀生成,③B与E反应有沉淀生成,④B与C反应有沉淀生成,⑤C与D反应有气体生成,⑥在②和③的反应中生成的沉淀是同一种物质。请回答下列问题:
溶液中的一种。已知:①A与D应有气体生成,②A与E反应有沉淀生成,③B与E反应有沉淀生成,④B与C反应有沉淀生成,⑤C与D反应有气体生成,⑥在②和③的反应中生成的沉淀是同一种物质。请回答下列问题:i.A与D反应产生气体的离子方程式为
ii.向一定量的
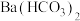 溶液中逐滴加入C溶液,直至不再生成沉淀,该过程中发生反应的离子方程式为
溶液中逐滴加入C溶液,直至不再生成沉淀,该过程中发生反应的离子方程式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】四氢铝锂( )常作为有机合成的重要还原剂。工业上以辉锂矿(主要成分是
)常作为有机合成的重要还原剂。工业上以辉锂矿(主要成分是 ,含少量
,含少量 )为原料合成四氢铝锂的流程如下,回答下列问题:
)为原料合成四氢铝锂的流程如下,回答下列问题:
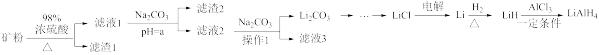
已知: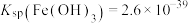 ,
,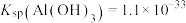 。当离子在溶液中浓度小于或等于
。当离子在溶液中浓度小于或等于 时,认为该离子沉淀完全。
时,认为该离子沉淀完全。
 微溶于水,其饱和溶液的浓度与温度的关系如下表所示:
微溶于水,其饱和溶液的浓度与温度的关系如下表所示:
(1)写出 与浓硫酸反应的离子方程式
与浓硫酸反应的离子方程式_______ 。滤渣2的主要成分为_______ (填化学式)。a的最小值约为_______ 。
(2)操作1的步骤为_______ 。
(3)为测定制备的四氢铝锂( )的纯度,称取样品a g加入水使其完全反应,收集到标准状况下气体b mL。
)的纯度,称取样品a g加入水使其完全反应,收集到标准状况下气体b mL。
① 溶解时发生反应的化学方程式为
溶解时发生反应的化学方程式为_______ 。
②四氢铝锂样品的纯度为_______ %。
 )常作为有机合成的重要还原剂。工业上以辉锂矿(主要成分是
)常作为有机合成的重要还原剂。工业上以辉锂矿(主要成分是 ,含少量
,含少量 )为原料合成四氢铝锂的流程如下,回答下列问题:
)为原料合成四氢铝锂的流程如下,回答下列问题: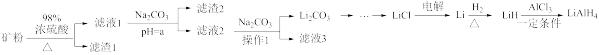
已知:
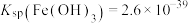 ,
,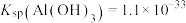 。当离子在溶液中浓度小于或等于
。当离子在溶液中浓度小于或等于 时,认为该离子沉淀完全。
时,认为该离子沉淀完全。 微溶于水,其饱和溶液的浓度与温度的关系如下表所示:
微溶于水,其饱和溶液的浓度与温度的关系如下表所示:| 温度/℃ | 10 | 30 | 60 | 90 |
浓度/( ) ) | 0.21 | 0.17 | 0.14 | 0.10 |
 与浓硫酸反应的离子方程式
与浓硫酸反应的离子方程式(2)操作1的步骤为
(3)为测定制备的四氢铝锂(
 )的纯度,称取样品a g加入水使其完全反应,收集到标准状况下气体b mL。
)的纯度,称取样品a g加入水使其完全反应,收集到标准状况下气体b mL。①
 溶解时发生反应的化学方程式为
溶解时发生反应的化学方程式为②四氢铝锂样品的纯度为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】在下列物质转化关系中,反应的条件和部分产物已略去。
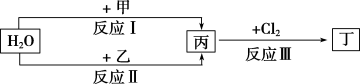
回答下列问题:
(1)若甲、乙是两种常见金属,且反应Ⅲ是工业制盐酸的反应。
①反应Ⅰ中甲在通常条件下和水剧烈反应,除丙外,还生成一种焰色反应为黄色的物质,则工业上生产甲的一般方法是___ 。
A.热分解法 B.热还原法 C.电解法
②反应Ⅱ中乙与H2O在高温下反应,除丙外,还生成一种有磁性的物质,则乙在周期表中的位置为___ ;反应Ⅱ的化学方程式是___ 。
(2)若甲、乙是离子化合物,且反应Ⅲ是工业制漂白粉的反应。
①反应Ⅲ的化学方程式是___ 。
②若反应Ⅰ是实验室制备某气体的反应,该气体分子含14个电子,是直线形结构。则反应Ⅰ的化学方程式是___ 。
③在饱和氯水中加块状石灰石,能制得较浓HClO溶液,同时放出一种气体,其反应的离子方程式是___ ;写出HClO的结构式:___ 。

回答下列问题:
(1)若甲、乙是两种常见金属,且反应Ⅲ是工业制盐酸的反应。
①反应Ⅰ中甲在通常条件下和水剧烈反应,除丙外,还生成一种焰色反应为黄色的物质,则工业上生产甲的一般方法是
A.热分解法 B.热还原法 C.电解法
②反应Ⅱ中乙与H2O在高温下反应,除丙外,还生成一种有磁性的物质,则乙在周期表中的位置为
(2)若甲、乙是离子化合物,且反应Ⅲ是工业制漂白粉的反应。
①反应Ⅲ的化学方程式是
②若反应Ⅰ是实验室制备某气体的反应,该气体分子含14个电子,是直线形结构。则反应Ⅰ的化学方程式是
③在饱和氯水中加块状石灰石,能制得较浓HClO溶液,同时放出一种气体,其反应的离子方程式是
您最近一年使用:0次
【推荐2】某工厂的工业废水中含有大量的 和较多的
和较多的 。为了减少污染并变废为宝,工厂计划从该废水中回收
。为了减少污染并变废为宝,工厂计划从该废水中回收 和金属铜。请根据以下流程图,回答下列问题。
和金属铜。请根据以下流程图,回答下列问题。
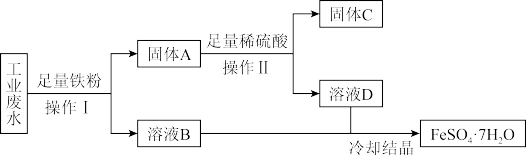
(1)操作Ⅰ的名称是_______ ,固体A是_______ (填化学式),固体C是_______ (填化学式)。
(2)鉴别溶液B中的金属阳离子时,应先滴加的试剂是_______ (填“氯水”或“ 溶液”;下同)无明显现象,再滴加入几滴
溶液”;下同)无明显现象,再滴加入几滴_______ ,溶液变为红色。
(3)若取2 溶液B加入试管中,然后滴加氢氧化钠溶液,产生的现象是
溶液B加入试管中,然后滴加氢氧化钠溶液,产生的现象是_______ ;此过程涉及反应的化学方程式是:_______ 。
(4)为防止 溶液氧化变质,应在溶液中加入少量
溶液氧化变质,应在溶液中加入少量_______ ,其原因是_______ 。
(5)把一定量铁粉放入氯化铁溶液中,完全反应后,所得溶液中 和
和 物质的量浓度恰好相等。则已反应的
物质的量浓度恰好相等。则已反应的 和未反应的
和未反应的 的物质的量之比为
的物质的量之比为_______ 。
 和较多的
和较多的 。为了减少污染并变废为宝,工厂计划从该废水中回收
。为了减少污染并变废为宝,工厂计划从该废水中回收 和金属铜。请根据以下流程图,回答下列问题。
和金属铜。请根据以下流程图,回答下列问题。
(1)操作Ⅰ的名称是
(2)鉴别溶液B中的金属阳离子时,应先滴加的试剂是
 溶液”;下同)无明显现象,再滴加入几滴
溶液”;下同)无明显现象,再滴加入几滴(3)若取2
 溶液B加入试管中,然后滴加氢氧化钠溶液,产生的现象是
溶液B加入试管中,然后滴加氢氧化钠溶液,产生的现象是(4)为防止
 溶液氧化变质,应在溶液中加入少量
溶液氧化变质,应在溶液中加入少量(5)把一定量铁粉放入氯化铁溶液中,完全反应后,所得溶液中
 和
和 物质的量浓度恰好相等。则已反应的
物质的量浓度恰好相等。则已反应的 和未反应的
和未反应的 的物质的量之比为
的物质的量之比为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】已知A是一种具有磁性、银白色的金属单质,B的摩尔质量为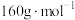 ,F的粒子直径在
,F的粒子直径在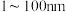 之间。有关A的一些转化如下图所示:
之间。有关A的一些转化如下图所示:
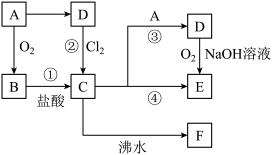
回答下列问题:
(1)B和D的化学式分别为_______ 、_______ 。
(2)①~④中属于化合反应的是_______ (填序号)。
(3)反应③的离子方程式为_______ 。
(4)写出反应①的化学方程式为_______ 。
(5)将C的饱和溶液滴入沸水中,并继续煮沸至红褐色,停止加热制得的分散系F是_______ (填“胶体”或“溶液”),它与C和E的本质区别是_______ 。
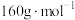 ,F的粒子直径在
,F的粒子直径在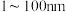 之间。有关A的一些转化如下图所示:
之间。有关A的一些转化如下图所示:
回答下列问题:
(1)B和D的化学式分别为
(2)①~④中属于化合反应的是
(3)反应③的离子方程式为
(4)写出反应①的化学方程式为
(5)将C的饱和溶液滴入沸水中,并继续煮沸至红褐色,停止加热制得的分散系F是
您最近一年使用:0次



