离子键的特征
离子键没有_____ 性和_____ 性。
阴、阳离子在各个方向上都可以与带相反电荷的离子发生静电作用,即没有_____ 性;在静电作用能够达到的范围内,只要空间条件允许,一个离子可以同时吸引多个带相反电荷的离子,即没有_____ 性。
离子键没有
阴、阳离子在各个方向上都可以与带相反电荷的离子发生静电作用,即没有
23-24高二上·全国·课前预习 查看更多[1]
更新时间:2023-07-17 07:53:18
|
相似题推荐
填空题
|
较易
(0.85)
名校
【推荐1】下列变化:①烧碱熔化;② 升华;③
升华;③ 溶于水;④
溶于水;④ 溶于水;⑤
溶于水;⑤ 溶于水;⑥
溶于水;⑥ 受热分解为
受热分解为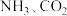 和
和 。其中仅离子键被破坏的是
。其中仅离子键被破坏的是_______ (填序号,下同)仅共价键被破坏的是_______ ;
 升华;③
升华;③ 溶于水;④
溶于水;④ 溶于水;⑤
溶于水;⑤ 溶于水;⑥
溶于水;⑥ 受热分解为
受热分解为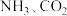 和
和 。其中仅离子键被破坏的是
。其中仅离子键被破坏的是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】下列五种物质中①Ne ②O2 ③NH3 ④ KOH ⑤Na2O(以下填写序号)只存在极性共价键的是____ ,只存在离子键的是______ ,既存在共价键又存在离子键的是_____ ,不存在化学键的是_____ 。属于离子化合物的是:_____ ,属于共价化合物的是:_____
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】用序号按要求回答下列问题:
(1)下列各种物质:①H2O ②NH3 ③KOH ④Na2O2 ⑤MgCl2 ⑥Ne不存在化学键的是______ ;只存在离子键的是______ ;属于共价化合物的是________ ;属于离子化合物的是________ ;含非极性键的离子化合物是 _________ ;含极性键的离子化合物是______ 。
(2)下列变化过程:①碘的升华②NaCl固体溶于水 ③O2溶于水 ④HCl气体溶于水⑤烧碱熔化 ⑥氯化铵受热分解,化学键没有被破坏的是__________ ; 仅破坏离子键的是__________ ;仅破坏共价键的是__________ ;既破坏离子键又破坏共价键的是__________ 。
(1)下列各种物质:①H2O ②NH3 ③KOH ④Na2O2 ⑤MgCl2 ⑥Ne不存在化学键的是
(2)下列变化过程:①碘的升华②NaCl固体溶于水 ③O2溶于水 ④HCl气体溶于水⑤烧碱熔化 ⑥氯化铵受热分解,化学键没有被破坏的是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】试分析下列各种情况下微粒间作用力的变化情况(填“离子键”“极性键”或“非极性键”):
(1)NaCl溶于水时破坏___________ 。
(2)HCl溶于水时破坏___________ 。
(3) 溶于水时破坏
溶于水时破坏___________ 。
(4)NaOH和HCl反应时形成___________ 和___________ 。
(5)反应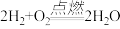 中,被破坏的是
中,被破坏的是___________ ,形成的是___________ 。
(6) 和
和 反应时,被破坏的化学键是
反应时,被破坏的化学键是___________ ,形成的化学键是___________ 。
(7) 熔化时被破坏的化学键是
熔化时被破坏的化学键是___________ 。
(1)NaCl溶于水时破坏
(2)HCl溶于水时破坏
(3)
 溶于水时破坏
溶于水时破坏(4)NaOH和HCl反应时形成
(5)反应
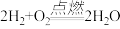 中,被破坏的是
中,被破坏的是(6)
 和
和 反应时,被破坏的化学键是
反应时,被破坏的化学键是(7)
 熔化时被破坏的化学键是
熔化时被破坏的化学键是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】通过前面内容的学习,你一定对物质有了更加深刻的认识。请从不同的角度阐述你对物质组成、结构和分类的认识____ 。
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】工业上最早在19世纪中叶便已生产的过氧化氢,目前成为社会需求量迅速增长的化学品,因为它有较强的氧化性,通常用于污水处理中,氧化除去水中的杂质。在过氧化氢分子中,有1个过氧键:-O-O-,每个氧原子再连接一个氢原子。纯的过氧化氢为蓝色的粘稠状液体,沸点是152.1℃,冰点是-0.89℃。
(1)过氧化氢的电子式为___________ ;
(2)过氧化氢是___________ 化合物(离子或共价);
(3)在低于-0.89℃时,过氧化氢是一种蓝色___________ 态物质,组成它的基本微粒是___________ 。
A.H2O2 B.H和O C.H2和O2 D.H和O2
(1)过氧化氢的电子式为
(2)过氧化氢是
(3)在低于-0.89℃时,过氧化氢是一种蓝色
A.H2O2 B.H和O C.H2和O2 D.H和O2
您最近一年使用:0次



