下列关于2C4H10(g)+13O2(g)=8CO2(g)+10H2O(l) ΔH=-5800kJ·mol-1的叙述错误的是
| A.该反应的焓变ΔH=-5800kJ·mol-1,是放热反应 |
| B.该反应的ΔH与各物质的状态有关,与化学计量数也有关 |
| C.该热化学方程式表示在25℃、101kPa下,2molC4H10气体完全燃烧生成CO2气体和液态水时放出的热量为5800kJ |
| D.该反应表明2mol丁烷燃烧时一定会放出5800kJ的热量 |
22-23高二下·云南普洱·阶段练习 查看更多[4]
四川省绵阳南山中学实验学校2023-2024学年高二上学期9月月考化学试题课时3热化学方程式随堂练习(已下线)专题01 反应热、焓变与热化学方程式【考点清单】(讲+练)-2023-2024学年高二化学期中考点大串讲(人教版2019选择性必修1)云南省普洱市云南省思茅第一中学2022-2023学年高二下学期6月月考化学试题
更新时间:2023/07/23 09:08:22
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】化学里面有很多“类比”,下列有关“类比”的说法正确的是
| A.Na在空气中燃烧生成Na2O2,Li在空气中燃烧也生成Li2O2 |
| B.碳酸钠与盐酸反应放热,碳酸氢钠与盐酸反应也放热 |
| C.Mg、Al与稀硫酸构成的原电池中较活泼的Mg作负极,Mg、Al与NaOH溶液构成的原电池中也是Mg作负极 |
| D.CO2通入紫色石蕊试液能显红色,SO2通入紫色石蕊也能显红色 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】化学反应中往往伴随着能量的变化,下列反应属于吸热反应的是
| A.钠和水的反应 |
| B.氧化钙与水的反应 |
| C.碳与水蒸气的反应 |
| D.甲烷的燃烧反应 |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列认识正确的是
| A.热化学方程式中,如果没有注明温度和压强,则表示反应热是在标准状况下测得的数据 |
| B.破坏反应物全部化学键所需能量小于破坏生成物全部化学键所需能量的反应是放热反应 |
| C.加入催化剂,可以改变化学反应的反应热 |
| D.根据能量守恒定律,反应物的总能量等于生成物的总能量 |
您最近半年使用:0次
【推荐2】碘与氢气反应的热化学方程式是:①
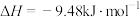 ,②
,②
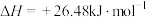 ,下列说法正确的是
,下列说法正确的是

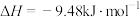 ,②
,②
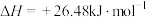 ,下列说法正确的是
,下列说法正确的是A.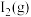 和 和 完全反应生成 完全反应生成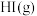 时放热 时放热 |
B. 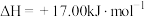 |
| C.②的反应物总能量比①的反应物总能量低 |
D.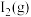 比 比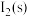 稳定 稳定 |
您最近半年使用:0次
【推荐3】下列过程都与热量变化有关,其中叙述正确的是( )


| A.Ba(OH)2·8H2O与NH4Cl常温下混合就能反应,故该反应放热 |
| B.已知2H2(g)+O2(g)=2H2O(g) ΔH=﹣483.6kJ·mol–1,故H2的燃烧热为241.8kJ·mol–1 |
| C.已知H+(aq)+OH-(aq)=H2O(l) ΔH=﹣57.3kJ·mol–1,故Ba2+(aq)+H+(aq)+OH-(aq)+SO42-(aq)=H2O(1)+BaSO4(s) ΔH=﹣57.3kJ·mol–1 |
| D.由图可知,反应C(金刚石,s)=C(石墨,s)的焓变ΔH=ΔH2-ΔH1 |
您最近半年使用:0次
单选题
|
适中
(0.65)
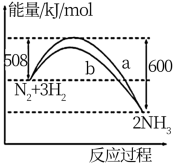
【推荐1】氨是一种重要的化工原料,主要用于化肥、纯碱、硝酸等工业。用N2和H2在一定条件下可合成NH3; NH3催化氧化可转化为NO,再氧化为NO2;一定条件下,NO2与N2O4之间存在平衡:2NO2(g)  N2O4(g) ΔH<0。某温度时,N2与H2反应过程中的能量变化曲线如图。下列叙述中不正确的是
N2O4(g) ΔH<0。某温度时,N2与H2反应过程中的能量变化曲线如图。下列叙述中不正确的是
 N2O4(g) ΔH<0。某温度时,N2与H2反应过程中的能量变化曲线如图。下列叙述中不正确的是
N2O4(g) ΔH<0。某温度时,N2与H2反应过程中的能量变化曲线如图。下列叙述中不正确的是
| A.该反应的ΔS<0 |
| B.b曲线是加入催化剂时的能量变化曲线 |
| C.由图象计算,若用E表示键能,该反应ΔH= E(N≡N)+ 3E(H-H)- 6E(N -H) |
| D.一定条件下,将2 mol N2(g)和6 mol H2(g)通入某密闭容器中,反应后放出的热量为184 kJ |
您最近半年使用:0次
【推荐2】已知:C(s)+ H2O(g) = CO(g) +H2(g) ΔH= -131.3 kJ/mol下列说法正确的是( )
| A.加入催化剂,可以减小该反应的反应热 |
| B.通入水蒸气可增大该反应的反应热 |
| C.该反应中反应物的总能量低于生成物的总能量 |
| D.反应 CO(g) +H2(g) = C(s)+ H2O(g) 的ΔH=+131.3 kJ/mol |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】关于热化学方程式,下列说法正确的是
A.2molSO2和1molO2充分反应后放出热量196.6kJ,则2SO2(g) + O2(g) 2SO3(g) △H=-196.6 kJ/mol 2SO3(g) △H=-196.6 kJ/mol |
| B.在稀溶液中:H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3kJ·mol-1,若将含1molCH3COOH的醋酸溶液与含1molNaOH的溶液混合,放出的热量小于57.3kJ |
| C.等量的硫蒸气和硫固体分别完全燃烧,后者放出热量多 |
| D.甲烷的燃烧热为-890.3KJ/mol,则甲烷燃烧的热化学方程式表示为CH4(g) + 2O2(g) = CO2(g) + 2H2O(g) △H=-890.3kJ/mol |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列有关热化学方程式,说法正确的是
| A.甲烷的燃烧热为890.3 kJ·mol-1,则甲烷燃烧热的热化学方程式可表示为CH4(g)+2O2(g)=CO2(g)+2H2O(g) ΔH=-890.3 kJ·mol-1 |
| B.已知:S(s)+O2(g)=SO2(g) ΔH1,S(g)+O2(g)=SO2(g) ΔH2,则ΔH1>ΔH2 |
| C.已知热化学方程式:N2(g)+3H2(g)⇌2NH3(g) ΔH=-92.4 kJ·mol-1,则在此条件下向某容器充入0.5molN2和1.5molH2充分反应后,可放出46.2kJ的热量 |
| D.已知强酸和强碱稀溶液的中和热可表示为:H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3 kJ·mol-1,则:H2SO4(aq)+Ba(OH)2(aq)=BaSO4(s)+2H2O(l) ΔH=-114.6 kJ·mol-1 |
您最近半年使用:0次



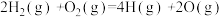 的过程会放出能量
的过程会放出能量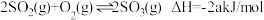
 ,则HCl和Ba(OH)2反应的中和热
,则HCl和Ba(OH)2反应的中和热

