按要求填空。
(1)33.3g某金属氯化物 中含有
中含有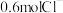 ,则M的相对原子质量为
,则M的相对原子质量为_______ 。
(2)标准状况下,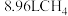 和
和 的混合气体,其质量为7.6g,则混合气体中
的混合气体,其质量为7.6g,则混合气体中 的体积为
的体积为_______ L, 的质量为
的质量为_______ g。
(3) 个
个 约含
约含_______ 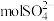 ,其质量为
,其质量为_______ g。
(4)中子数为18的硫原子,其微粒符号可表示为_______ 。
(5)质量数为37、中子数为20的原子,其结构示意图可表示为_______ 。
(6)已知Mm+的电子数为a,M的质量数为A,则 的M的中子数为
的M的中子数为_______ 。
(1)33.3g某金属氯化物
 中含有
中含有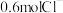 ,则M的相对原子质量为
,则M的相对原子质量为(2)标准状况下,
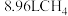 和
和 的混合气体,其质量为7.6g,则混合气体中
的混合气体,其质量为7.6g,则混合气体中 的体积为
的体积为 的质量为
的质量为(3)
 个
个 约含
约含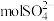 ,其质量为
,其质量为(4)中子数为18的硫原子,其微粒符号可表示为
(5)质量数为37、中子数为20的原子,其结构示意图可表示为
(6)已知Mm+的电子数为a,M的质量数为A,则
 的M的中子数为
的M的中子数为
更新时间:2023-08-08 15:15:57
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】A元素原子M电子层上有6个电子。B元素与A元素的原子核外电子层数相同,B元素的原子最外电子层只有1个电子。
(1)B元素的原子结构示意图为___________ 。
(2)A、B两元素形成的化合物的名称是________________ 。
(3)用电子式表示B2A的形成过程______________________
(1)B元素的原子结构示意图为
(2)A、B两元素形成的化合物的名称是
(3)用电子式表示B2A的形成过程
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】按要求填空
(1)S2﹣中含有 18 个电子,画出 S 的原子结构示意图_____ .
(2)一水合氨(NH3•H2O)是一种弱电解质,在水中可电离出铵根离子和氢氧 根离子,试写出一水合氨的电离方程式_____ .
(3)正长石的组成可表示为 KAlSi3Ox,试根据化合价计算 x=______ .
(1)S2﹣中含有 18 个电子,画出 S 的原子结构示意图
(2)一水合氨(NH3•H2O)是一种弱电解质,在水中可电离出铵根离子和氢氧 根离子,试写出一水合氨的电离方程式
(3)正长石的组成可表示为 KAlSi3Ox,试根据化合价计算 x=
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】元素①~⑧在元素周期表中的位置如图,回答有关问题:
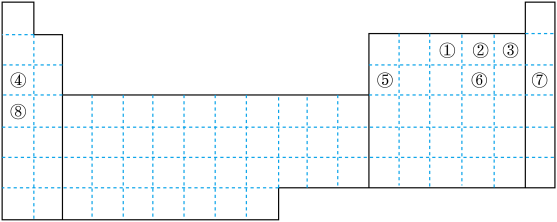
(1)画出⑦的原子结构示意图___________ 。
(2)写出②含有10个中子的核素的化学符号___________ 。
(3)表中②、③、⑥对应的简单离子半径由小到大的顺序为___________ (填离子符号)。
(4)请写出①的氢化物发生催化氧化的化学方程式___________ 。
(5)请写出元素①~⑧中能形成两性氢氧化物的元素对应的单质与⑧的最高价氧化物的水化物反应的离子方程式___________ 。

(1)画出⑦的原子结构示意图
(2)写出②含有10个中子的核素的化学符号
(3)表中②、③、⑥对应的简单离子半径由小到大的顺序为
(4)请写出①的氢化物发生催化氧化的化学方程式
(5)请写出元素①~⑧中能形成两性氢氧化物的元素对应的单质与⑧的最高价氧化物的水化物反应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】在浓硝酸中放入铜片:
(1)开始反应的化学方程式为_______ ,实验现象为_______ 。
(2)若铜有剩余,则反应将要结束时的离子方程式为___________ 。
(3)若将12.8 g铜跟一定量的浓硝酸反应,铜耗完时,共产生气体5.6 L(标准状况下)。则所消耗硝酸的物质的量是________________________ 。
(1)开始反应的化学方程式为
(2)若铜有剩余,则反应将要结束时的离子方程式为
(3)若将12.8 g铜跟一定量的浓硝酸反应,铜耗完时,共产生气体5.6 L(标准状况下)。则所消耗硝酸的物质的量是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】按要求填写下列空格
①9gH2O含H原子的物质的量为_____________ mol;
②标准状况下,体积为11.2 L 的CO2所含原子的总数是_______________
③等质量的O2和O3所含原子个数比为________
④8.4g NaHCO3 正好与20mL盐酸完全反应。此盐酸的物质的量浓度是__________ ,产生的CO2在标准状况下的体积是_____________ L
⑤ 用单线桥法表示反应:2KMnO4+16HCl(浓) = 2KCl+2MnCl2+5Cl2↑+8H2O转移电子的方向和数目____________________________________________________ 。
⑥写出离子反应方程式CO2 + 2OH-= CO32-+ H2O所对应的一个化学方程式:__________ 。
①9gH2O含H原子的物质的量为
②标准状况下,体积为11.2 L 的CO2所含原子的总数是
③等质量的O2和O3所含原子个数比为
④8.4g NaHCO3 正好与20mL盐酸完全反应。此盐酸的物质的量浓度是
⑤ 用单线桥法表示反应:2KMnO4+16HCl(浓) = 2KCl+2MnCl2+5Cl2↑+8H2O转移电子的方向和数目
⑥写出离子反应方程式CO2 + 2OH-= CO32-+ H2O所对应的一个化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】必修Ⅰ第二章带领我们认识了海水中重要元素-钠和氯,同时引入了一个新的物理量——物质的量,帮助我们建立宏观物质和微观微粒之间的联系。以下是小明和李华两位同学学习第二章后相互赠送的化学礼物——亲自命制的习题。作为他们共同的好朋友,请你也收下并完成这两份礼物,陪伴他们共同成长与进步。
Ⅰ.小明送出的礼物(节选):
(1)钠长期置于空气中,最后形成的物质是_______ ,该物质与足量盐酸反应的离子方程式为_______ ,为除去该反应生成的气体中混有的HCl,应选用试剂_______ 。
(2)加热法除去碳酸钠固体中少量的碳酸氢钠反应化学方程式为_______ 。
Ⅱ.李华送出的礼物(节选):
(3)除去氯气中的HCl选用试剂_______ 。
(4)漂白粉的制备化学方程式_______ 。
(5)56g Fe与足量的氯气完全反应转移_______ 个电子数。
(6)相同质量的CO和CO2所含的氧原子个数之比是_______ 。
Ⅰ.小明送出的礼物(节选):
(1)钠长期置于空气中,最后形成的物质是
(2)加热法除去碳酸钠固体中少量的碳酸氢钠反应化学方程式为
Ⅱ.李华送出的礼物(节选):
(3)除去氯气中的HCl选用试剂
(4)漂白粉的制备化学方程式
(5)56g Fe与足量的氯气完全反应转移
(6)相同质量的CO和CO2所含的氧原子个数之比是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】回答下列问题
(1)①HClO的结构式为___________ ;
②水分子的空间构型___________ ;
③铁红的化学式___________ ;
(2)相同条件下,冰的密度比水小的原因是___________ ;
(3)氧元素的一种核素,核内有10个中子,该核素的符号可表示为___________ ;
(4)用氯气制备“84”消毒液的离子方程式为___________ ,消毒液消毒衣服时要先用温水稀释后再浸泡一段时间,但温度不能高于50℃。则温度不宜过高的原因是___________ ;
(5)写出铝粉与氢氧化钠溶液的反应的化学方程式,并用单线桥表示电子转移的方向和数目___________ 。
(6) 遇水产生氢气,该反应的化学方程式
遇水产生氢气,该反应的化学方程式___________ 。
(1)①HClO的结构式为
②水分子的空间构型
③铁红的化学式
(2)相同条件下,冰的密度比水小的原因是
(3)氧元素的一种核素,核内有10个中子,该核素的符号可表示为
(4)用氯气制备“84”消毒液的离子方程式为
(5)写出铝粉与氢氧化钠溶液的反应的化学方程式,并用单线桥表示电子转移的方向和数目
(6)
 遇水产生氢气,该反应的化学方程式
遇水产生氢气,该反应的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】日本决定于2023年8月23日将福岛核电站的核污水排入大海,引起了国际上的关注和担忧。其中含有大量的放射性元素如角( ),碘(
),碘( ),碳(
),碳( )等对人体能够造成一定的危害。
)等对人体能够造成一定的危害。
(1)碘( )的质量数是
)的质量数是___________ ,中子数是___________ 。在生活中,我们也会摄入含碘( )的食品来补充人体所需的甲状腺激素,(
)的食品来补充人体所需的甲状腺激素,( )与(
)与( )互为
)互为___________ 。
(2)从元素周期表查得氢元素的某一数值为1.008,该数值表示___________。
(3)碳( )由于其半衰期长达5730年,在考古发现中起到了一定的作用,请画出其电子式
)由于其半衰期长达5730年,在考古发现中起到了一定的作用,请画出其电子式___________ 。
(4)前20号元素中,有A,B,C,D四种元素,它们的质子数依次增大,C的原子序数是另外三种元素的K层电子数之和的两倍。A的负离子和B的正离子电子层数相同,A和D的原子的最外层电子数相同,D需要得一个电子才能达到稳定结构。请依次写出A.C原子,D离子的结构示意图___________ ,___________ ,___________ 。
 ),碘(
),碘( ),碳(
),碳( )等对人体能够造成一定的危害。
)等对人体能够造成一定的危害。(1)碘(
 )的质量数是
)的质量数是 )的食品来补充人体所需的甲状腺激素,(
)的食品来补充人体所需的甲状腺激素,( )与(
)与( )互为
)互为(2)从元素周期表查得氢元素的某一数值为1.008,该数值表示___________。
| A.一种氢原子的质量数 | B.氢元素的近似相对原子质量 |
| C.三种氢原子的平均相对原子质量 | D.氢元素的相对原子质量 |
 )由于其半衰期长达5730年,在考古发现中起到了一定的作用,请画出其电子式
)由于其半衰期长达5730年,在考古发现中起到了一定的作用,请画出其电子式(4)前20号元素中,有A,B,C,D四种元素,它们的质子数依次增大,C的原子序数是另外三种元素的K层电子数之和的两倍。A的负离子和B的正离子电子层数相同,A和D的原子的最外层电子数相同,D需要得一个电子才能达到稳定结构。请依次写出A.C原子,D离子的结构示意图
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】核外电子排布规律
(1)能量最低原理
电子总是尽可能先从内层排起,当一层充满后再填充下一层,即按___________ 顺序排列。
(2)电子层最多容纳的电子数
①第n层最多容纳___________ 个电子,K、L、M、N层最多容纳的电子数依次为2、8、18、32。
②K层为最外层时最多容纳的电子数为2,除K层外,其他各层为最外层时,最多容纳的电子数为___________ 。
③K层为次外层时,所排电子数为2,除K层外,其他各层为次外层时,最多容纳的电子数为___________ 。
(1)能量最低原理
电子总是尽可能先从内层排起,当一层充满后再填充下一层,即按
(2)电子层最多容纳的电子数
①第n层最多容纳
②K层为最外层时最多容纳的电子数为2,除K层外,其他各层为最外层时,最多容纳的电子数为
③K层为次外层时,所排电子数为2,除K层外,其他各层为次外层时,最多容纳的电子数为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】(1)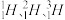 是三种不同的
是三种不同的_____ ,它们互为_____ ,它们都属于氢_____ (填元素,核素,同位素)
(2)α射线是由α粒子组成的,α粒子是一种没有核外电子的粒子,它带有两个 单位的正电荷,质量数等于 4,由此可推断α粒子有______ 个质子,_______ 个 中子。
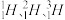 是三种不同的
是三种不同的(2)α射线是由α粒子组成的,α粒子是一种没有核外电子的粒子,它带有两个 单位的正电荷,质量数等于 4,由此可推断α粒子有
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】据报道,某些花岗岩会产生氡(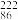 Rn),从而对人体产生伤害。请回答:
Rn),从而对人体产生伤害。请回答:
(1)该原子的质量数是________ ,质子数是________ ,中子数是________ 。
(2)研究发现,镭能蜕变为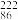 Rn,故将
Rn,故将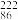 Rn称为镭射气;钍能蜕变为
Rn称为镭射气;钍能蜕变为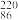 Rn,故将
Rn,故将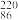 Rn称为钍射气;锕能蜕变为
Rn称为钍射气;锕能蜕变为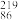 Rn,故将
Rn,故将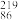 Rn称为锕射气。
Rn称为锕射气。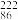 Rn、
Rn、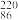 Rn、
Rn、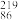 Rn
Rn________ 。
A.属于同种元素B.互为同位素
C.属于同种核素D.属于同种原子
(3)由(2)可知,________ 决定元素种类,________ 决定核素种类。
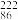 Rn),从而对人体产生伤害。请回答:
Rn),从而对人体产生伤害。请回答:(1)该原子的质量数是
(2)研究发现,镭能蜕变为
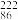 Rn,故将
Rn,故将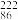 Rn称为镭射气;钍能蜕变为
Rn称为镭射气;钍能蜕变为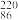 Rn,故将
Rn,故将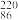 Rn称为钍射气;锕能蜕变为
Rn称为钍射气;锕能蜕变为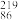 Rn,故将
Rn,故将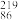 Rn称为锕射气。
Rn称为锕射气。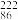 Rn、
Rn、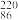 Rn、
Rn、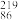 Rn
RnA.属于同种元素B.互为同位素
C.属于同种核素D.属于同种原子
(3)由(2)可知,
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】请完成下列问题:
(1)画出氯原子结构示意图___ 。
(2)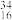 S2-微粒中的质子数是
S2-微粒中的质子数是___ ,中子数是___ 。
(3)49g硫酸的物质的量为___ mol,其完全电离产生H+的个数为___ 。
(4)写出实验室制氯气的离子方程式:___ 。
(1)画出氯原子结构示意图
(2)
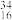 S2-微粒中的质子数是
S2-微粒中的质子数是(3)49g硫酸的物质的量为
(4)写出实验室制氯气的离子方程式:
您最近一年使用:0次



