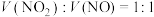已知Cu+遇酸会发生歧化反应。检验K2[Cu(C2O4)2]分解产物的实验如图所示,下列说法正确的是


| A.上述实验现象说明气体A中一定含有CO2 |
| B.上述实验现象说明固体A中一定含有Cu、Cu2+ |
| C.向固体A中加入浓硝酸,生成的气体仍一定能使澄清石灰水变浑浊 |
D. 在反应过程中一定发生了歧化反应 在反应过程中一定发生了歧化反应 |
更新时间:2023-08-10 15:51:11
|
相似题推荐
单选题
|
较难
(0.4)
解题方法
【推荐1】有一包白色粉末,由Na2SiO3、BaSO4、BaCO3、Na2SO3、NaOH中的一种或几种组成,为了探究它的成分,进行了如下实验:

下列判断错误的是( )

下列判断错误的是( )
| A.生成白色沉淀D的离子方程式为SiO32-+2H+=H2SiO3↓ |
| B.BaSO4一定不存在,NaOH可能存在 |
| C.Na2SiO3、BaSO4、BaCO3、Na2SO3一定存在,NaOH可能存在 |
| D.气体B和气体E均可使澄清的石灰水变浑浊 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】某溶液中存在以下离子中的几种:Ag+、NH 、Fe2+、Na+、K+、AlO
、Fe2+、Na+、K+、AlO 、I-、SO
、I-、SO 、SO
、SO 、NO
、NO ,且存在的离子具有相同的物质的量浓度。向该溶液中加入过量的盐酸酸化的BaCl2溶液,产生了白色沉淀和气体。则下列说法正确的是
,且存在的离子具有相同的物质的量浓度。向该溶液中加入过量的盐酸酸化的BaCl2溶液,产生了白色沉淀和气体。则下列说法正确的是
 、Fe2+、Na+、K+、AlO
、Fe2+、Na+、K+、AlO 、I-、SO
、I-、SO 、SO
、SO 、NO
、NO ,且存在的离子具有相同的物质的量浓度。向该溶液中加入过量的盐酸酸化的BaCl2溶液,产生了白色沉淀和气体。则下列说法正确的是
,且存在的离子具有相同的物质的量浓度。向该溶液中加入过量的盐酸酸化的BaCl2溶液,产生了白色沉淀和气体。则下列说法正确的是A.溶液中可能同时存在Ag+、NO | B.溶液中可能同时存在SO 、I- 、I- |
| C.溶液中可能同时存在Fe2+、I- | D.沉淀和气体可能同时是BaSO4和SO2 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐1】由于6s2惰性电子对效应,金Au、汞Hg、铊Tl、铅Pb、铋Bi的最稳定氧化态分别为-1,0,+1,+2,+3。下列说法错误 的是
| A.根据这个规律,人们制出负一价的金的化合物CsAu |
B.与汞同族锌镉为较活泼金属而汞为不活泼金属,且对于+1氧化态,Hg倾向于形成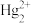 |
C.二氧化铅氧化性很强,可和浓盐酸反应制取氯气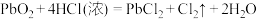 |
D.铋酸钠与酸性硫酸锰的离子方程式: |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】根据表中信息判断,下列选项不正确的是( )
序号 | 反应物 | 产物 |
① | KMnO4、H2O2、H2SO4 | K2SO4、MnSO4 |
② | Cl2、FeBr2 | FeCl3、FeBr3 |
③ | MnO4﹣ | Cl2、Mn2+ |
| A.第①组反应的其余产物为H2O和O2 |
| B.第②组反应中当足量Cl2与1mol FeBr2反应时转移的电子数为2NA个 |
| C.氧化性由强到弱顺序为MnO4->Cl2>Fe3+ |
| D.第③组反应中生成1mol Cl2,转移电子2mol |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐1】下列反应必须加入氧化剂且一步反应就能完成的是
①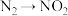 ②
② ③
③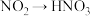 ④
④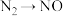 ⑤
⑤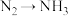
①
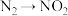 ②
② ③
③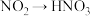 ④
④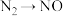 ⑤
⑤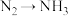
| A.①②③④ | B.②③④ | C.④ | D.③④ |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】将甲和乙的混合气体通入过量的丙溶液中,一定能产生沉淀的组合是
| 序号 | 甲 | 乙 | 丙 | 装置图 |
| ① | CO2 | SO2 | 石灰水 | |
| ② | CO2 | NH3 | CaCl2 | |
| ③ | HCl | CO2 | 石灰水 | |
| ④ | CO2 | SO2 | Ba(NO3)2 | |
| ⑤ | NO2 | SO2 | BaCl2 | |
| ⑥ | NH3 | CO2 | NaCl |
| A.②③④ | B.①④⑤ | C.①③④⑤⑥ | D.①②③④ |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐1】关于C、N、Si、S等非金属元素及其化合物的下列说法错误的是
| A.它们都能以游离态存在于自然界中 |
| B.氮氧化物、二氧化硫是形成酸雨的主要物质 |
| C.它们的最高价氧化物都能与强碱反应生成含氧酸盐 |
| D.加热条件下,碳、硫单质都能与浓硝酸、浓硫酸发生反应 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】某无色溶液W由下列离子中的若干种组成:H+、 、Fe3+、Ba2+、Mg2+、
、Fe3+、Ba2+、Mg2+、 、I-、OH-、
、I-、OH-、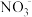 。向W中加入铝粉后有气体Y、含铝元素的离子X等生成。若不考虑水的电离,则下列说法中正确的是
。向W中加入铝粉后有气体Y、含铝元素的离子X等生成。若不考虑水的电离,则下列说法中正确的是
 、Fe3+、Ba2+、Mg2+、
、Fe3+、Ba2+、Mg2+、 、I-、OH-、
、I-、OH-、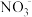 。向W中加入铝粉后有气体Y、含铝元素的离子X等生成。若不考虑水的电离,则下列说法中正确的是
。向W中加入铝粉后有气体Y、含铝元素的离子X等生成。若不考虑水的电离,则下列说法中正确的是| A.X一定是Al3+ | B.Y一定是H2 |
| C.W中最多含有6种离子 | D.溶液中不可能含 |
您最近一年使用:0次

 。某固体粉末X中可能含有等物质的量的Fe2O3、Fe3O4、NaHCO3、Na2CO3、Na2S2O3、NaAlO2中的若干种。为确定该固体粉末的成分,现取X进行连续实验,实验过程及现象如下:
。某固体粉末X中可能含有等物质的量的Fe2O3、Fe3O4、NaHCO3、Na2CO3、Na2S2O3、NaAlO2中的若干种。为确定该固体粉末的成分,现取X进行连续实验,实验过程及现象如下: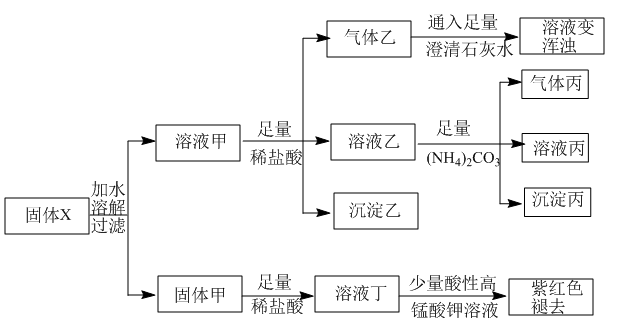
 ,可能含有
,可能含有
 ,其中Cu、Fe均为+2价),其反应为:
,其中Cu、Fe均为+2价),其反应为: 。关于此反应,下列说法正确的是
。关于此反应,下列说法正确的是 仅是氧化产物
仅是氧化产物 ,有1mol硫被氧化
,有1mol硫被氧化 完全溶于0.5L6mol/L的
完全溶于0.5L6mol/L的 溶液中,得到标况下
溶液中,得到标况下 与NO的混合气体,产生的混合气体通入标况下
与NO的混合气体,产生的混合气体通入标况下 恰好能溶于水,向反应后的溶液中加入
恰好能溶于水,向反应后的溶液中加入 的NaOH溶液恰好使溶液中的
的NaOH溶液恰好使溶液中的 沉淀,下列说法错误的是
沉淀,下列说法错误的是