将agNH3溶于水得到VmL溶液,假设该溶液的密度为ρg/cm3,质量分数为w,溶液中NH 为bmol。已知氨水的密度比水小且浓度越大密度越小。下列叙述正确的是
为bmol。已知氨水的密度比水小且浓度越大密度越小。下列叙述正确的是
 为bmol。已知氨水的密度比水小且浓度越大密度越小。下列叙述正确的是
为bmol。已知氨水的密度比水小且浓度越大密度越小。下列叙述正确的是A.据电荷守恒知:溶液中c(OH-)=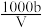 +c(H+) +c(H+) |
B.溶质的质量分数为w= ×100% ×100% |
C.溶质的物质的量浓度c=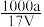 mol/L mol/L |
| D.上述溶液中再加入VmL水后,所得溶液的质量分数大于0.5w |
更新时间:2023-08-31 20:51:39
|
【知识点】 物质的量浓度计算-与溶质成分有关的计算解读
相似题推荐
多选题
|
较难
(0.4)
解题方法
【推荐1】下列说法不正确的是
A.20℃时,饱和KCl溶液的密度为1.174g·cm-3,质量分数为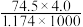 ×100%,此溶液中KCl的物质的量浓度为4.0mol·L-1 ×100%,此溶液中KCl的物质的量浓度为4.0mol·L-1 |
| B.100g浓度为cmol·L-1的氨水中加入一定量的水稀释成0.5cmol·L-1,则加入水的体积小于100mL(已知氨水的浓度越大,其密度越小) |
C.将标准状况下的aLHCl气体溶于1000mL水中,得到盐酸的密度为bg·mL-1,则该盐酸的物质的量浓度为 mol·L-1 mol·L-1 |
D.VLFe2(SO4)3溶液中含Fe3+mg,则溶液中 的物质的量浓度为 的物质的量浓度为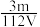 mol·L-1 mol·L-1 |
您最近一年使用:0次
多选题
|
较难
(0.4)
【推荐2】某结晶水合物的化学式为R·nH2O,其摩尔质量为Mg·mol-1。25℃时,将ag该晶体溶于bg水中恰好可形成VmL饱和溶液。下列关系正确的是
A.饱和溶液的物质的量浓度c=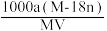 mol·L-1 mol·L-1 |
B.饱和溶液中溶质的质量分数w= ×100% ×100% |
C.25℃时R的溶解度S=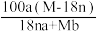 g g |
D.饱和溶液的密度ρ=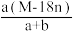 g·L-1 g·L-1 |
您最近一年使用:0次



