某结晶水合物的化学式为R·nH2O,其摩尔质量为Mg·mol-1。25℃时,将ag该晶体溶于bg水中恰好可形成VmL饱和溶液。下列关系正确的是
A.饱和溶液的物质的量浓度c=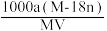 mol·L-1 mol·L-1 |
B.饱和溶液中溶质的质量分数w= ×100% ×100% |
C.25℃时R的溶解度S=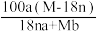 g g |
D.饱和溶液的密度ρ=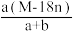 g·L-1 g·L-1 |
2023高三·全国·专题练习 查看更多[1]
(已下线)第2讲 物质的浓度及溶液配制
更新时间:2023-06-28 16:21:49
|
相似题推荐
多选题
|
较难
(0.4)
解题方法
【推荐1】现有硫酸钠溶液V mL,它的密度是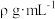 ,其中钠离子的质量分数是a%,则下列有关该溶液的说法错误的是。
,其中钠离子的质量分数是a%,则下列有关该溶液的说法错误的是。
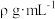 ,其中钠离子的质量分数是a%,则下列有关该溶液的说法错误的是。
,其中钠离子的质量分数是a%,则下列有关该溶液的说法错误的是。A.溶质的质量分数是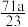 % % |
B.溶液的物质的量浓度是 |
C.溶质和溶剂的物质的量之比是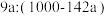 |
D.硫酸根离子的质量分数是 |
您最近一年使用:0次
多选题
|
较难
(0.4)
解题方法
【推荐2】vmL密度为 g/cm3的某溶液中,含有相对分子质量为M的溶质m g,该溶液中溶质的质量分数为W%,物质的量浓度为cmol/L,那么下列关系式正确的是
g/cm3的某溶液中,含有相对分子质量为M的溶质m g,该溶液中溶质的质量分数为W%,物质的量浓度为cmol/L,那么下列关系式正确的是
 g/cm3的某溶液中,含有相对分子质量为M的溶质m g,该溶液中溶质的质量分数为W%,物质的量浓度为cmol/L,那么下列关系式正确的是
g/cm3的某溶液中,含有相对分子质量为M的溶质m g,该溶液中溶质的质量分数为W%,物质的量浓度为cmol/L,那么下列关系式正确的是A.c= | B.c=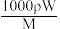 | C.W%=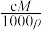 | D.m=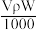 |
您最近一年使用:0次
多选题
|
较难
(0.4)
【推荐1】Mg、Al、Fe 三种金属的混合物与足量的稀硫酸反应,生成 2.8L H2(标准状况)则三种金属的物 质的量之和不可能是( )
| A.0.12 mol | B.0.15 mol | C.0.08 mol | D.0.1 mol |
您最近一年使用:0次
多选题
|
较难
(0.4)
解题方法
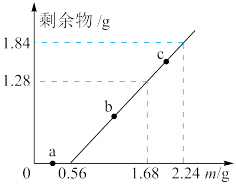
【推荐2】实验研究发现,金属与硝酸发生氧化还原反应时,硝酸的浓度越稀,对应还原产物中氮元素的化合价越低。现有一定量的铝粉和铁粉的混合物与足量很稀的硝酸充分反应,反应过程中无气体放出,在反应结束后的溶液中逐滴加入5mol/LNaOH溶液,所加NaOH溶液的体积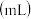 与产生沉淀的物质的量
与产生沉淀的物质的量 关系如图所示,下列说法正确的是
关系如图所示,下列说法正确的是
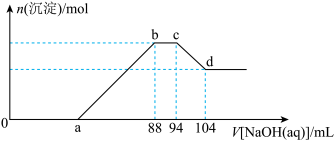
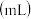 与产生沉淀的物质的量
与产生沉淀的物质的量 关系如图所示,下列说法正确的是
关系如图所示,下列说法正确的是
A. 点到 点到 点的反应为: 点的反应为: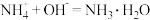 |
B.样品中铝粉和铁粉的质量之比为 : : |
C. 点对应 点对应 溶液的体积为 溶液的体积为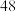  |
D.原硝酸溶液中硝酸的物质的量为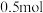 |
您最近一年使用:0次
多选题
|
较难
(0.4)
名校
解题方法
【推荐1】将8.0g镁铁合金加入500mL稀盐酸中恰好完全反应,得到标准状况下氢气4.48L。下列有关说法不正确的是
| A.该合金中镁、铁的物质的量之比为1:1 |
| B.反应中转移电子0.6mol |
| C.该盐酸的物质的量浓度为0.8mol/L |
| D.将标准状况下8.96LHCl气体溶于500mL水中即可配制成该盐酸 |
您最近一年使用:0次
多选题
|
较难
(0.4)
名校
解题方法
【推荐2】将agNH3溶于水得到VmL溶液,假设该溶液的密度为ρg/cm3,质量分数为w,溶液中NH 为bmol。已知氨水的密度比水小且浓度越大密度越小。下列叙述正确的是
为bmol。已知氨水的密度比水小且浓度越大密度越小。下列叙述正确的是
 为bmol。已知氨水的密度比水小且浓度越大密度越小。下列叙述正确的是
为bmol。已知氨水的密度比水小且浓度越大密度越小。下列叙述正确的是A.据电荷守恒知:溶液中c(OH-)=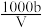 +c(H+) +c(H+) |
B.溶质的质量分数为w= ×100% ×100% |
C.溶质的物质的量浓度c=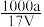 mol/L mol/L |
| D.上述溶液中再加入VmL水后,所得溶液的质量分数大于0.5w |
您最近一年使用:0次
【推荐3】1.52g铜镁合金完全溶解于50mL密度为1.40 g/mL、质量分数为63%的浓硝酸中,得到NO2和N2O4的混合气体1120 mL(标准状况),向反应后的溶液中加入1.0 mol/L NaOH溶液,当金属离子全部沉淀时,得到2.54 g沉淀。下列说法正确的是
| A.该浓硝酸中HNO3的物质的量浓度为14mol/L |
| B.该合金中铜与镁的物质的量之比为1:2 |
| C.NO2和N2O4的混合气体中,NO2的体积分数是80% |
| D.得到2.54 g沉淀时,加入NaOH溶液的体积是600mL |
您最近一年使用:0次

 盐R进行相关实验,数据和现象如下:
盐R进行相关实验,数据和现象如下:
 。
。