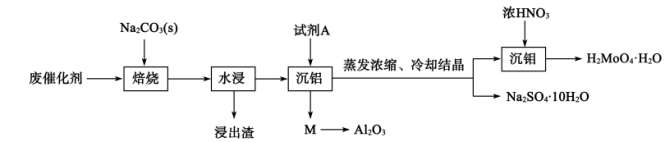
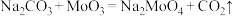实验研究发现,金属与硝酸发生氧化还原反应时,硝酸的浓度越稀,对应还原产物中氮元素的化合价越低。现有一定量的铝粉和铁粉的混合物与足量很稀的硝酸充分反应,反应过程中无气体放出,在反应结束后的溶液中逐滴加入5mol/LNaOH溶液,所加NaOH溶液的体积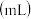 与产生沉淀的物质的量
与产生沉淀的物质的量 关系如图所示,下列说法正确的是
关系如图所示,下列说法正确的是
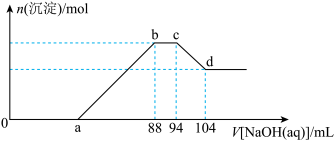
 与产生沉淀的物质的量
与产生沉淀的物质的量 关系如图所示,下列说法正确的是
关系如图所示,下列说法正确的是
A. 点到 点到 点的反应为: 点的反应为: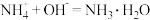 |
B.样品中铝粉和铁粉的质量之比为 : : |
C. 点对应 点对应 溶液的体积为 溶液的体积为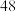  |
D.原硝酸溶液中硝酸的物质的量为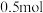 |
更新时间:2022-12-02 11:55:54
|
相似题推荐
多选题
|
较难
(0.4)
名校
【推荐1】在20 ℃时,在一刚性容器内部有一个不漏气且可滑动的活塞将容器分隔成左右两室。左室充入氮气,右室充入氢气与氧气的混合气体,活塞恰好停留在离左端的1/4处(如下图左所示),然后引燃氢、氧混合气体,反应完毕后恢复至原来温度,活塞恰好停在中间(如下图右所示),如果忽略水蒸气体积,则反应前氢气与氧气的体积比可能是
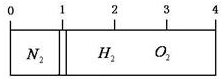
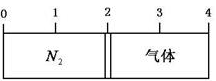


| A.3∶4 | B.4∶5 | C.6:2 | D.7∶2 |
您最近一年使用:0次
多选题
|
较难
(0.4)
解题方法
【推荐2】将15.6gNa2O2和5.4gAl同时放入一定量的水中,充分反应后得到200mL溶液,再向该溶液中缓慢通入HCl气体6.72L(标准状况),若忽略反应过程中溶液的体积变化,则下列判断正确的是
| A.反应过程中得到6.72L(标准状况)的气体 |
| B.最终得到的溶液中c(Na+)= c(Cl-)+ c(OH-) |
| C.最终得到7.8g沉淀 |
| D.最终得到的溶液中c(NaCl)=1.5mol/L |
您最近一年使用:0次
多选题
|
较难
(0.4)
【推荐1】已知:2Fe2++Br2=2Fe3++2Br-,2Br-+Cl2=Br2+2Cl- , 2Fe3++2I-=2Fe2++I2。向FeI2、FeBr2的混合溶液中通入适量氯气,溶液中某些离子的物质的量变化如图所示。下列有关说法中,正确的是
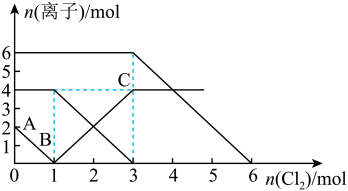

| A.还原性:I-<Fe2+<Br- |
| B.当通入2molCl2时,溶液中已发生的离子反应可表示为:2Fe2++2I-+2Cl2=2Fe3++I2+4Cl- |
| C.原溶液中n(Fe2+)∶n(I-)∶n(Br-)=2∶1∶3 |
| D.原混合溶液中FeBr2的物质的量为6mol |
您最近一年使用:0次
多选题
|
较难
(0.4)
名校
解题方法
【推荐2】向盛有 KMnO4 溶液的试管中加入过量的 MnSO4溶液,产生黑色沉淀,溶液由紫红色变为无色;过滤,向滤液中加入少量的铋酸钠(NaBiO3)粉末,溶液又变为紫红色。下列推断错误的是
| A.氧化性:NaBiO3>KMnO4>MnO2 |
| B.生成 8.7g 黑色沉淀,转移 0.2mol 电子 |
| C.利用 NaBiO3 可以检验溶液中的 Mn2+ |
| D.NaBiO3 不能与浓盐酸发生反应生成氯气 |
您最近一年使用:0次
多选题
|
较难
(0.4)
【推荐1】实验研究发现,硝酸发生氧化还原反应时,硝酸的浓度越稀,对应还原产物中氮元素的化合价越低。现有一定量的铁铝合金与很稀的硝酸充分反应,反应过程中无气体放出。在反应结束后的溶液x中,逐滴加入4mol•L﹣1的氢氧化钠溶液,所加氢氧化钠溶液的体积(mL)与产生的沉淀的物质的量(mol)的关系如图所示。则下列有关计算和判断正确的是( )
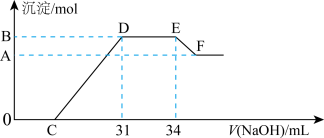

| A.溶液x中所含的阳离子有:Al3+、H+、Fe3+、Fe2+ |
| B.在DE段,发生反应的离子方程式为NH4++OH﹣→NH3•H2O |
| C.无法求出B点对应的沉淀的物质的量 |
| D.C点对应的氢氧化钠溶液的体积为7mL |
您最近一年使用:0次
多选题
|
较难
(0.4)
名校
解题方法
【推荐2】常温时,将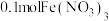 和
和 溶于水得2L混合溶液,然后向该溶液中投入mg铁粉,铁粉充分反应后(固体无剩余),该过程中收集到的气体的体积为VL(已换算成标准状况下的体积),往溶液中滴加
溶于水得2L混合溶液,然后向该溶液中投入mg铁粉,铁粉充分反应后(固体无剩余),该过程中收集到的气体的体积为VL(已换算成标准状况下的体积),往溶液中滴加 溶液,溶液不变红。下列有关说法正确的是
溶液,溶液不变红。下列有关说法正确的是
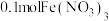 和
和 溶于水得2L混合溶液,然后向该溶液中投入mg铁粉,铁粉充分反应后(固体无剩余),该过程中收集到的气体的体积为VL(已换算成标准状况下的体积),往溶液中滴加
溶于水得2L混合溶液,然后向该溶液中投入mg铁粉,铁粉充分反应后(固体无剩余),该过程中收集到的气体的体积为VL(已换算成标准状况下的体积),往溶液中滴加 溶液,溶液不变红。下列有关说法正确的是
溶液,溶液不变红。下列有关说法正确的是A.由于氧化性 ,因此首先发生的反应是 ,因此首先发生的反应是 |
| B.V可能为11.2 |
C.在铁粉充分反应后的溶液中,铁元素以 和 和 的形式存在 的形式存在 |
D.反应过程中溶液的质量一直在增大,且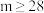 |
您最近一年使用:0次
多选题
|
较难
(0.4)
名校
解题方法
【推荐3】将12.8 g铜片加入100 mL一定浓度的硝酸溶液中,铜片完全溶解,产生NO和NO2的混合气体4.48 L(标准状况下);若向反应后的溶液中加入400 mL 2 mol/L NaOH溶液,能使溶液中的Cu2+恰好完全沉淀。下列说法不正确的是
| A.铜片与硝酸反应过程中转移电子0.4 mol |
| B.原硝酸溶液的物质的量浓度为10 mol/L |
| C.混合气体中NO和NO2的体积之比为2∶1 |
D.反应后溶液中剩余NO 的物质的量为0.4 mol 的物质的量为0.4 mol |
您最近一年使用:0次
多选题
|
较难
(0.4)
解题方法
【推荐1】将物质的量均为0.1 mol K2SO4和Al2(SO4)3溶于水,向其中加入一定量的Ba(OH)2溶液,测得铝元素有一半留在溶液中,则生成BaSO4的物质的量可能为
| A.0.15 mol | B.0.30 mol | C.0.35 mol | D.0.4 mol |
您最近一年使用:0次
多选题
|
较难
(0.4)
【推荐2】向15.0 mL 1.0 mol/L的(NH4)Al(SO4)2溶液中逐滴加入1.0 mol/L的NaOH溶液,并不断搅拌。当生成0.78 g沉淀时,所用NaOH溶液的体积可能为
| A.30 mL | B.45 mL | C.50 mL | D.65 mL |
您最近一年使用:0次