填空。
(1)常温下,CrO2Cl2为深红色液体,能与CCl4、CS2等互溶,据此可判断CrO2Cl2是___________ (填“极性”或“非极性”)分子。
(2)金属镍粉在CO气流中轻微加热,生成无色挥发性液体Ni(CO)4,呈正四面体结构。Ni(CO)4易溶于下列物质中的___________ (填字母)。
a.水 b.CCl4 c.苯 d.NiSO4溶液
(3)甲醛、甲醇和甲酸等碳原子个数较少的醛、醇和羧酸均易溶于水,而甲烷、甲酸甲酯难溶于水,试解释其原因:___________ 。
(4)下列分子中若有手性分子,请用“*”标出其手性碳原子___________ ;若无手性分子,此小题不必作答。
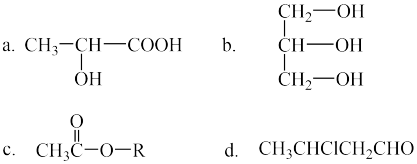
(1)常温下,CrO2Cl2为深红色液体,能与CCl4、CS2等互溶,据此可判断CrO2Cl2是
(2)金属镍粉在CO气流中轻微加热,生成无色挥发性液体Ni(CO)4,呈正四面体结构。Ni(CO)4易溶于下列物质中的
a.水 b.CCl4 c.苯 d.NiSO4溶液
(3)甲醛、甲醇和甲酸等碳原子个数较少的醛、醇和羧酸均易溶于水,而甲烷、甲酸甲酯难溶于水,试解释其原因:
(4)下列分子中若有手性分子,请用“*”标出其手性碳原子
2023高三·全国·专题练习 查看更多[1]
(已下线)第5讲 分子结构与性质
更新时间:2023-09-29 07:52:57
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】课本的第27页介绍了一种热带雌蚕蛾为了吸引同类雄蛾会分泌出叫“蚕蛾醇”的物质。
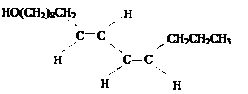
蚕蛾醇有多种顺反异构体,如请回答:
(1)蚕蛾醇共有多少种顺反异构体(含自身)__________________ 。
(2)当分子中有1个碳原子分别连有4个不同的原子或原子团时,该碳原子称为手性碳原子。则该蚕蛾醇手性碳原子数为____________ 。
(3)该蚕蛾醇的分子式为________________ 。
(4)该蚕蛾醇不具有的性质是__________ (从下面序列中选择序号填入)
①与钠反应②氧化③加聚④加成⑤NaOH中和反应
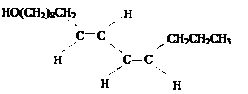
蚕蛾醇有多种顺反异构体,如请回答:
(1)蚕蛾醇共有多少种顺反异构体(含自身)
(2)当分子中有1个碳原子分别连有4个不同的原子或原子团时,该碳原子称为手性碳原子。则该蚕蛾醇手性碳原子数为
(3)该蚕蛾醇的分子式为
(4)该蚕蛾醇不具有的性质是
①与钠反应②氧化③加聚④加成⑤NaOH中和反应
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】回答下列问题
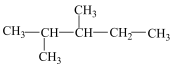
(1)某有机物A的结构简式如图,有机物A中共有____________ 个手性碳原子;若该有机物A是由烯烃和 加成得到的,则原烯烃的结构有
加成得到的,则原烯烃的结构有_____________ 种.
(2)结构为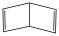 的二氯代物有
的二氯代物有_____________ 种
(3)并五苯(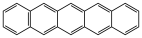 )的一氯代物有
)的一氯代物有_____________ 种,二氯蒽(蒽: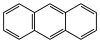 )有
)有_____________ 种.
(1)某有机物A的结构简式如图,有机物A中共有
 加成得到的,则原烯烃的结构有
加成得到的,则原烯烃的结构有
(2)结构为
 的二氯代物有
的二氯代物有(3)并五苯(
 )的一氯代物有
)的一氯代物有 )有
)有
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】药物Z可用于治疗哮喘、系统性红斑狼疮等,可由X(咖啡酸)和Y(1,4-环己二酮单乙二醇缩酮)为原料合成(如下图)。
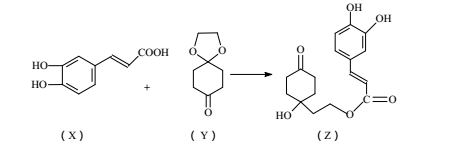
试填空:
(1)X的分子式为_____ ;该分子中最多共面的碳原子数为 ____ 。
(2)Y中是否含有手性碳原子______ (填“是”或“否”)。
(3)Z能发生____ 反应。(填序号)
A.取代反应 B.消去反应 C.加成反应
(4)1molZ与足量的氢氧化钠溶液充分反应,需要消耗氢氧化钠______ mol;1molZ与足量的浓溴水充分反应,需要消耗Br2 _____ mol。

试填空:
(1)X的分子式为
(2)Y中是否含有手性碳原子
(3)Z能发生
A.取代反应 B.消去反应 C.加成反应
(4)1molZ与足量的氢氧化钠溶液充分反应,需要消耗氢氧化钠
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】如图表示不同类型共价键形成时电子云重叠情况:
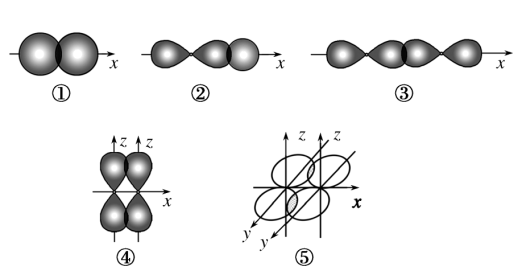
(1)其中形成的化学键属于轴对称的有_______ 。
(2)下列物质中,通过方式①化学键形成的是_______ ;通过方式②化学键形成的是_______ ;只通过方式③化学键形成的是_______ ;同时含有③、④、⑤三种方式化学键的物质是_______ 。
A. Cl2 B.HCl C.N2 D.H2
(3)甲、乙、丙三种有机物的结构如下:
甲: 乙:CH2=CH2丙:
乙:CH2=CH2丙:
①甲分子中有_______ 个σ键,_______ 个π键。
②乙分子中_______ (填“有”或“没有”)极性键,_______ (填“是”或“不是”)极性分子。
③丙分子中σ键与π键的数目之比为_______ 。

(1)其中形成的化学键属于轴对称的有
(2)下列物质中,通过方式①化学键形成的是
A. Cl2 B.HCl C.N2 D.H2
(3)甲、乙、丙三种有机物的结构如下:
甲:
 乙:CH2=CH2丙:
乙:CH2=CH2丙:
①甲分子中有
②乙分子中
③丙分子中σ键与π键的数目之比为
您最近一年使用:0次
【推荐2】从硝酸工业中排放的氮氧化物NOx是一种大气污染物。最常见的吸收法是利用NaOH溶液吸收,发生以下方程:
①NO+NO2=N2O3
②N2O3+2NaOH=2NaNO2+H2O
③2NO2+2NaOH=NaNO2+___________+___________
实验表明,反应②发生的速率大于反应③发生的速率。
(1)补全方程式③并标出电子转移数目:___________ 。
2NO2+2NaOH=NaNO2+___________+___________
(2)NO2的分子构型和分子的极性分别为___________。
(3)C、N、O的第一电离能大小为___________ ,其原因是___________ 。
①NO+NO2=N2O3
②N2O3+2NaOH=2NaNO2+H2O
③2NO2+2NaOH=NaNO2+___________+___________
实验表明,反应②发生的速率大于反应③发生的速率。
(1)补全方程式③并标出电子转移数目:
2NO2+2NaOH=NaNO2+___________+___________
(2)NO2的分子构型和分子的极性分别为___________。
| A.直线形,非极性 | B.角形,极性 | C.平面三角形,非极性 | D.三角锥形,极性 |
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】回答下列问题
(1)按照物质的树状分类和交叉分类,HNO3应属于___________
①酸②氢化物③氧化物④含氧酸⑤难挥发性酸⑥强氧化性酸⑦一元酸⑧化合物
(2)在下列物质中:①HCl、②N2、③NH3、④Na2O2、⑤H2O2、⑥NH4Cl、⑦NaOH、⑧Ar、⑨CO2、⑩C2H4,不存在化学键的是___________ ;只存在非极性键的分子是___________ ;只存在双键的分子是___________ ;只存在σ键的分子是___________ ,既存在σ键又存在π键的分子是___________ ,既存在离子键又存在极性键的是___________ 。(填入序号①~⑩)
(1)按照物质的树状分类和交叉分类,HNO3应属于___________
①酸②氢化物③氧化物④含氧酸⑤难挥发性酸⑥强氧化性酸⑦一元酸⑧化合物
| A.①②③④⑤⑥⑦⑧ | B.①④⑥⑦⑧ | C.①⑨ | D.①④⑤⑥⑦ |
您最近一年使用:0次
【推荐1】
(1)地壳中含量最多的元素基态原子核外未成对电子数为__________ 个。
(2)H2O分子内的O-H键、分子间的范德华力和分子间氢键从强到弱依次为________ 。邻羟基苯甲醛比对羟基苯甲醛的沸点_____ (填“低”或“高”),其原因为_____________ 。
(3)H+可与H2O形成H3O+,H3O+原子采用__________ 杂化。H3O+中H-O-H键角比H2O中H-O-H键角大,原因为__________ 。
(4)CaO与NaCl的晶胞同为面心立方结构,已知CaO晶体密度为a g·cm-3 ,NA表示阿伏加德罗常数,则CaO晶胞体积为_______ cm3
(1)地壳中含量最多的元素基态原子核外未成对电子数为
(2)H2O分子内的O-H键、分子间的范德华力和分子间氢键从强到弱依次为
(3)H+可与H2O形成H3O+,H3O+原子采用
(4)CaO与NaCl的晶胞同为面心立方结构,已知CaO晶体密度为a g·cm-3 ,NA表示阿伏加德罗常数,则CaO晶胞体积为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】(1)比较结合 H+能力的相对强弱:H2O_____ NH3 (填“>”、“<”或“=”);用一个离子 方程式说明 H3O+和 NH4+给出 H+能力的相对强弱_____ 。
(2)NaOCN 是离子化合物,各原子均满足 8 电子稳定结构。写出 NaOCN 的电子式_____ 。
(3)乙酸汽化时,测定气体的相对分子质量,有数据表明其摩尔质量变为 120g·mol-1,从结构上 分析其可能的原因是_____
(2)NaOCN 是离子化合物,各原子均满足 8 电子稳定结构。写出 NaOCN 的电子式
(3)乙酸汽化时,测定气体的相对分子质量,有数据表明其摩尔质量变为 120g·mol-1,从结构上 分析其可能的原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】按要求填空:
(1)某原子含有 6 个质子和 8 个中子,用核素符号表示该原子__________ ;(用元素符号表示)
(2)写电子式:HClO:____ ;NH4+:_____ ;写结构式:CCl4:_____ ;CS2:_____ ;
(3)画出钙原子的原子结构示意图:____ ;画出溴离子的离子结构示意图:____ ;
(4)用电子式表示氯化钠的形成过程:_________________________
(5)按要求排序:
下列离子半径由大到小的顺序是:S2- ;Al3+ ;Na+ ;F- ;______________
下列物质熔沸点由高到低的顺序是:H2O;Na2O;H2Se;I2 ;______________
(1)某原子含有 6 个质子和 8 个中子,用核素符号表示该原子
(2)写电子式:HClO:
(3)画出钙原子的原子结构示意图:
(4)用电子式表示氯化钠的形成过程:
(5)按要求排序:
下列离子半径由大到小的顺序是:S2- ;Al3+ ;Na+ ;F- ;
下列物质熔沸点由高到低的顺序是:H2O;Na2O;H2Se;I2 ;
您最近一年使用:0次



