从硝酸工业中排放的氮氧化物NOx是一种大气污染物。最常见的吸收法是利用NaOH溶液吸收,发生以下方程:
①NO+NO2=N2O3
②N2O3+2NaOH=2NaNO2+H2O
③2NO2+2NaOH=NaNO2+___________+___________
实验表明,反应②发生的速率大于反应③发生的速率。
(1)补全方程式③并标出电子转移数目:___________ 。
2NO2+2NaOH=NaNO2+___________+___________
(2)NO2的分子构型和分子的极性分别为___________。
(3)C、N、O的第一电离能大小为___________ ,其原因是___________ 。
①NO+NO2=N2O3
②N2O3+2NaOH=2NaNO2+H2O
③2NO2+2NaOH=NaNO2+___________+___________
实验表明,反应②发生的速率大于反应③发生的速率。
(1)补全方程式③并标出电子转移数目:
2NO2+2NaOH=NaNO2+___________+___________
(2)NO2的分子构型和分子的极性分别为___________。
| A.直线形,非极性 | B.角形,极性 | C.平面三角形,非极性 | D.三角锥形,极性 |
更新时间:2024-04-12 10:05:57
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】(1)某一反应体系中的物质有:HCl、SnCl2、H2SnCl6、As、H3AsO3、H2O,已知:HCl是反应物之一。
①写出配平的该反应的化学方程式:______________________
②被氧化的元素是____________ 。
(2)氢化亚铜(CuH)是一种难溶物质,用CuSO4溶液和“另一物质”在40~50℃时反应可生成它.CuH具有的性质有:不稳定,易分解;在氯气中能燃烧;与稀盐酸反应能生成气体;Cu+在酸性条件下发生的反应是:2Cu+=Cu2++Cu.
根据以上信息,结合自己所掌握的化学知识,回答下列问题:
①写出CuH在氯气中燃烧的化学反应方程式:___________________________________ .
②如果把CuH溶解在足量的稀硝酸中生成的气体只有NO,请写出CuH溶解在足量稀硝酸中反应的离子方程式:__________________________________________________ .
(3) 在25℃、101kPa下,1g甲醇燃烧生成CO2和液态水时放热22.68kJ。则表示甲醇燃烧热的热化学方程式为________________________________________________
①写出配平的该反应的化学方程式:
②被氧化的元素是
(2)氢化亚铜(CuH)是一种难溶物质,用CuSO4溶液和“另一物质”在40~50℃时反应可生成它.CuH具有的性质有:不稳定,易分解;在氯气中能燃烧;与稀盐酸反应能生成气体;Cu+在酸性条件下发生的反应是:2Cu+=Cu2++Cu.
根据以上信息,结合自己所掌握的化学知识,回答下列问题:
①写出CuH在氯气中燃烧的化学反应方程式:
②如果把CuH溶解在足量的稀硝酸中生成的气体只有NO,请写出CuH溶解在足量稀硝酸中反应的离子方程式:
(3) 在25℃、101kPa下,1g甲醇燃烧生成CO2和液态水时放热22.68kJ。则表示甲醇燃烧热的热化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】
(1)在常温下,发生下列几种反应:
①16H++10Z-+2XO =2X2++5Z2+8H2O
=2X2++5Z2+8H2O
②2A2++B2=2A3++2B-
③2B-+Z2=B2+2Z-
根据上述反应,XO 、Z2、B2、A3+氧化性从强到弱的顺序为:
、Z2、B2、A3+氧化性从强到弱的顺序为:_________________
(2)氧化还原反应中实际上包含氧化和还原两个过程。下面是一个还原过程的反应式:NO + 4H+ + 3e- ═ NO↑ + 2H2O,KMnO4、Na2CO3、Cu2O、Fe2(SO4)3四种物质中的一种物质(甲)能使上述还原过程发生。
+ 4H+ + 3e- ═ NO↑ + 2H2O,KMnO4、Na2CO3、Cu2O、Fe2(SO4)3四种物质中的一种物质(甲)能使上述还原过程发生。
①写出并配平该氧化还原反应的化学方程式_____________________ ;
②反应中硝酸体现了______________ ;
③反应中若产生标准状况下11.2L气体,则转移电子的物质的量是________ mol;
(1)在常温下,发生下列几种反应:
①16H++10Z-+2XO
 =2X2++5Z2+8H2O
=2X2++5Z2+8H2O②2A2++B2=2A3++2B-
③2B-+Z2=B2+2Z-
根据上述反应,XO
 、Z2、B2、A3+氧化性从强到弱的顺序为:
、Z2、B2、A3+氧化性从强到弱的顺序为:(2)氧化还原反应中实际上包含氧化和还原两个过程。下面是一个还原过程的反应式:NO
 + 4H+ + 3e- ═ NO↑ + 2H2O,KMnO4、Na2CO3、Cu2O、Fe2(SO4)3四种物质中的一种物质(甲)能使上述还原过程发生。
+ 4H+ + 3e- ═ NO↑ + 2H2O,KMnO4、Na2CO3、Cu2O、Fe2(SO4)3四种物质中的一种物质(甲)能使上述还原过程发生。①写出并配平该氧化还原反应的化学方程式
②反应中硝酸体现了
③反应中若产生标准状况下11.2L气体,则转移电子的物质的量是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】三草酸合铁酸钾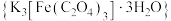 是制备铁触媒上的主要原料。在光照下分解:
是制备铁触媒上的主要原料。在光照下分解:
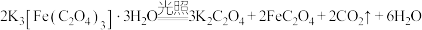 。回答下列问题:
。回答下列问题:
(1)基态 原子的电子排布式为
原子的电子排布式为___________ ,基态 与
与 中未成对电子的数目之比为
中未成对电子的数目之比为___________ 。
(2)三草酸合铁酸钾所含元素中,第一电离能最大的是___________ (填元素符号,下同),电负性最大的是___________ 。
(3)1个 与1个
与1个 分子中
分子中 键数目之比为
键数目之比为___________ , 分子的立体构型为
分子的立体构型为___________ 。
(4)金刚石的晶胞结构如图所示,碳原子分别位于顶点、面心和体内。

若图中原子1的坐标为 ,则原子2的坐标为
,则原子2的坐标为___________ 。
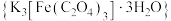 是制备铁触媒上的主要原料。在光照下分解:
是制备铁触媒上的主要原料。在光照下分解: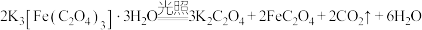 。回答下列问题:
。回答下列问题:(1)基态
 原子的电子排布式为
原子的电子排布式为 与
与 中未成对电子的数目之比为
中未成对电子的数目之比为(2)三草酸合铁酸钾所含元素中,第一电离能最大的是
(3)1个
 与1个
与1个 分子中
分子中 键数目之比为
键数目之比为 分子的立体构型为
分子的立体构型为(4)金刚石的晶胞结构如图所示,碳原子分别位于顶点、面心和体内。

若图中原子1的坐标为
 ,则原子2的坐标为
,则原子2的坐标为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】合成氨是人类科学技术发展史上的一项重大成就,在很大程度上解决了地球上因粮食不足而导致的饥饿问题,是化学和技术对社会发展与进步的巨大贡献。
(1)基态N原子中,能量最高的电子的电子云在空间有___________ 个伸展方向,原子轨道呈___________ 形。
(2) 分子中,N、H电负性大小顺序为
分子中,N、H电负性大小顺序为___________ 。从原子结构的角度分析B、N和O的第一电离能由大到小的顺序为___________ 。
(3)铁触媒是普遍使用的以铁为主体的多成分催化剂,通常还含有 、
、 、CaO、MgO、
、CaO、MgO、 等氧化物中的几种。
等氧化物中的几种。
①Cr原子的价电子排布图为___________ 。
②上述氧化物所涉及的元素中,处于元素周期表中p区的元素是___________ 。
(4)目前合成氨通常采用的压强为10MPa-30MPa、温度为400-500℃,十分耗能。我国科研人员研制出了“Fe-LiH”等催化剂,温度,压强分别降到了350℃、1MPa,这是近年来合成氨反应研究中的重要突破。
①第三电离能
___________ 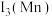 (填“>”或“<”),原因是
(填“>”或“<”),原因是___________ 。
②比较 与
与 的半径大小关系:
的半径大小关系: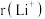
___________  。(填“>”或“<”)
。(填“>”或“<”)
(1)基态N原子中,能量最高的电子的电子云在空间有
(2)
 分子中,N、H电负性大小顺序为
分子中,N、H电负性大小顺序为(3)铁触媒是普遍使用的以铁为主体的多成分催化剂,通常还含有
 、
、 、CaO、MgO、
、CaO、MgO、 等氧化物中的几种。
等氧化物中的几种。①Cr原子的价电子排布图为
②上述氧化物所涉及的元素中,处于元素周期表中p区的元素是
(4)目前合成氨通常采用的压强为10MPa-30MPa、温度为400-500℃,十分耗能。我国科研人员研制出了“Fe-LiH”等催化剂,温度,压强分别降到了350℃、1MPa,这是近年来合成氨反应研究中的重要突破。
①第三电离能

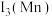 (填“>”或“<”),原因是
(填“>”或“<”),原因是②比较
 与
与 的半径大小关系:
的半径大小关系: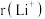
 。(填“>”或“<”)
。(填“>”或“<”)
您最近一年使用:0次
【推荐3】金属氢化物是具有良好发展前景的储氢材料。
(1)LiH中,离子半径:Li+_________ H-(填“>”、“=”或“<”)。
(2)某储氢材料是短周期金属元素M的氢化物。M的部分电离能如下表所示:
M是_________ (填元素符号)。
(3)CH4、NH3、H2O、BCl3、HF分子中键角大小顺序是_____ 。
(4)有以下物质:①H2O,②NaOH,③H2O2,④H2,⑤C2H4,⑥Ar,⑦Na2O2,⑧HCN,既有σ键又有π键的是_____________________ ;只含有σ键的是__________ ;含有由两个原子的s轨道重叠形成的σ键的是________ ;不存在化学键的是________ ;含有离子键和非极性键的是_________ 。
(1)LiH中,离子半径:Li+
(2)某储氢材料是短周期金属元素M的氢化物。M的部分电离能如下表所示:
| I1/kJ·mol-1 | I2/kJ·mol-1 | I3/kJ·mol-1 | I4/kJ·mol-1 | I5/kJ·mol-1 |
| 738 | 1451 | 7733 | 10540 | 13630 |
M是
(3)CH4、NH3、H2O、BCl3、HF分子中键角大小顺序是
(4)有以下物质:①H2O,②NaOH,③H2O2,④H2,⑤C2H4,⑥Ar,⑦Na2O2,⑧HCN,既有σ键又有π键的是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】铝及其化合物广泛应用于金属冶炼、有机合成等领域。
⑴铝热反应可以冶炼金属铬,Cr基态核外电子排布式为_______ 。
⑵已知反应:
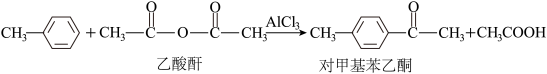
①乙酸酐分子中碳原子轨道的杂化类型为______ 。
②1 mol对甲基苯乙酮分子中含有的σ键的数目为_____ 。
③甲苯分子难溶于水的原因是______ 。
④单个AlCl3气态分子的空间构型为______ ,AlCl3可与Cl-形成AlCl ,与AlCl
,与AlCl 互为等电子体的分子为
互为等电子体的分子为______ 。
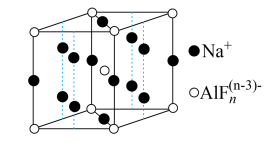
(3)某遮光剂的晶胞如右图所示,则n=______ 。
⑴铝热反应可以冶炼金属铬,Cr基态核外电子排布式为
⑵已知反应:

①乙酸酐分子中碳原子轨道的杂化类型为
②1 mol对甲基苯乙酮分子中含有的σ键的数目为
③甲苯分子难溶于水的原因是
④单个AlCl3气态分子的空间构型为
 ,与AlCl
,与AlCl 互为等电子体的分子为
互为等电子体的分子为(3)某遮光剂的晶胞如右图所示,则n=

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】元素周期表中第ⅦA族包括氟、氯、溴、碘、砹五种元素,统称为卤素。其中代表元素氯富集在海水中,其单质及其化合物在生活、生产中有着广泛地应用。回答下列问题:
(1)基态氯原子能量最高能层上的原子轨道数为______ ;现代化学中,常用光谱分析来鉴定元素,这与原子的___________ 有关。
(2)物质的熔点与其结构密切相关。某同学判断某些卤化物的熔点为NaF>NaCl,SiF4<SiCl4。该同学的主要判断依据是___________ 。
(3)在氢卤酸中,HF是唯一的弱酸,主要原因是__________ 。
(4)光气(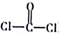 )用作有机合成、农药、药物、染料及其他化工制品的中间体。从电子云的重叠角度分析,该分子中含有的共价键类型是
)用作有机合成、农药、药物、染料及其他化工制品的中间体。从电子云的重叠角度分析,该分子中含有的共价键类型是_______ ,C原子的杂化方式为____ ,分子的空间构型为______ 。
(5)PtCl2(NH3)2为平面结构,可以形成甲、乙两种固体。其中,一种为淡黄色固体,在水中溶解度小;另一种为棕黄色固体,在水中溶解度大,是癌症治疗的常用化学药物。
① 棕黄色固体是图中的___ (填“甲”或“乙”),试解释它在水中的溶解度比淡黄色固体大的原因是___ 。
② Pt原子在三维空间里可按图 所示方式堆积形成金属Pt晶体:
该晶胞的堆积方式为____ ,M 原子的配位数为________ ,若该晶体的密度为ρg·cm3,阿伏伽德罗常数的值为NA,则Pt原子的原子半径为______ pm。
(1)基态氯原子能量最高能层上的原子轨道数为
(2)物质的熔点与其结构密切相关。某同学判断某些卤化物的熔点为NaF>NaCl,SiF4<SiCl4。该同学的主要判断依据是
(3)在氢卤酸中,HF是唯一的弱酸,主要原因是
(4)光气(
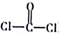 )用作有机合成、农药、药物、染料及其他化工制品的中间体。从电子云的重叠角度分析,该分子中含有的共价键类型是
)用作有机合成、农药、药物、染料及其他化工制品的中间体。从电子云的重叠角度分析,该分子中含有的共价键类型是(5)PtCl2(NH3)2为平面结构,可以形成甲、乙两种固体。其中,一种为淡黄色固体,在水中溶解度小;另一种为棕黄色固体,在水中溶解度大,是癌症治疗的常用化学药物。
① 棕黄色固体是图中的

② Pt原子在三维空间里可按图 所示方式堆积形成金属Pt晶体:
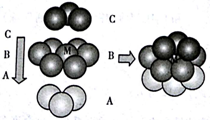
该晶胞的堆积方式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】回答下列问题
(1) 是一种重要的无机化合物,可作食盐的补碘剂
是一种重要的无机化合物,可作食盐的补碘剂
①基态K原子中核外电子占据的最高能层的符号是_______ ,占据该能层电子的电子云轮廓图形状为_______ 。K和Cr属于同一周期,且核外最外层电子构型相同,但金属K的熔点、沸点都比金属Cr的低,原因是_______ 。
② 的阴离子,中心原子的价层电子对数为
的阴离子,中心原子的价层电子对数为_______ ,其VSEPR模型名称为_______ 。
(2)Mn、Fe均为第四周期过渡元素,两元素的部分电离能(I)数据列于下表:
回答下列问题:
Mn元素价电子层的电子排布式为_______ ,比较两元素的 、
、 可知,气态
可知,气态 失去一个电子比气态
失去一个电子比气态 再失去一个电子难。对此你的解释是
再失去一个电子难。对此你的解释是_______ 。
(1)
 是一种重要的无机化合物,可作食盐的补碘剂
是一种重要的无机化合物,可作食盐的补碘剂①基态K原子中核外电子占据的最高能层的符号是
②
 的阴离子,中心原子的价层电子对数为
的阴离子,中心原子的价层电子对数为(2)Mn、Fe均为第四周期过渡元素,两元素的部分电离能(I)数据列于下表:
| 元素 | Mn | Fe | |
| 电离能(kJ/mol) |  | 717 | 759 |
 | 1509 | 1561 | |
 | 3248 | 2957 | |
Mn元素价电子层的电子排布式为
 、
、 可知,气态
可知,气态 失去一个电子比气态
失去一个电子比气态 再失去一个电子难。对此你的解释是
再失去一个电子难。对此你的解释是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】元素A、B、C都是短周期元素,A元素原子的2p轨道上只有两个未成对电子,B的3p轨道上有空轨道,A、B同主族,B、C同周期,C是本周期中电负性最大的.
请回答:
(1)A原子的核外电子排布的电子排布图______________ ,B原子的核外电子排布式________ ,C原子的价电子排布式____________ 。
(2)A、B、C的气态氢化物的化学式分别是___________ ,其中最不稳定的是__________ 。
(3)它们的最高价氧化物的水化物中,酸性最强的是_________ 。
(4)AC4的化学式___________ ,结构式__________ ,中心原子A的杂化方式________ 杂化,是__________ (填“极性”或“非极性”)分子。
请回答:
(1)A原子的核外电子排布的电子排布图
(2)A、B、C的气态氢化物的化学式分别是
(3)它们的最高价氧化物的水化物中,酸性最强的是
(4)AC4的化学式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】(1) 是一种常用溶剂,每个
是一种常用溶剂,每个 分子中存在
分子中存在___________ 个 键。在H-S、H-Cl两种共价键中,化学键的极性较大的是
键。在H-S、H-Cl两种共价键中,化学键的极性较大的是___________ ,键长较长的是___________ 。
(2)水与 中,分子极性较小的是
中,分子极性较小的是___________ (填分子式)。
(3) 与
与 分子的空间结构分别是
分子的空间结构分别是___________ 和___________ ;相同条件下两者在水中的溶解度较大的是___________ (写分子式),理由是___________ 。
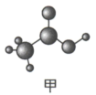
(4)醋酸分子的球棍模型如图甲所示。在醋酸分子中,碳原子的轨道杂化类型有___________ 。
 是一种常用溶剂,每个
是一种常用溶剂,每个 分子中存在
分子中存在 键。在H-S、H-Cl两种共价键中,化学键的极性较大的是
键。在H-S、H-Cl两种共价键中,化学键的极性较大的是(2)水与
 中,分子极性较小的是
中,分子极性较小的是(3)
 与
与 分子的空间结构分别是
分子的空间结构分别是(4)醋酸分子的球棍模型如图甲所示。在醋酸分子中,碳原子的轨道杂化类型有

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】按要求回答以下内容。
(1)Cu基态原子的价电子排布式_______ ; 它位于周期表的_______ 区。
(2)基态S原子电子占据最高能级的电子云轮廓图为_______ 形; SO2分子中的中心原子杂化方式为_______ ,SO 的空间结构为
的空间结构为_______ 。
(3)近期我国科学家对嫦娥五号月球土壤样品进行了分析,研究表明每吨月壤样品的钛含量是地球土壤平均含量的6倍多。Ti 在元素周期表的位置_______ ; 基态Ti原子的电子排布式 _______ 。
(4)H2O2的空间结构示意图如下。
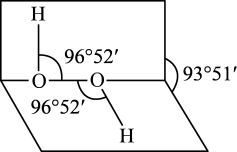
①下列关于H2O2的说法中正确的是_______ (填字母)。
A.分子中有极性键 B.分子中有非极性键
C.氧原子的轨道发生了sp2 杂化 D.分子是非极性分子
②H2O2可使酸性K2Cr2O7溶液由橙黄色变为绿色,铬元素被还原为+3价,该反应的离子方程式是_______ 。
(1)Cu基态原子的价电子排布式
(2)基态S原子电子占据最高能级的电子云轮廓图为
 的空间结构为
的空间结构为(3)近期我国科学家对嫦娥五号月球土壤样品进行了分析,研究表明每吨月壤样品的钛含量是地球土壤平均含量的6倍多。Ti 在元素周期表的位置
(4)H2O2的空间结构示意图如下。

①下列关于H2O2的说法中正确的是
A.分子中有极性键 B.分子中有非极性键
C.氧原子的轨道发生了sp2 杂化 D.分子是非极性分子
②H2O2可使酸性K2Cr2O7溶液由橙黄色变为绿色,铬元素被还原为+3价,该反应的离子方程式是
您最近一年使用:0次



