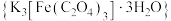 是制备铁触媒上的主要原料。在光照下分解:
是制备铁触媒上的主要原料。在光照下分解: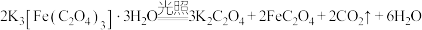 。回答下列问题:
。回答下列问题:(1)基态
 原子的电子排布式为
原子的电子排布式为 与
与 中未成对电子的数目之比为
中未成对电子的数目之比为(2)三草酸合铁酸钾所含元素中,第一电离能最大的是
(3)1个
 与1个
与1个 分子中
分子中 键数目之比为
键数目之比为 分子的立体构型为
分子的立体构型为(4)金刚石的晶胞结构如图所示,碳原子分别位于顶点、面心和体内。

若图中原子1的坐标为
 ,则原子2的坐标为
,则原子2的坐标为相似题推荐
(1)图a、b、c分别表示C、N、O和F的逐级电离能I变化趋势(纵坐标的标度不同)。第二电离能的变化图是
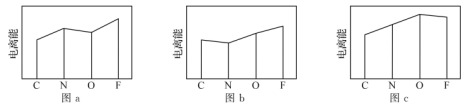
(2)已知C—H、C—F的键能分别为413.4
 、485
、485 。在2022年冬奥会上“水立方”华丽转身为“冰立方”,实现了奥运场馆的再利用,其美丽的透光气囊材料由乙烯(
。在2022年冬奥会上“水立方”华丽转身为“冰立方”,实现了奥运场馆的再利用,其美丽的透光气囊材料由乙烯( )与四氟乙烯(
)与四氟乙烯( )的共聚物(ETFE)制成。
)的共聚物(ETFE)制成。 、
、 分子的稳定性关系:前者
分子的稳定性关系:前者(3)相同条件下,
 与
与 在水中的溶解度较大的是
在水中的溶解度较大的是(4)已知
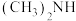 比
比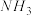 接收质子的能力强,可能的原因是
接收质子的能力强,可能的原因是(1)四种元素中第一电离能最大的是
(2)A有两种同素异形体,其中沸点较高的是
(3)化合物CD3中心原子的杂化轨道类型为
(4)化合物D2A的立体构型为
(5)CuSO4溶液可用作C4中毒的解毒剂,反应可生成C的最高价含氧酸和铜,该反应的化学方程式为:
(6)A和B形成化合物F,晶胞结构如图所示,晶胞参致a=0.566nm,晶胞中A原子的配位数为

【推荐3】根据信息回答下列问题:
(1)如图是部分元素原子的第一电离能I1随原子序数变化的曲线图(其中12号至17号元素的有关数据缺失)。
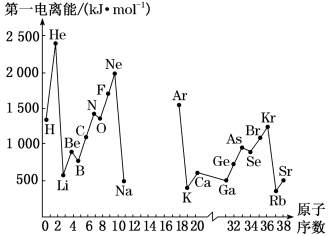
①认真分析图中同周期元素第一电离能的变化规律,推断Na~Ar元素中,Al的第一电离能的大小范围为
②图中Ge元素中未成对电子有
(2)已知元素的电负性和元素的化合价一样,也是元素的一种基本性质。下面给出部分元素的电负性:
元素 | Al | B | Be | C | Cl | F | Li |
电负性 | 2.0 | 1.5 | 2.5 | 3.0 | 4.0 | 1.0 | |
元素 | Mg | N | Na | O | P | S | Si |
电负性 | 1.2 | 3.0 | 0.9 | 3.5 | 2.1 | 2.5 | 1.8 |
已知:两成键元素间电负性差值大于1.7时,形成离子键,两成键元素间电负性差值小于1.7时,形成共价键。
①根据表中给出的数据,可推知元素的电负性具有的变化规律
②通过分析电负性值变化规律,确定Al元素电负性值的最小范围
③判断下列物质是离子化合物还是共价化合物:
A Li3N B PCl3 C MgCl2 D SiC
Ⅰ.属于离子化合物的是
Ⅱ.属于共价化合物的是
请设计一个实验方案证明上述所得到的结论
(1)硅能形成与烷烃类似的硅烷,写出乙硅烷的电子式:
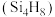 中
中 键与
键与 键的个数比为
键的个数比为(2)我国航天事业发展迅猛,太阳能电池材料使用的是砷化镓(GaAs)。基态砷原子中电子占据的最高能层符号是
(3)光催化还原
 制备
制备 的反应中,带状纳米
的反应中,带状纳米 是该反应的良好催化剂。Zn、Ge、O电负性由大到小的顺序是
是该反应的良好催化剂。Zn、Ge、O电负性由大到小的顺序是(4)硅和锗都能与氯元素形成四氯化物
 和
和 ,从原子结构角度解释原因:
,从原子结构角度解释原因:(5)太阳能电池材料的很多金属或金属化合物在灼烧时会产生特殊的火焰颜色,请用原子结构的知识阐述产生此现象的原因:
 是微电子工业中优良的等离子刻蚀气体,
是微电子工业中优良的等离子刻蚀气体, 分子的空间结构为
分子的空间结构为 中,N原子的杂化轨道类型为
中,N原子的杂化轨道类型为(2)在5-氨基四唑(
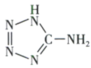 )中所含元素的电负性由大到小的顺序为
)中所含元素的电负性由大到小的顺序为 键数目为
键数目为(3)
 的空间结构为
的空间结构为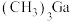 分子空间结构为平面三角形,则其中镓原子的杂化方式是
分子空间结构为平面三角形,则其中镓原子的杂化方式是(1)基态N原子中,核外电子占据的最高能层的符号是
(2)写出3p轨道上有2个未成对电子的元素的符号:
(3)某元素被科学家称之为人体微量元素中的“防癌之王”,其原子的外围电子排布式为4s24p4,该元素的名称是
(4)已知铁是26号元素,写出Fe的价层电子排布式
(5)从原子结构的角度分析B、N和O的第一电离能由大到小的顺序为
(6)写出C的核外电子排布图为:
(7)Zn2+的核外电子排布式为
(2)根据VSEPR模型,H3O+的分子立体结构为
(3)按要求写出由第二周期元素为中心原子,通过sp3杂化形成中性分子的化学式(各写一种)
正四面体分子
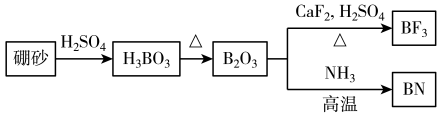
请回答下列问题:
(1) 在BF3分子中,F-B-F的键角是
 的立体结构为
的立体结构为(2)在与石墨结构相似的六方氮化硼晶体中,层内B原子与N原子之间的化学键为
(1)下列分子中若有手性原子,请用“*”标出其手性碳原子
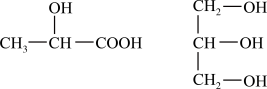
(2)试比较下列含氧酸的酸性强弱(填“>”、“<”或“=”):H2SO4
(3)根据价层电子对互斥理论判断下列问题:H2S分子的VSEPR构型为
(4)H2O的沸点(100℃)比H2S的沸点(-61℃)高,这是由于
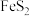 晶胞为立方体,边长为
晶胞为立方体,边长为 ,如图所示。
,如图所示。
(1)与
 紧邻的阴离子个数为
紧邻的阴离子个数为(2)晶胞的密度为

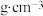 。
。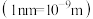
Ⅰ.金的结构
(1)金元素位于元素周期表第6周期ⅠB族,金的价电子排布式为
(2)金晶体的晶胞为面心立方晶胞,Au在晶胞中的配位数是
Ⅱ.金的提取
硫脲(
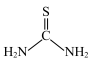 )液相提金原理:
)液相提金原理:
(3)硫脲易溶于水,原因是
Ⅲ.金的应用
一种最稳定的负载型纳米金团簇,具有最完美的对称性,其结构如图所示:
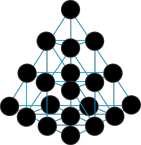
(4)该金团簇的化学式为
a.Au b.
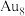 c.
c.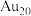
(5)该金团簇中有



