根据信息回答下列问题:
(1)如图是部分元素原子的第一电离能I1随原子序数变化的曲线图(其中12号至17号元素的有关数据缺失)。
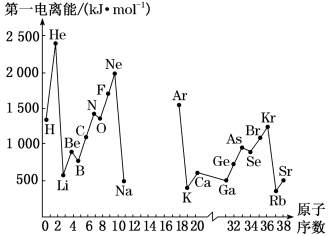
①认真分析图中同周期元素第一电离能的变化规律,推断Na~Ar元素中,Al的第一电离能的大小范围为
②图中Ge元素中未成对电子有
(2)已知元素的电负性和元素的化合价一样,也是元素的一种基本性质。下面给出部分元素的电负性:
元素 | Al | B | Be | C | Cl | F | Li |
电负性 | 2.0 | 1.5 | 2.5 | 3.0 | 4.0 | 1.0 | |
元素 | Mg | N | Na | O | P | S | Si |
电负性 | 1.2 | 3.0 | 0.9 | 3.5 | 2.1 | 2.5 | 1.8 |
已知:两成键元素间电负性差值大于1.7时,形成离子键,两成键元素间电负性差值小于1.7时,形成共价键。
①根据表中给出的数据,可推知元素的电负性具有的变化规律
②通过分析电负性值变化规律,确定Al元素电负性值的最小范围
③判断下列物质是离子化合物还是共价化合物:
A Li3N B PCl3 C MgCl2 D SiC
Ⅰ.属于离子化合物的是
Ⅱ.属于共价化合物的是
请设计一个实验方案证明上述所得到的结论
相似题推荐
I.光伏材料是指能将太阳能直接转换成电能的材料。光伏材料又称太阳能材料,只有半导体材料具有这种功能。可作太阳能电池材料的有单晶硅、多晶硅、非晶硅、GaAs、GaAlAs、InP、CdS、CdTe等。
(1)写出31号元素镓(Ga)的原子结构示意图:
(2)P、S、Ga电负性从大到小的顺序为
(3)As元素的第一电离能
(4)写出原子序数最小的第VIII族元素基态原子的核外电子排布式:
(5)写出3p轨道上只有2个未成对电子的元素的符号:
II.从化学键的角度分析,化学反应的过程就是反应物的化学键断裂和生成物的化学键形成的过程。在化学反应过程中,断裂化学键需要消耗能量,形成化学键又会释放能量。
| 化学键 | H—H | N—H | N≡N |
| 键能/(kJ/mol) | 436 | 391 | 945 |

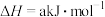 ,根据上表中所列键能数据可计算出a=
,根据上表中所列键能数据可计算出a=(1)周期表中元素E位于第
(2)化合物R的电子式为
(3)B—的电子排布式为
(4)C的氢化物的空间构型为
(5)B元素的电负性
(1)在第三周期中,第一电离能最小的元素是
(2)在元素周期表中,电负性最大的元素是
(3)最活泼的金属元素是
(4)最活泼的非金属元素是
(5)第二、三、四周期元素中p轨道半充满的原子是
(6)电负性相差最大的两种元素是
(1)三乙醇胺的制备:
 。三乙醇胺所含的元素中,电负性由小到大的顺序为
。三乙醇胺所含的元素中,电负性由小到大的顺序为(2)辉砷钴矿(主要成分为
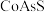 )是一种常见的钴矿石。
)是一种常见的钴矿石。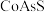 中三种元素的电负性大小关系为
中三种元素的电负性大小关系为元素 | H | Li | Be | B | C | N | O | F |
电负性 | 2.1 | 1.0 | 1.5 | 2.0 | 2.5 | 3.0 | 3.5 | 4.0 |
元素 | Na | Mg | Al | Si | P | S | Cl | K |
电负性 | 0.9 | 1.2 | 1.5 | 1.7 | 2.1 | 2.3 | 3.0 | 0.8 |
(1)根据表中所给数据分析,同主族内不同元素X值的变化规律是
(2)预测周期表中电负性最大的元素应为
(3)经验规律告诉我们:当形成化学键的两原子相应元素的电负性差值大于1.7时,所形成的化学键一般为离子键;当小于1.7时,一般为共价键。试推断AlBr3中的化学键类型为

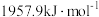 、
、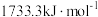 ,前者高于后者的原因是
,前者高于后者的原因是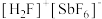 (氟锑酸,是一种超强酸),其中阳离子
(氟锑酸,是一种超强酸),其中阳离子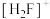 的空间构型为
的空间构型为

