在下列横线上,填上适当的元素符号:
(1)在第三周期中,第一电离能最小的元素是_________ ,第一电离能最大的元素是______ 。
(2)在元素周期表中,电负性最大的元素是_______ ,电负性最小的元素是_________ (放射性元素除外)。
(3)最活泼的金属元素是_______ 。
(4)最活泼的非金属元素是______ 。
(5)第二、三、四周期元素中p轨道半充满的原子是_______ 。
(6)电负性相差最大的两种元素是________ (放射性元素除外)。
(1)在第三周期中,第一电离能最小的元素是
(2)在元素周期表中,电负性最大的元素是
(3)最活泼的金属元素是
(4)最活泼的非金属元素是
(5)第二、三、四周期元素中p轨道半充满的原子是
(6)电负性相差最大的两种元素是
19-20高二·全国·课时练习 查看更多[5]
第3节 原子结构与元素性质——A学习区 夯实基础(鲁科版选修3)(已下线)1.3.2 元素的电负性及其变化规律-2020-2021学年高二化学课时同步练(鲁科2019选择性必修2)(已下线)1.2.2 原子结构与元素周期律(基础过关A练)-2021-2022学年高二化学课时过关提优AB练(人教版2019选择性必修2)(已下线)1.2.3 元素的电负性及其变化规律-2021-2022学年高二化学同步课时跟踪训练(人教版2019选择性必修2)1.3.2元素的电离能、电负性及其变化规律(课后)-鲁科版选择性必修2
更新时间:2020-04-09 11:19:05
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】根据原子结构、元素周期表和元素周期律的知识回答下列问题:
(1)某元素原子基态核外电子有14种不同的运动状态,该元素位于第____ 周期第____ 族,属于____ 区,占据最高能级的电子云轮廓图为____ 形。
(2)1~36号元素中基态原子核外电子排布中未成对电子数最多的元素的核外电子排布式是____ ,其价电子轨道表示式为____ 。
(3)价电子排布式为3d54s2的原子,其原子结构示意图为____ ,其最高正价为____ 价。
(4)《中华本草》等中医典籍中,记载了炉甘石(ZnCO3)入药,可用于治疗皮肤炎症或表面创伤。ZnCO3中,阴离子空间构型为____ ,C原子的杂化方式为____ 。
(1)某元素原子基态核外电子有14种不同的运动状态,该元素位于第
(2)1~36号元素中基态原子核外电子排布中未成对电子数最多的元素的核外电子排布式是
(3)价电子排布式为3d54s2的原子,其原子结构示意图为
(4)《中华本草》等中医典籍中,记载了炉甘石(ZnCO3)入药,可用于治疗皮肤炎症或表面创伤。ZnCO3中,阴离子空间构型为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】金属铝质轻且有良好的防腐蚀性,在国防工业中有非常重要的作用。完成下列填空:
(1)铝原子核外电子云有___ 种不同的伸展方向,有___ 种不同运动状态的电子。
(2)镓(Ga)与铝同族。写出镓的氯化物和氨水反应的化学方程式___ 。
(3)硅与铝同周期。SiO2是硅酸盐玻璃(Na2CaSi6O14)的主要成分,Na2CaSi6O14也可写成氧化物形式___ 。盛放NaOH溶液的试剂瓶若用玻璃瓶塞容易形成粘性的硅酸盐而无法打开,发生反应的化学方程式为___ 。长石是铝硅盐酸,不同类长石其氧原子的物质的量分数相同。由钠长石化学式NaAlSi3O8可推知钙长石的化学式为___ 。
(4)用铝和金属氧化物反应制备金属单质是工业上常用的方法。如:2Al+4BaO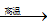 3Ba↑+BaO•Al2O3。常温下Al的金属性比Ba的金属性
3Ba↑+BaO•Al2O3。常温下Al的金属性比Ba的金属性___ (选填“强”“弱”)。利用上述方法可制取Ba的主要原因是___ 。
a.高温时Al的活泼性大于Ba b.高温有利于BaO分解
c.高温时BaO•Al2O3比Al2O3稳定 d.Ba的沸点比Al的低
(1)铝原子核外电子云有
(2)镓(Ga)与铝同族。写出镓的氯化物和氨水反应的化学方程式
(3)硅与铝同周期。SiO2是硅酸盐玻璃(Na2CaSi6O14)的主要成分,Na2CaSi6O14也可写成氧化物形式
(4)用铝和金属氧化物反应制备金属单质是工业上常用的方法。如:2Al+4BaO
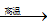 3Ba↑+BaO•Al2O3。常温下Al的金属性比Ba的金属性
3Ba↑+BaO•Al2O3。常温下Al的金属性比Ba的金属性a.高温时Al的活泼性大于Ba b.高温有利于BaO分解
c.高温时BaO•Al2O3比Al2O3稳定 d.Ba的沸点比Al的低
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】百余种不同的元素,是构成大千世界中所有物质的“基石”。科学家们根据元素的性质递变规律、电子排布等对元素进行编排设计元素周期表。根据所学内容完成以下题目:
Ⅰ.硫代碳酸钠能用于处理废水中的重金属离子,可通过反应制备: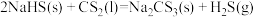
(1) 的结构示意图是
的结构示意图是___________ , 的分子构型是
的分子构型是___________ 。
(2)用电子式表示 的形成过程
的形成过程___________ 。
(3)下列事实中,能说明硫的非金属性比碳强的是___________ 。(填选项)
a. 的酸性比
的酸性比 的酸性强
的酸性强
b.在硫与碳的化合物 中S显负价
中S显负价
c.足量硫酸加入碳酸钠溶液中能生成二氧化碳气体
d.硫的单质的硬度比金刚石低
(4)结合原子结构知识,从键长、键能角度阐释 比
比 更稳定的原因
更稳定的原因___________ 。
Ⅱ.氢能是一种清洁的可再生能源,储存氢能是其开发的重要环节,其中 是较好的储氢材料。
是较好的储氢材料。
(5) 元素位于元素周期表的
元素位于元素周期表的___________ 。
(6)由元素周期律能得到___________ 。(填选项)
a.碱性: b.与水反应的剧烈程度:
b.与水反应的剧烈程度:
c.溶解性: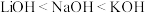 d.密度:
d.密度:
(7) 中不存在的作用力有
中不存在的作用力有___________ 。(填选项)
a.离子键 b.共价键 c.金属键 d.分子间作用力
Ⅲ.如果给核外电子足够的能量,这些电子便会摆脱原子核的束缚而离去。核外电子离开该原子或离子所需要的能量主要受两大因素的影响:
①原子核对核外电子的吸引力
②形成稳定结构的倾向,一般最外层电子为2、8、4的原子较为稳定
以下是一些原子核失去核外不同电子所需要的能量(kJ/mol)
注:阴影表示与上一数据存在显著性差异
(8)已知元素a是短周期元素,根据所给信息分析,表中元素a最有可能是___________ 。
(9)根据所给信息分析,为什么 失去一个电子所需要的能量大于
失去一个电子所需要的能量大于
___________ 。
Ⅰ.硫代碳酸钠能用于处理废水中的重金属离子,可通过反应制备:
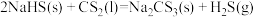
(1)
 的结构示意图是
的结构示意图是 的分子构型是
的分子构型是(2)用电子式表示
 的形成过程
的形成过程(3)下列事实中,能说明硫的非金属性比碳强的是
a.
 的酸性比
的酸性比 的酸性强
的酸性强b.在硫与碳的化合物
 中S显负价
中S显负价c.足量硫酸加入碳酸钠溶液中能生成二氧化碳气体
d.硫的单质的硬度比金刚石低
(4)结合原子结构知识,从键长、键能角度阐释
 比
比 更稳定的原因
更稳定的原因Ⅱ.氢能是一种清洁的可再生能源,储存氢能是其开发的重要环节,其中
 是较好的储氢材料。
是较好的储氢材料。(5)
 元素位于元素周期表的
元素位于元素周期表的(6)由元素周期律能得到
a.碱性:
 b.与水反应的剧烈程度:
b.与水反应的剧烈程度:
c.溶解性:
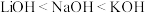 d.密度:
d.密度:
(7)
 中不存在的作用力有
中不存在的作用力有a.离子键 b.共价键 c.金属键 d.分子间作用力
Ⅲ.如果给核外电子足够的能量,这些电子便会摆脱原子核的束缚而离去。核外电子离开该原子或离子所需要的能量主要受两大因素的影响:
①原子核对核外电子的吸引力
②形成稳定结构的倾向,一般最外层电子为2、8、4的原子较为稳定
以下是一些原子核失去核外不同电子所需要的能量(kJ/mol)
| 失去第n个电子 | 锂 | 元素a | 镁 | 铝 |
| 失去第1个电子 | 520 | 502 | 738 | 580 |
| 失去第2个电子 | 1451 | 1820 | ||
| 失去第3个电子 | 11815 | 6920 | 2750 | |
| 失去第4个电子 | 9550 | 10540 |
(8)已知元素a是短周期元素,根据所给信息分析,表中元素a最有可能是
(9)根据所给信息分析,为什么
 失去一个电子所需要的能量大于
失去一个电子所需要的能量大于
您最近一年使用:0次
【推荐2】根据元素周期表中完整周期元素的性质,完成下列空格。
(1)在第三周期中,第一电离能最小的元素符号是___________ ,其原子的结构示意图为___________ ,第一电离能最大的元素符号是___________ ,其价电子排布式为___________ 。
(2)在元素周期表中,电负性最大的元素名称是___________ ,其价电子排布图为___________ 。
(1)在第三周期中,第一电离能最小的元素符号是
(2)在元素周期表中,电负性最大的元素名称是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】有机物种类繁多,应用广泛。
(1)邻氨基吡啶(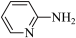 )的铜配合物在有机不对称合成中起催化诱导效应。邻氨基吡啶中所有元素的电负性由大到小的顺序为
)的铜配合物在有机不对称合成中起催化诱导效应。邻氨基吡啶中所有元素的电负性由大到小的顺序为_______ (填元素符号)。 能溶于水的原因是
能溶于水的原因是_______ 。
(2)鸟嘌呤和吡咯的结构如下图所示。
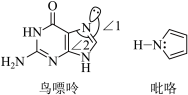
①鸟嘌呤中N原子的杂化方式为_______ ,夹角∠1_______ ∠2(填“>”或“<”)。
②分子中的大 键可以用符号
键可以用符号 表示,其中m代表参与形成大
表示,其中m代表参与形成大 键的原子数,n代表参与形成大
键的原子数,n代表参与形成大 键的电子数,吡咯中的大
键的电子数,吡咯中的大 键可表示为
键可表示为_______ 。
(3)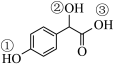 分子中3个-OH的电离能力由强到弱的顺序是
分子中3个-OH的电离能力由强到弱的顺序是_______ (用①、②、③表示)。
(4)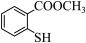 与
与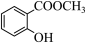 相比,前者的水溶性更
相比,前者的水溶性更_______ (填“大”或“小”)。—SH与—OH性质相似,写出与NaOH溶液反应的化学方程式_______ 。
(1)邻氨基吡啶(
 )的铜配合物在有机不对称合成中起催化诱导效应。邻氨基吡啶中所有元素的电负性由大到小的顺序为
)的铜配合物在有机不对称合成中起催化诱导效应。邻氨基吡啶中所有元素的电负性由大到小的顺序为 能溶于水的原因是
能溶于水的原因是(2)鸟嘌呤和吡咯的结构如下图所示。

①鸟嘌呤中N原子的杂化方式为
②分子中的大
 键可以用符号
键可以用符号 表示,其中m代表参与形成大
表示,其中m代表参与形成大 键的原子数,n代表参与形成大
键的原子数,n代表参与形成大 键的电子数,吡咯中的大
键的电子数,吡咯中的大 键可表示为
键可表示为(3)
 分子中3个-OH的电离能力由强到弱的顺序是
分子中3个-OH的电离能力由强到弱的顺序是(4)
 与
与 相比,前者的水溶性更
相比,前者的水溶性更
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】已知元素的电负性和原子半径一样,也是元素的基本性质。下表给出14种元素的电负性:
试结合元素周期律相关知识完成下列问题。
(1)根据上表给出的数据,可推知元素的电负性具有的变化规律是__________ (从电负性与结构的关系考虑)。
(2)请预测Br与I元素电负性的大小关系:_________ 。
(3)经验规律告诉我们:当成键的两原子相应元素的电负性差值大于1.7时,一般为离子键,而小于1.7时,一般为共价键。试推断 中化学键的类型是
中化学键的类型是 ___________ 。
(4)预测元素周期表中电负性最小的元素是_____ (放射性元素除外)。
| 元素 | AL | B | Be | C | Cl | F | Li | Mg | N | Na | O | P | S | Si |
| 电负性 | 1.5 | 2.0 | 1.5 | 2.5 | 3.0 | 4.0 | 1.0 | 1.2 | 3.0 | 0.9 | 3.5 | 2.1 | 2.5 | 1.8 |
试结合元素周期律相关知识完成下列问题。
(1)根据上表给出的数据,可推知元素的电负性具有的变化规律是
(2)请预测Br与I元素电负性的大小关系:
(3)经验规律告诉我们:当成键的两原子相应元素的电负性差值大于1.7时,一般为离子键,而小于1.7时,一般为共价键。试推断
 中化学键的类型是
中化学键的类型是 (4)预测元素周期表中电负性最小的元素是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】离子液体被认为是21世纪理想的绿色溶剂,是指室温或者接近室温时呈液态,而本身由阴、阳离子构成的化合物。某离子液体[bmim]Cl可与 混合形成离子液体;[bmim]Cl也可以转化成其他离子液体。如图是[bmim]Cl与
混合形成离子液体;[bmim]Cl也可以转化成其他离子液体。如图是[bmim]Cl与 离子交换反应合成离子液体[bmim]
离子交换反应合成离子液体[bmim]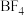 的流程。
的流程。

(1)[bmim]}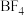 中C原子的杂化方式为
中C原子的杂化方式为___________ , 的空间构型为
的空间构型为___________ 。
(2)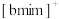 阳离子中的几种元素电负性由大到小顺序为
阳离子中的几种元素电负性由大到小顺序为___________ 。
(3)已知分子中的大π键可以用 表示,其中m代表参与形成大π键的原子数,n代表大π键中的电子数,则
表示,其中m代表参与形成大π键的原子数,n代表大π键中的电子数,则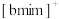 中五元环大π键可以表示为
中五元环大π键可以表示为___________ 。
(4) 熔点为77.8℃,
熔点为77.8℃, 熔点高于1000℃,其原因是
熔点高于1000℃,其原因是___________ 。
(5) 和[bmim]Cl混合形成离子液体的过程中会存在以下转化:
和[bmim]Cl混合形成离子液体的过程中会存在以下转化: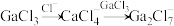 ,已知一个
,已知一个 中含有两个配位键,试画出
中含有两个配位键,试画出 的结构式:
的结构式:___________ 。
(6)氟及其化合物的用途非常广泛。
①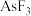 、
、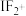 、
、 、
、 中价层电子对数不同于其他微粒的为
中价层电子对数不同于其他微粒的为___________ 。
②基于 设计的Borm-Haber循环如图所示。
设计的Borm-Haber循环如图所示。
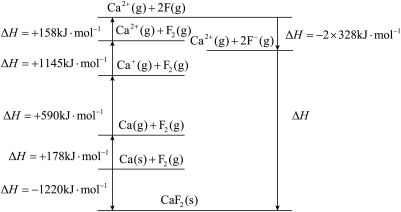
由图可知,F-F键的键能为___________  ;钙的第一电离能为
;钙的第一电离能为___________  。
。
 混合形成离子液体;[bmim]Cl也可以转化成其他离子液体。如图是[bmim]Cl与
混合形成离子液体;[bmim]Cl也可以转化成其他离子液体。如图是[bmim]Cl与 离子交换反应合成离子液体[bmim]
离子交换反应合成离子液体[bmim]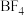 的流程。
的流程。
(1)[bmim]}
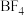 中C原子的杂化方式为
中C原子的杂化方式为 的空间构型为
的空间构型为(2)
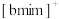 阳离子中的几种元素电负性由大到小顺序为
阳离子中的几种元素电负性由大到小顺序为(3)已知分子中的大π键可以用
 表示,其中m代表参与形成大π键的原子数,n代表大π键中的电子数,则
表示,其中m代表参与形成大π键的原子数,n代表大π键中的电子数,则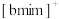 中五元环大π键可以表示为
中五元环大π键可以表示为(4)
 熔点为77.8℃,
熔点为77.8℃, 熔点高于1000℃,其原因是
熔点高于1000℃,其原因是(5)
 和[bmim]Cl混合形成离子液体的过程中会存在以下转化:
和[bmim]Cl混合形成离子液体的过程中会存在以下转化: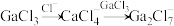 ,已知一个
,已知一个 中含有两个配位键,试画出
中含有两个配位键,试画出 的结构式:
的结构式:(6)氟及其化合物的用途非常广泛。
①
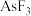 、
、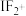 、
、 、
、 中价层电子对数不同于其他微粒的为
中价层电子对数不同于其他微粒的为②基于
 设计的Borm-Haber循环如图所示。
设计的Borm-Haber循环如图所示。
由图可知,F-F键的键能为
 ;钙的第一电离能为
;钙的第一电离能为 。
。
您最近一年使用:0次

 基态核外电子排布式为
基态核外电子排布式为 基态核外电子排布式为
基态核外电子排布式为


