能源、材料与生产生活和社会发展密切相关。
I.光伏材料是指能将太阳能直接转换成电能的材料。光伏材料又称太阳能材料,只有半导体材料具有这种功能。可作太阳能电池材料的有单晶硅、多晶硅、非晶硅、GaAs、GaAlAs、InP、CdS、CdTe等。
(1)写出31号元素镓(Ga)的原子结构示意图:_______ 。
(2)P、S、Ga电负性从大到小的顺序为_______ 。
(3)As元素的第一电离能_______ (填“大于”“小于”或“等于”)Se元素的第一电离能。
(4)写出原子序数最小的第VIII族元素基态原子的核外电子排布式:_______ 。
(5)写出3p轨道上只有2个未成对电子的元素的符号:_______ 、_______ 。
II.从化学键的角度分析,化学反应的过程就是反应物的化学键断裂和生成物的化学键形成的过程。在化学反应过程中,断裂化学键需要消耗能量,形成化学键又会释放能量。
(6)已知:
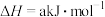 ,根据上表中所列键能数据可计算出a=
,根据上表中所列键能数据可计算出a=_______ 。
I.光伏材料是指能将太阳能直接转换成电能的材料。光伏材料又称太阳能材料,只有半导体材料具有这种功能。可作太阳能电池材料的有单晶硅、多晶硅、非晶硅、GaAs、GaAlAs、InP、CdS、CdTe等。
(1)写出31号元素镓(Ga)的原子结构示意图:
(2)P、S、Ga电负性从大到小的顺序为
(3)As元素的第一电离能
(4)写出原子序数最小的第VIII族元素基态原子的核外电子排布式:
(5)写出3p轨道上只有2个未成对电子的元素的符号:
II.从化学键的角度分析,化学反应的过程就是反应物的化学键断裂和生成物的化学键形成的过程。在化学反应过程中,断裂化学键需要消耗能量,形成化学键又会释放能量。
| 化学键 | H—H | N—H | N≡N |
| 键能/(kJ/mol) | 436 | 391 | 945 |

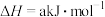 ,根据上表中所列键能数据可计算出a=
,根据上表中所列键能数据可计算出a=
22-23高二上·天津河北·期末 查看更多[3]
天津外国语大学附属外国语学校2022-2023学年高二上学期期末考化学试题(已下线)专题01 化学反应的热效应-【好题汇编】备战2023-2024学年高二化学上学期期末真题分类汇编(天津专用)(已下线)专项01 破解热化学方程式的书写-【好题汇编】备战2023-2024学年高二化学上学期期末真题分类汇编(天津专用)
更新时间:2023-02-19 18:38:16
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】回答下列问题。
(1)下列变化过程,属于放热是___________ 。
A.碳酸钙分解 B.氢气在氯气中燃烧 C.Ba(OH)2·8H2O与NH4Cl
D.铝热反应 E.酸碱中和反应 F.FeCl3水解
(2)①C(s)+O2(g)=CO2(g) =-437.3kJ/mol
=-437.3kJ/mol
②H2(g)+ O2(g)=H2O(g)
O2(g)=H2O(g)  =-285.8 kJ/mol
=-285.8 kJ/mol
③CO(g)+ O2(g)=CO2(g)
O2(g)=CO2(g)  =-283.0 kJ/mol
=-283.0 kJ/mol
固态碳和水蒸气反应生成CO和H2的热化学方程式为___________ 。
(3)根据键能数据估算CH4(g)+4F2(g)=CF4(g)+4HF(g)的反应热 为
为___________ 。
(4)标准状况下,3.36L仅由C、H元素组成的某气体质量4.5g完全燃烧生成CO2(g)和H2O(l)时,放出233.97kJ的热量。该气体的分子式为___________ ,热值为___________ kJ/g,该气体燃烧热的热化学方程式为___________ 。
(1)下列变化过程,属于放热是
A.碳酸钙分解 B.氢气在氯气中燃烧 C.Ba(OH)2·8H2O与NH4Cl
D.铝热反应 E.酸碱中和反应 F.FeCl3水解
(2)①C(s)+O2(g)=CO2(g)
 =-437.3kJ/mol
=-437.3kJ/mol②H2(g)+
 O2(g)=H2O(g)
O2(g)=H2O(g)  =-285.8 kJ/mol
=-285.8 kJ/mol③CO(g)+
 O2(g)=CO2(g)
O2(g)=CO2(g)  =-283.0 kJ/mol
=-283.0 kJ/mol固态碳和水蒸气反应生成CO和H2的热化学方程式为
(3)根据键能数据估算CH4(g)+4F2(g)=CF4(g)+4HF(g)的反应热
 为
为| 化学键 | C-H | C-F | H-F | F-F |
| 键能kJ/mol | 414 | 489 | 565 | 155 |
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】I.请根据有关知识,填写下列空白:
(1)下列反应中,属于吸热反应的是______ (填数字序号,下同),属于放热反应的是______ 。
①煅烧石灰石制生石灰;②氢氧化钠固体溶于水;③碳与水蒸气的反应;④酸碱中和反应;⑤生石灰与水作用制熟石灰;⑥食物因氧化而腐败
(2)已知H2和O2反应放热,且断开1 mol H−H、1 mol O=O、1 mol O−H键需要吸收的能量分别为Q1kJ、Q2kJ、Q3kJ,由此可以推知下列关系正确的是______ (填字母编号)。
A.Q1+ Q2> Q3 B.2Q1+ Q2<4Q3 C.Q1+Q2>2Q3 D.2Q1+Q2<2Q3
II.下列物质:①CaBr2 ②H2O ③NH4Cl ④H2O2 ⑤Na2O2 ⑥Ca(OH)2 ⑦HClO ⑧ I2
(3)只存在非极性键的是_____ (用序号填空,下同)。
(4)既含有共价键又含有离子键的是______________ 。
(5)当其熔化时,不破坏化学键的是______________ 。
(1)下列反应中,属于吸热反应的是
①煅烧石灰石制生石灰;②氢氧化钠固体溶于水;③碳与水蒸气的反应;④酸碱中和反应;⑤生石灰与水作用制熟石灰;⑥食物因氧化而腐败
(2)已知H2和O2反应放热,且断开1 mol H−H、1 mol O=O、1 mol O−H键需要吸收的能量分别为Q1kJ、Q2kJ、Q3kJ,由此可以推知下列关系正确的是
A.Q1+ Q2> Q3 B.2Q1+ Q2<4Q3 C.Q1+Q2>2Q3 D.2Q1+Q2<2Q3
II.下列物质:①CaBr2 ②H2O ③NH4Cl ④H2O2 ⑤Na2O2 ⑥Ca(OH)2 ⑦HClO ⑧ I2
(3)只存在非极性键的是
(4)既含有共价键又含有离子键的是
(5)当其熔化时,不破坏化学键的是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】已知,在铁触媒的催化下N2 (g)+ 3H2(g) 2NH3 (g) ∆H,请完成下列填空:
2NH3 (g) ∆H,请完成下列填空:
(1)反应过程的能量变化示意图如下图所示,已知N≡N和H-H的键能分别为946kJ·mol-1、436kJ·mol-1,则N-H的键能为________ kJ·mol-1。

(2)当达到平衡后,在某时刻降低温度,正、逆反应速率的变化情况符合像下图________(填“标号”)。
(3)下列措施能够提高H2平衡转化率的是________ 。
A升高温度 B增大压强 C.恒温恒压下通入Ar
D.恒温恒容下通入N2 E. 恒温恒容下通入H2 F.及时分离出NH3
(4)在一定温度下,在10L的密闭容器中充入3mol N2和10 mol H2和适量的铁触媒,产生NH3的物质的量变化情况如下表所示:
①在0~2min,用N2表示的化学反应速率v(N2)= ________ 。
②H2的平衡转化率为________ ,达到平衡时放出的热量为________ 。
③在该温度下,合成氨反应的化学平衡常数K=________ 可以不写“单位”)。
 2NH3 (g) ∆H,请完成下列填空:
2NH3 (g) ∆H,请完成下列填空:(1)反应过程的能量变化示意图如下图所示,已知N≡N和H-H的键能分别为946kJ·mol-1、436kJ·mol-1,则N-H的键能为

(2)当达到平衡后,在某时刻降低温度,正、逆反应速率的变化情况符合像下图________(填“标号”)。
A.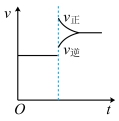 | B.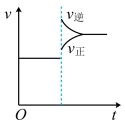 |
C.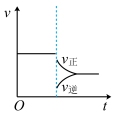 | D. |
(3)下列措施能够提高H2平衡转化率的是
A升高温度 B增大压强 C.恒温恒压下通入Ar
D.恒温恒容下通入N2 E. 恒温恒容下通入H2 F.及时分离出NH3
(4)在一定温度下,在10L的密闭容器中充入3mol N2和10 mol H2和适量的铁触媒,产生NH3的物质的量变化情况如下表所示:
| 时间t/min | 0 | 1 | 2 | 3 | 4 | 5 |
| N(NH3)/mol | 0 | 1.8 | 2.8 | 3.5 | 4 | 4 |
②H2的平衡转化率为
③在该温度下,合成氨反应的化学平衡常数K=
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】铬与氮能形成多种化合物,其中氮化铬(CrN)具有高的硬度和良好的耐磨性,是一种很受重视的耐磨涂层。将低碳铬铁在真空加热炉于1150℃氮化得到粗氮化铬铁,再经硫酸处理,除去铁杂质。经过滤、水洗、干燥,即得氮化铬。也可由氨和卤化铬反应制得。
(1)三价铬离子能形成多种配位化合物。 中提供电子对形成配位键的原子是N、O、Cl,配体是NH3、
中提供电子对形成配位键的原子是N、O、Cl,配体是NH3、___________ 和Cl- ,中心离子的配位数为___________ ,N、O、Cl原子半径较大的是___________ ,N和O电负性较大的是___________ ,N和O第一电离能较大的是___________ 。
(2)Cr是24号元素,则基态Cr核外电子排布式为___________ 。
(3) 中心原子轨道的杂化类型为
中心原子轨道的杂化类型为___________ 。
(4)元素As与N同族。预测As的氢化物分子的立体结构为___________ ,其沸点比 的
的___________ (填“高”或“低”),其判断理由___________ 。
(1)三价铬离子能形成多种配位化合物。
 中提供电子对形成配位键的原子是N、O、Cl,配体是NH3、
中提供电子对形成配位键的原子是N、O、Cl,配体是NH3、(2)Cr是24号元素,则基态Cr核外电子排布式为
(3)
 中心原子轨道的杂化类型为
中心原子轨道的杂化类型为(4)元素As与N同族。预测As的氢化物分子的立体结构为
 的
的
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】根据下表中五种元素的第一至第四电离能数据(单位:kJ·mol-1),回答下面各题:
(1)在周期表中,最可能处于同一族的是________ 。
A.Q和R B.S和T C.T和U D.R和T E.R和U
(2)下列离子的氧化性最弱的是________ 。
A.S2+ B.R2+ C.T3+ D.U+
(3)下列元素中,化学性质和物理性质最像Q元素的是________ 。
A.硼 B.铍 C.氦 D.氢
(4)如果R、S、T是同周期的三种主族元素,则它们的原子序数由小到大的顺序是_____________ ,其中元素________ 的第一电离能反常高。(用字母表示)
| 元素代号 | I1 | I2 | I3 | I4 |
| Q | 2 080 | 4 000 | 6 100 | 9 400 |
| R | 500 | 4 600 | 6 900 | 9 500 |
| S | 740 | 1 500 | 7 700 | 10 500 |
| T | 580 | 1 800 | 2 700 | 11 600 |
| U | 420 | 3 100 | 4 400 | 5 900 |
(1)在周期表中,最可能处于同一族的是
A.Q和R B.S和T C.T和U D.R和T E.R和U
(2)下列离子的氧化性最弱的是
A.S2+ B.R2+ C.T3+ D.U+
(3)下列元素中,化学性质和物理性质最像Q元素的是
A.硼 B.铍 C.氦 D.氢
(4)如果R、S、T是同周期的三种主族元素,则它们的原子序数由小到大的顺序是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】X、Y、Z、W、R是原子序数依次增大的前四周期元素,这五种元素的相关信息如下:
(1)基态R原子的电子排布式为________________ 。
(2)Y2分子中σ键和π键的数目比为________ 。
(3)X、Y、Z三种元素的第一电离能由小到大的顺序为____ (用元素符号表示),元素Y的简单气态氢化物的沸点比元素X的简单气态氢化物沸点高的主要原因是____ 。
(4)元素Z、W组成的微粒WZ42-的空间构型是_____ ,其中W原子的杂化轨道类型为_____ 。
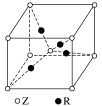
(5)已知Z、R能形成一种化合物,其晶胞结构如图所示,该化合物的化学式为______ ;若相邻的Z原子和R原子间的距离为acm,设阿伏加德常数的值为NA,则该晶体的密度为______ g·cm-3(用含a、NA的代数式表示)。
| 元素 | 相关信息 |
| X | 其中一种核素在考古时常用来鉴定一些文物的年代 |
| Y | 原子核外电子有7种不同的运动状态 |
| Z | 地壳中含量最高的元素 |
| W | 价电子排布式为(n+1)sn(n+1)pn+2 |
| R | 基态原子最外能层只有一个电子,其他能层均已充满电子 |
(1)基态R原子的电子排布式为
(2)Y2分子中σ键和π键的数目比为
(3)X、Y、Z三种元素的第一电离能由小到大的顺序为
(4)元素Z、W组成的微粒WZ42-的空间构型是
(5)已知Z、R能形成一种化合物,其晶胞结构如图所示,该化合物的化学式为

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】已知元素电负性的差值大于1.7时,原子间形成离子键,小于1.7时,原子间形成共价键,请指出下列原子之间形成的化学键是离子键还是共价键。
Be(1.5)和F(4.0):____________ ,Si(1.8)和Cl(3.0):____________ 。
Be(1.5)和F(4.0):
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】Ⅰ.完成下列问题
(1)依据第3周期元素第一电离能的变化规律,参照如图Mg、S元素的位置,用小黑点标出Al、Si、P三种元素的相对位置________ 。
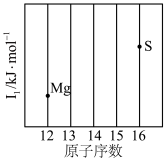
Ⅱ.元素的电负性是元素的一种基本性质,下面给出10种元素的电负性。
(2)通过分析电负性的变化规律,确定Mg元素电负性的最小范围___________ 。
(3)下列物质属于离子化合物的是___________
(1)依据第3周期元素第一电离能的变化规律,参照如图Mg、S元素的位置,用小黑点标出Al、Si、P三种元素的相对位置

Ⅱ.元素的电负性是元素的一种基本性质,下面给出10种元素的电负性。
| 元素 | Al | Be | Mg | C | Cl | Na | Li | N | Si | O | H |
| O电负性 | 1.5 | 1.5 | 2.5 | 3.0 | 0.9 | 1.0 | 3.0 | 1.8 | 3.5 | 2.1 |
(2)通过分析电负性的变化规律,确定Mg元素电负性的最小范围
(3)下列物质属于离子化合物的是___________
| A.BeCl2 | B.Li3N | C.HCl | D.CCl4 |
您最近一年使用:0次
【推荐3】依据原子结构知识回答:
(1) 基态原子的电子排布式是
基态原子的电子排布式是_______________________________ ;S的价层电子排布式是_________________ 。
(2)基态的 原子有
原子有______ 个未成对电子, 的外围电子排布图为
的外围电子排布图为______________ 。
(3)四种元素 、K、O、
、K、O、 中第一电离能最小的是
中第一电离能最小的是 _____ ,电负性最大的是 ______ 。
(4)下列有关微粒性质的排列顺序中,错误的是______ 。
A.元素的电负性: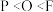
 元素的第一电离能:
元素的第一电离能: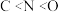
C.离子半径: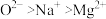
 原子的未成对电子数:
原子的未成对电子数:
(1)
 基态原子的电子排布式是
基态原子的电子排布式是(2)基态的
 原子有
原子有 的外围电子排布图为
的外围电子排布图为(3)四种元素
 、K、O、
、K、O、 中第一电离能最小的是
中第一电离能最小的是 (4)下列有关微粒性质的排列顺序中,错误的是
A.元素的电负性:
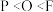
 元素的第一电离能:
元素的第一电离能: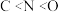
C.离子半径:
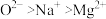
 原子的未成对电子数:
原子的未成对电子数:
您最近一年使用:0次



