回答下列问题。
(1)下列变化过程,属于放热是___________ 。
A.碳酸钙分解 B.氢气在氯气中燃烧 C.Ba(OH)2·8H2O与NH4Cl
D.铝热反应 E.酸碱中和反应 F.FeCl3水解
(2)①C(s)+O2(g)=CO2(g) =-437.3kJ/mol
=-437.3kJ/mol
②H2(g)+ O2(g)=H2O(g)
O2(g)=H2O(g)  =-285.8 kJ/mol
=-285.8 kJ/mol
③CO(g)+ O2(g)=CO2(g)
O2(g)=CO2(g)  =-283.0 kJ/mol
=-283.0 kJ/mol
固态碳和水蒸气反应生成CO和H2的热化学方程式为___________ 。
(3)根据键能数据估算CH4(g)+4F2(g)=CF4(g)+4HF(g)的反应热 为
为___________ 。
(4)标准状况下,3.36L仅由C、H元素组成的某气体质量4.5g完全燃烧生成CO2(g)和H2O(l)时,放出233.97kJ的热量。该气体的分子式为___________ ,热值为___________ kJ/g,该气体燃烧热的热化学方程式为___________ 。
(1)下列变化过程,属于放热是
A.碳酸钙分解 B.氢气在氯气中燃烧 C.Ba(OH)2·8H2O与NH4Cl
D.铝热反应 E.酸碱中和反应 F.FeCl3水解
(2)①C(s)+O2(g)=CO2(g)
 =-437.3kJ/mol
=-437.3kJ/mol②H2(g)+
 O2(g)=H2O(g)
O2(g)=H2O(g)  =-285.8 kJ/mol
=-285.8 kJ/mol③CO(g)+
 O2(g)=CO2(g)
O2(g)=CO2(g)  =-283.0 kJ/mol
=-283.0 kJ/mol固态碳和水蒸气反应生成CO和H2的热化学方程式为
(3)根据键能数据估算CH4(g)+4F2(g)=CF4(g)+4HF(g)的反应热
 为
为| 化学键 | C-H | C-F | H-F | F-F |
| 键能kJ/mol | 414 | 489 | 565 | 155 |
更新时间:2024-01-17 21:42:58
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】根据所学知识回答问题:
(1)写出下列反应的热化学方程式:
①NH3(气态)在高温高压催化剂下分解生成1mol N2(气态)与H2(气态),吸收92.2kJ的热量___________ 。
②1mol H2(气态)与适量O2(气态)起反应,生成H2O(液态)能放出285.8kJ的热量___________ 。
(2)工业上制二甲醚是在一定温度(230~280℃)、压强(2.0~10.0 MPa)和催化剂作用下进行的,反应器中发生了下列反应:
CO(g)+2H2(g) CH3OH(g)ΔH1=-90.7 kJ·mol-1①
CH3OH(g)ΔH1=-90.7 kJ·mol-1①
2CH3OH(g) CH3OCH3(g)+H2O(g) ΔH2=-23.5 kJ·mol-1②
CH3OCH3(g)+H2O(g) ΔH2=-23.5 kJ·mol-1②
CO(g)+H2O(g) CO2(g)+H2(g) ΔH3=-41.2 kJ·mol-1③
CO2(g)+H2(g) ΔH3=-41.2 kJ·mol-1③
反应器中的总反应可表示为3CO(g)+3H2(g) CH3OCH3(g)+CO2(g),计算该反应的ΔH=
CH3OCH3(g)+CO2(g),计算该反应的ΔH=___________ 。
(3)一定温度下,反应H2+Cl2═2HCl中的某一基元反应H2+Cl·→HCl+H·,其能量变化如图所示。 表示反应物分子中旧化学键没有完全断裂、新化学键没有完全形成的过渡态。
表示反应物分子中旧化学键没有完全断裂、新化学键没有完全形成的过渡态。
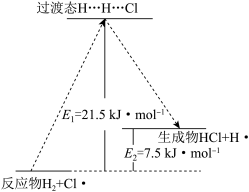
该基元反应的活化能为___________ kJ•mol-1,△H为___________ kJ•mol-1。
(1)写出下列反应的热化学方程式:
①NH3(气态)在高温高压催化剂下分解生成1mol N2(气态)与H2(气态),吸收92.2kJ的热量
②1mol H2(气态)与适量O2(气态)起反应,生成H2O(液态)能放出285.8kJ的热量
(2)工业上制二甲醚是在一定温度(230~280℃)、压强(2.0~10.0 MPa)和催化剂作用下进行的,反应器中发生了下列反应:
CO(g)+2H2(g)
 CH3OH(g)ΔH1=-90.7 kJ·mol-1①
CH3OH(g)ΔH1=-90.7 kJ·mol-1①2CH3OH(g)
 CH3OCH3(g)+H2O(g) ΔH2=-23.5 kJ·mol-1②
CH3OCH3(g)+H2O(g) ΔH2=-23.5 kJ·mol-1②CO(g)+H2O(g)
 CO2(g)+H2(g) ΔH3=-41.2 kJ·mol-1③
CO2(g)+H2(g) ΔH3=-41.2 kJ·mol-1③反应器中的总反应可表示为3CO(g)+3H2(g)
 CH3OCH3(g)+CO2(g),计算该反应的ΔH=
CH3OCH3(g)+CO2(g),计算该反应的ΔH=(3)一定温度下,反应H2+Cl2═2HCl中的某一基元反应H2+Cl·→HCl+H·,其能量变化如图所示。
 表示反应物分子中旧化学键没有完全断裂、新化学键没有完全形成的过渡态。
表示反应物分子中旧化学键没有完全断裂、新化学键没有完全形成的过渡态。
该基元反应的活化能为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】能源是人类生活和社会发展的基础,研究化学反应中的能量变化,有助于更好地利用化学反应为生产和生活服务。阅读下列有关能源的材料,回答有关问题:
(1)从能量的角度看,断开化学键要___ ,形成化学键要___ 。
(2)焙烧产生的SO2可用于制硫酸。已知25℃、101kPa时:
①2SO2(g)+O2(g) 2SO3(g)ΔH1=-197kJ/mol;
2SO3(g)ΔH1=-197kJ/mol;
②H2O(g)=H2O(l)ΔH2=-44kJ/mol;
③2SO2(g)+O2(g)+2H2O(g)=2H2SO4(l)ΔH3=-545kJ/mol。
写出SO3(g)与H2O(l)反应的热化学方程式是____ 。
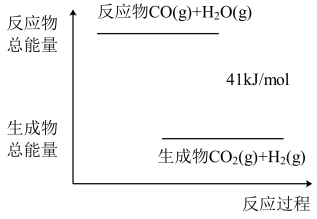
(3)已知一定条件下,CO(g)+H2O(g) CO2(g)+H2(g)反应过程能量变化如图所示,该反应为
CO2(g)+H2(g)反应过程能量变化如图所示,该反应为___ 反应(填“吸热”或“放热”)。
(4)已知热化学方程式:SO2(g)+ O2(g)
O2(g) SO3(g)ΔH=-98.32kJ/mol,在容器中充入2molSO2和1molO2充分反应,最终放出的热量为
SO3(g)ΔH=-98.32kJ/mol,在容器中充入2molSO2和1molO2充分反应,最终放出的热量为_____ 。
A.98.32kJ B.196.64kJ/mol C.<196.64kJ D.>196.64kJ
(1)从能量的角度看,断开化学键要
(2)焙烧产生的SO2可用于制硫酸。已知25℃、101kPa时:
①2SO2(g)+O2(g)
 2SO3(g)ΔH1=-197kJ/mol;
2SO3(g)ΔH1=-197kJ/mol;②H2O(g)=H2O(l)ΔH2=-44kJ/mol;
③2SO2(g)+O2(g)+2H2O(g)=2H2SO4(l)ΔH3=-545kJ/mol。
写出SO3(g)与H2O(l)反应的热化学方程式是
(3)已知一定条件下,CO(g)+H2O(g)
 CO2(g)+H2(g)反应过程能量变化如图所示,该反应为
CO2(g)+H2(g)反应过程能量变化如图所示,该反应为
(4)已知热化学方程式:SO2(g)+
 O2(g)
O2(g) SO3(g)ΔH=-98.32kJ/mol,在容器中充入2molSO2和1molO2充分反应,最终放出的热量为
SO3(g)ΔH=-98.32kJ/mol,在容器中充入2molSO2和1molO2充分反应,最终放出的热量为A.98.32kJ B.196.64kJ/mol C.<196.64kJ D.>196.64kJ
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】用CO2制备甲醇的反应原理为:CO2(g)+3H2(g) CH3OH(g)+H2O(g)。该反应进程可通过如图所示的两步反应实现。
CH3OH(g)+H2O(g)。该反应进程可通过如图所示的两步反应实现。
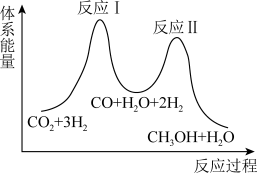
回答下列问题:
(1)反应I的化学方程式是____ 。
(2)由图可知,反应____ (填“I”或“II”)为慢反应。
(3)反应II:CO(g)+2H2(g) CH3OH(g) △H
CH3OH(g) △H____ 0(填“>”“<”或“=”)。
(4)在容积可变的密闭容器中投入0.5molCO和1molH2,发生反应:CO(g)+2H2(g) CH3OH(g),测得平衡时CH3OH的物质的量随温度、压强变化如图所示。
CH3OH(g),测得平衡时CH3OH的物质的量随温度、压强变化如图所示。

①P总1____ P总2(填“>”“<”或“=”),判断理由是____ 。
②若P总1=0.25MPa,则500K时该反应的平衡常数Kp=____ MPa-2。
 CH3OH(g)+H2O(g)。该反应进程可通过如图所示的两步反应实现。
CH3OH(g)+H2O(g)。该反应进程可通过如图所示的两步反应实现。
回答下列问题:
(1)反应I的化学方程式是
(2)由图可知,反应
(3)反应II:CO(g)+2H2(g)
 CH3OH(g) △H
CH3OH(g) △H(4)在容积可变的密闭容器中投入0.5molCO和1molH2,发生反应:CO(g)+2H2(g)
 CH3OH(g),测得平衡时CH3OH的物质的量随温度、压强变化如图所示。
CH3OH(g),测得平衡时CH3OH的物质的量随温度、压强变化如图所示。
①P总1
②若P总1=0.25MPa,则500K时该反应的平衡常数Kp=
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】Ⅰ.(1)从能量的变化和反应的快慢等角度研究反应:2H2(g)+O2(g)=2H2O(g)。已知该反应为放热反应,下图能正确表示该反应中能量变化的是___________ 。
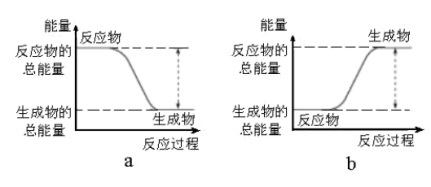
从断键和成键的角度分析上述反应中能量的变化,化学键的键能如下表所示:
则生成1molH2O(g)可以放出热量___________ kJ。
(2)下列反应中,既属于氧化还原反应,又属于放热反应的是___________
a.盐酸与烧碱溶液反应 b.柠檬酸和碳酸氢钠反应
c.氢气在氧气中燃烧生成水 d.高温煅烧石灰石使其分解
e.铝和盐酸反应 f.浓硫酸溶于水
Ⅱ.A、B、C、D 四种金属按下表中装置进行实验。
根据实验现象回答下列问题:
①装置甲中溶液中的阴离子移向___________ 极(填“A”或“B”)。
②装置乙中正极的电极反应式为___________ 。
③装置丙中溶液的pH___________ (填“变大”“变小”或“不变”)。
④四种金属活动性由强到弱的顺序是___________ 。

从断键和成键的角度分析上述反应中能量的变化,化学键的键能如下表所示:
| 化学键 | H-H | O=O | H-O |
| 键能(kJ·mol-1) | 436 | 496 | 463 |
则生成1molH2O(g)可以放出热量
(2)下列反应中,既属于氧化还原反应,又属于放热反应的是
a.盐酸与烧碱溶液反应 b.柠檬酸和碳酸氢钠反应
c.氢气在氧气中燃烧生成水 d.高温煅烧石灰石使其分解
e.铝和盐酸反应 f.浓硫酸溶于水
Ⅱ.A、B、C、D 四种金属按下表中装置进行实验。
| 装置 | 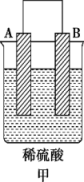 | 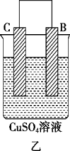 | 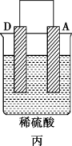 |
| 现象 | 二价金属A不断溶解 | C的质量增加 | A上有气体产生 |
根据实验现象回答下列问题:
①装置甲中溶液中的阴离子移向
②装置乙中正极的电极反应式为
③装置丙中溶液的pH
④四种金属活动性由强到弱的顺序是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】请根据所学知识回答下列问题。
(1) 受热分解释放出
受热分解释放出 可引发白磷(
可引发白磷( )燃烧,31g
)燃烧,31g 完全燃烧生成五氧化二磷固体释放出akJ热量。下列说法中不正确的是
完全燃烧生成五氧化二磷固体释放出akJ热量。下列说法中不正确的是_______ (填字母)。
A. 的分解过程中只有共价键断裂没有共价键生成
的分解过程中只有共价键断裂没有共价键生成
B.若白磷完全燃烧释放出8akJ热量,则需要标准状况下 的体积为224L
的体积为224L
C.易燃易爆物应远离火源
(2)天然气已经成为我国主要的民用清洁能源,但天然气与空气混合达到一定比例后遇明火会发生爆炸,所以安全使用天然气,防止发生爆炸是极为重要的。已知天然气的主要成分甲烷( )燃烧时的能量变化如图所示:
)燃烧时的能量变化如图所示:
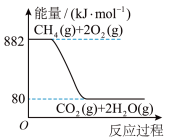
请回答下列问题。
①下列说法中正确的是_______ (填字母)。
A.天然气属于清洁能源,所以它属于新能源
B.甲烷完全燃烧时化学能全部转化为热能
C.标准状况下,44.8L甲烷完全燃烧时有8mol极性键断裂
D.用天然气做饭时,为使甲烷充分燃烧,通入的空气越多越好
② (g)完全燃烧时生成18g气态水放出的热量是
(g)完全燃烧时生成18g气态水放出的热量是_______ kJ。
③若家庭做饭需64160kJ热量,假设天然气(按 算)的热效率为80%,则需要天然气的质量为
算)的热效率为80%,则需要天然气的质量为_______ g。
(1)
 受热分解释放出
受热分解释放出 可引发白磷(
可引发白磷( )燃烧,31g
)燃烧,31g 完全燃烧生成五氧化二磷固体释放出akJ热量。下列说法中不正确的是
完全燃烧生成五氧化二磷固体释放出akJ热量。下列说法中不正确的是A.
 的分解过程中只有共价键断裂没有共价键生成
的分解过程中只有共价键断裂没有共价键生成B.若白磷完全燃烧释放出8akJ热量,则需要标准状况下
 的体积为224L
的体积为224LC.易燃易爆物应远离火源
(2)天然气已经成为我国主要的民用清洁能源,但天然气与空气混合达到一定比例后遇明火会发生爆炸,所以安全使用天然气,防止发生爆炸是极为重要的。已知天然气的主要成分甲烷(
 )燃烧时的能量变化如图所示:
)燃烧时的能量变化如图所示:
请回答下列问题。
①下列说法中正确的是
A.天然气属于清洁能源,所以它属于新能源
B.甲烷完全燃烧时化学能全部转化为热能
C.标准状况下,44.8L甲烷完全燃烧时有8mol极性键断裂
D.用天然气做饭时,为使甲烷充分燃烧,通入的空气越多越好
②
 (g)完全燃烧时生成18g气态水放出的热量是
(g)完全燃烧时生成18g气态水放出的热量是③若家庭做饭需64160kJ热量,假设天然气(按
 算)的热效率为80%,则需要天然气的质量为
算)的热效率为80%,则需要天然气的质量为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】碳是形成化合物种类最多的元素,其单质及其化合物是人类生产生活的主要能源物质。已知: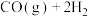
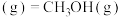
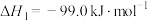 。
。
(1)该反应的熵变
_______ 0(填“>”“<”“=”),该反应自发进行的条件是_______ (填“低温”“高温”或“任意温度”)。
(2)反应
 ,则
,则
_______  (填“>”“<”“=”)。
(填“>”“<”“=”)。
(3)已知1g液态甲醇完全燃烧放出的热量为22.7kJ(298K、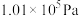 时测定)。写出该条件下表示甲醇燃烧热的热化学方程式
时测定)。写出该条件下表示甲醇燃烧热的热化学方程式_______ 。
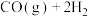
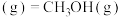
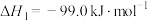 。
。(1)该反应的熵变

(2)反应

 ,则
,则
 (填“>”“<”“=”)。
(填“>”“<”“=”)。(3)已知1g液态甲醇完全燃烧放出的热量为22.7kJ(298K、
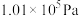 时测定)。写出该条件下表示甲醇燃烧热的热化学方程式
时测定)。写出该条件下表示甲醇燃烧热的热化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】回答下列问题:
(1)已知1mol烃B中所含电子总数为66NA,且C、H两种元素的质量比为16:3,则其分子式为___________ ,在它的同分异构体中,一氯代物只有一种的是___________ (写结构简式)。
(2)已知:①C(s)+O2(g)=CO2(g);△H=-393.51kJ·mol-1
②C(s)+ O2(g)=CO(g);△H=-110.5kJ·mol-1
O2(g)=CO(g);△H=-110.5kJ·mol-1
则反应C(s)+CO2(g)=2CO(g)的△H=___________ 。
(3)已知1g氢气完全燃烧生成液态水可放出热量143kJ,则氢气燃烧热的热化学方程式:______ 。
(4)涤纶的结构简式为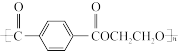 ,写出其单体的结构简式
,写出其单体的结构简式___________ 。
(5) 的核磁共振氢谱吸收峰面积之比:
的核磁共振氢谱吸收峰面积之比:___________ 。
(1)已知1mol烃B中所含电子总数为66NA,且C、H两种元素的质量比为16:3,则其分子式为
(2)已知:①C(s)+O2(g)=CO2(g);△H=-393.51kJ·mol-1
②C(s)+
 O2(g)=CO(g);△H=-110.5kJ·mol-1
O2(g)=CO(g);△H=-110.5kJ·mol-1则反应C(s)+CO2(g)=2CO(g)的△H=
(3)已知1g氢气完全燃烧生成液态水可放出热量143kJ,则氢气燃烧热的热化学方程式:
(4)涤纶的结构简式为
 ,写出其单体的结构简式
,写出其单体的结构简式(5)
 的核磁共振氢谱吸收峰面积之比:
的核磁共振氢谱吸收峰面积之比:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】(1)请用下列4种物质的序号填空:①O2 ②NH4NO3 ③K2O2 ④NH3,既有离子键又有极性键的是________ 。
请按要求完成下列问题:
(2)已知丙烷(C3H8)的燃烧热是-2219.9kJ/mol,请写出丙烷燃烧的热化学方程式:_________________________________________ 。
(3)当它氧化生成1g H2O(l)时放出的热量是:______________________________ 。
(4)已知下列热化学方程式:
①H2(g)+ O2(g)=H2O(l) ΔH=-285.8kJ·mol-1
O2(g)=H2O(l) ΔH=-285.8kJ·mol-1
②H2(g)+ O2(g)=H2O(g) ΔH=-241.8kJ·mol-1
O2(g)=H2O(g) ΔH=-241.8kJ·mol-1
③C(s)+O2(g)=CO(g) ΔH=-110.5kJ·mol-1
④C(s)+O2(g)=CO2(g) ΔH=-393.5kJ·mol-1
回答下列问题:
①H2的燃烧热ΔH为______ ;C的燃烧热为______ 。
②燃烧1g H2生成液态水,放出的热量为________ 。
③已知CO的燃烧热为283.0kJ·mol-1,现有CO、H2和CO2组成的混合气体116.8L(标准状况),完全燃烧后放出总能量为867.9kJ,且生成18g液态水,则混合气体中H2为______ L,CO在混合气体中的体积分数约为______ (精确至小数点后2位)。
请按要求完成下列问题:
(2)已知丙烷(C3H8)的燃烧热是-2219.9kJ/mol,请写出丙烷燃烧的热化学方程式:
(3)当它氧化生成1g H2O(l)时放出的热量是:
(4)已知下列热化学方程式:
①H2(g)+
 O2(g)=H2O(l) ΔH=-285.8kJ·mol-1
O2(g)=H2O(l) ΔH=-285.8kJ·mol-1②H2(g)+
 O2(g)=H2O(g) ΔH=-241.8kJ·mol-1
O2(g)=H2O(g) ΔH=-241.8kJ·mol-1③C(s)+O2(g)=CO(g) ΔH=-110.5kJ·mol-1
④C(s)+O2(g)=CO2(g) ΔH=-393.5kJ·mol-1
回答下列问题:
①H2的燃烧热ΔH为
②燃烧1g H2生成液态水,放出的热量为
③已知CO的燃烧热为283.0kJ·mol-1,现有CO、H2和CO2组成的混合气体116.8L(标准状况),完全燃烧后放出总能量为867.9kJ,且生成18g液态水,则混合气体中H2为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】下表中的数据表示破坏1mol化学键需消耗的能量(即键能,单位为kJ·mol−1)。回答问题
(1)下列关于键能的叙述正确的是___________(填字母,下同)。
(2)已知热化学方程式:H2(g)+Cl2(g)=2HCl(g) ΔH=-183kJ·mol−1,则Cl2的键能为___________ kJ·mol−1。
(3)参考下表中的数据,判断下列分子受热时最稳定的是___________。
(4)能用键能大小解释的是___________。
| 化学键 | H-H | H-Cl |
| 键能 | 436 | 431 |
| A.每生成1molH-Cl吸收431.4kJ能量 |
| B.每生成1molH-Cl放出431.4kJ能量 |
| C.每拆开1molH-Cl放出431.4kJ能量 |
| D.每拆开1molH-Cl吸收431.4kJ能量 |
(3)参考下表中的数据,判断下列分子受热时最稳定的是___________。
| 化学键 | H-H | H-F | H-Cl | H-Br |
| 键能/(kJ·mol-1) | 436 | 565 | 431 | 368 |
| A.H2 | B.HF | C.HCl | D.HBr |
| A.常温常压下,溴呈液态,碘呈固态 | B.氮气的化学性质比氧气稳定 |
| C.稀有气体一般很难发生化学反应 | D.硝酸易挥发而硫酸难挥发 |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】化学反应是人类获取能量的重要途径,我们可以通过化学反应实现化学能向热能、电能的直接转化。
I.回答下列问题:
(1)从断键和成键角度分析上述反应中能量的变化。部分化学键的键能如下表:
则常温常压下,1mol H2 在空气中充分燃烧,生成 1mol H2O (g)放出热量______ kJ。
II.各类电池广泛用在交通工具(如电动汽车、电动自行车等)上,实现了节能减排,也为生活带来了极大的便利。
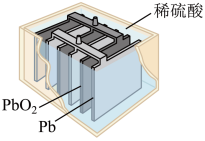
(2)传统汽车中使用的电池主要是铅蓄电池,其构造如图所示。
①电池工作时,电子由___________ 流出(填“Pb”或“ PbO2”)
②该电池的工作原理为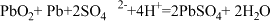 ,其工作时电解质溶液的 pH 将
,其工作时电解质溶液的 pH 将___________ (填“增大”“减小”或“不变”)。
(3)2020 年上海进博会展览中,诸多氢能源汽车纷纷亮相,氢氧燃料电池被誉为氢能源汽车的心脏。某种氢氧燃料电池的内部结构如图所示:
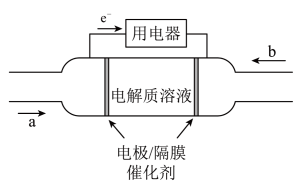
①a 处通入的气体是___________ ;
②电池每消耗标准状况下 5.6L 氢气,电路中通过的电子数目为___________ 。
III.为了更好地利用化学反应中物质和能量的变化,在化学研究和工业生产中还需要关注化学反应的快慢和限度。能量、速率与限度是认识和研究化学反应的重要因素。某温度下,向2.0L 的恒容密闭容器中充入 2.0mol N2 和 2.0mol H2 ,发生反应,实验数据如下表所示:
(4)0~50s 内的平均反应速率v(N2)=___________ 。
(5)为加快反应速率,可采取的措施是___________ (填字母)。
a.升高温度 b.增大容器体积 c.加入合适的催化剂
I.回答下列问题:
(1)从断键和成键角度分析上述反应中能量的变化。部分化学键的键能如下表:
| 化学键 | H-H | 0=0 | H-O |
| 键能(kJ/mol) | 436 | 496 | 463 |
II.各类电池广泛用在交通工具(如电动汽车、电动自行车等)上,实现了节能减排,也为生活带来了极大的便利。
(2)传统汽车中使用的电池主要是铅蓄电池,其构造如图所示。

①电池工作时,电子由
②该电池的工作原理为
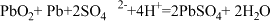 ,其工作时电解质溶液的 pH 将
,其工作时电解质溶液的 pH 将(3)2020 年上海进博会展览中,诸多氢能源汽车纷纷亮相,氢氧燃料电池被誉为氢能源汽车的心脏。某种氢氧燃料电池的内部结构如图所示:

①a 处通入的气体是
②电池每消耗标准状况下 5.6L 氢气,电路中通过的电子数目为
III.为了更好地利用化学反应中物质和能量的变化,在化学研究和工业生产中还需要关注化学反应的快慢和限度。能量、速率与限度是认识和研究化学反应的重要因素。某温度下,向2.0L 的恒容密闭容器中充入 2.0mol N2 和 2.0mol H2 ,发生反应,实验数据如下表所示:
| t/s | 0 | 50 | 150 | 250 | 350 |
| n(NH3)/mol | 0 | 0.24 | 0.36 | 0.40 | 0.40 |
(4)0~50s 内的平均反应速率v(N2)=
(5)为加快反应速率,可采取的措施是
a.升高温度 b.增大容器体积 c.加入合适的催化剂
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】化学反应过程中释放或吸收的热量在生活、生产、科技及科学研究中具有广泛的应用。
(1)冷敷袋在日常生活中有降温、保鲜和镇痛等用途。制作冷敷袋利用_____ (填“放热”或“吸热”)的化学变化或物理变化的原理。
(2)“即热饭盒”给人们生活带来方便,它可利用下面_____ (填字母)反应释放的热量加热食物。
A.生石灰和水 B.浓硫酸和水 C.钠和水
(3)已知:2molH2与足量O2充分燃烧生成液态水时放出572kJ热量。
①该反应的能量变化可用图中的_____ (填字母“a”或“b”)表示。
②写出H2燃烧生成液态水的热化学反应方程式:_____ 。
(4)同温同压下,H2(g)+Cl2(g)=2HCl(g),在光照和点燃条件下的△H(化学计量数相同)分别为△H1、△H2,△H1_____ △H2(填“>”“<”或“=”)。
(5)已知H-H键键能为436kJ•mol-1,H-N键键能为391kJ•mol-1,根据热化学方程式:N2(g)+3H2(g) 2NH3(g) △H=-92.4kJ•mol-1,则N≡N键键能是
2NH3(g) △H=-92.4kJ•mol-1,则N≡N键键能是_____ 。
(6)“神舟”系列火箭用偏二甲肼(C2H8O2)作燃料,N2O4作氧化剂,反应后产物无污染。
已知:反应1:N2(g)+2O2(g)=N2O4(g) △H1=xkJ•mol-1
反应2:C2H8N2(1)+4O2(g)=N2(g)+2CO2(g)+4H2O(g) △H2=ykJ•mol-1
写出C2H8O2(l)和N2O4(g)反应生成N2(g)、CO2(g)、H2O(g)的热化学方程式_____ 。
(1)冷敷袋在日常生活中有降温、保鲜和镇痛等用途。制作冷敷袋利用
(2)“即热饭盒”给人们生活带来方便,它可利用下面
A.生石灰和水 B.浓硫酸和水 C.钠和水
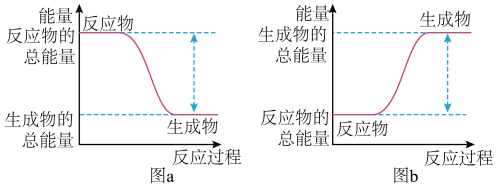
(3)已知:2molH2与足量O2充分燃烧生成液态水时放出572kJ热量。
①该反应的能量变化可用图中的

②写出H2燃烧生成液态水的热化学反应方程式:
(4)同温同压下,H2(g)+Cl2(g)=2HCl(g),在光照和点燃条件下的△H(化学计量数相同)分别为△H1、△H2,△H1
(5)已知H-H键键能为436kJ•mol-1,H-N键键能为391kJ•mol-1,根据热化学方程式:N2(g)+3H2(g)
 2NH3(g) △H=-92.4kJ•mol-1,则N≡N键键能是
2NH3(g) △H=-92.4kJ•mol-1,则N≡N键键能是(6)“神舟”系列火箭用偏二甲肼(C2H8O2)作燃料,N2O4作氧化剂,反应后产物无污染。
已知:反应1:N2(g)+2O2(g)=N2O4(g) △H1=xkJ•mol-1
反应2:C2H8N2(1)+4O2(g)=N2(g)+2CO2(g)+4H2O(g) △H2=ykJ•mol-1
写出C2H8O2(l)和N2O4(g)反应生成N2(g)、CO2(g)、H2O(g)的热化学方程式
您最近一年使用:0次

 CO(g)+ 3H2(g) ΔH=+206.4kJ·mol-1,则制得56g CO需要吸收的热量为
CO(g)+ 3H2(g) ΔH=+206.4kJ·mol-1,则制得56g CO需要吸收的热量为

